緩和ケアとは「生命を脅かす病に関連する問題に直面している患者とその家族のQOLを,痛みやその他の身体的・心理社会的・スピリチュアルな問題を早期に見出し的確に評価を行い対応することで,苦痛を予防し和らげることを通して向上させるアプローチである」1)と定義されている.我が国では2021年改訂版 循環器疾患における緩和ケアについての提言2)において,心不全に対する緩和ケアはstage Cの段階から心不全治療と並行し提供するよう記載されている.しかし,先天性心疾患の性質上,心疾患における終末期を迎える経過は,急性増悪を繰り返しながら徐々に全身の機能が低下するという特徴がある.そのため治療が全身状態の改善や苦痛の緩和につながることがあり,予後予測や延命治療中止の判断が難しい3).我が国における緩和ケアはがんへの対応が中心となり発展した歴史があり,非がん疾患に対する緩和ケアに関する教育や研修の場を提供する必要性が認識されたのが比較的近年である.緩和ケア講習として日本心不全学会が開催する基本的心不全緩和ケアトレーニングコース(HEPT: heart failure palliative care training program for comprehensivecare provider)4)が2019年から導入されたが,心不全への緩和ケアを勉強する機会が少なく,具体的な提供内容は担当者に委ねられていることが多かったことも,小児の心不全緩和ケアを苦手とする医師が多い要因と考えられる.
我が国では,緩和ケア評価ツールとして,がん緩和ケアにおける評価尺度のSTAS(support team assessment schedule)が広く使用されてきた歴史がある5).STASは原則として医療者が評価する尺度であるが,世界的に「患者の声を聴くことが重要である」という患者報告型アウトカムを推進する動きが時代と共に加速し,その後IPOS(integrated palliative care outcome scale)が開発された6).IPOSは,患者報告型アウトカムであると同時に,他者からの評価が可能な緩和ケア評価ツールであるため,患者の自覚する症状と他者の認識に乖離がないかを判断することが可能である.また自己評価が困難となった場合においても,同一ツールで評価を継続することが可能である.IPOSはがん患者の緩和ケアにおける評価目的に使用される場合が多いが,身体症状などの物理的な項目で信頼性の高いツールとして認識されており6, 7),成人の心不全患者にも用いられている8).小児での日本語版IPOSの使用報告はないが,患者報告型に加えて他者から評価も可能である点が,患者の認知機能や判断力に差の大きい小児において評価がしやすいと考え,今回IPOSを用いて小児末期心不全患者に緩和ケア評価を行った.
IPOSの利用方法
IPOSの概要
近年,慢性心不全患者においても緩和ケアの重要性が再評価されており,慢性心不全の評価ツールとしてMinnesota Living with Heart Failure Questionnaire9),Quality of Life in Severe Heart Failure Questionnaire10)などが存在する.これらは心肺運動負荷試験により運動生理学的指標との関連で妥当性を評価するが,項目数が多く,回答する患者の負担が大きいことが問題となり11),小児には不向きである.IPOSは17問のみで質問数が限られており,質問項目も簡便であるため,患者自身での回答がより容易である.
IPOSの使用方法
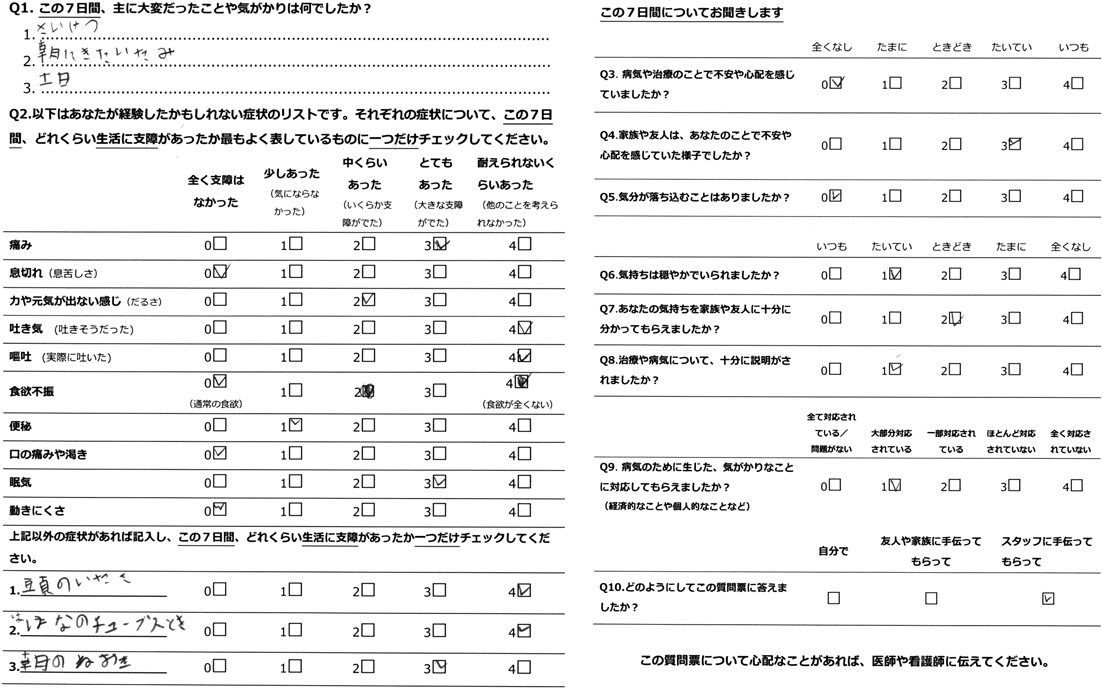
IPOSは,身体的苦痛10項目(痛み,息切れ,倦怠感,嘔気,嘔吐,食欲不振,便秘,口渇感,眠気,動きにくさ),心理的苦痛5項目(患者の不安,家族の不安,気分の落ち込み,気分の穏やかさ,気持ちの共有),社会的苦痛2項目(情報の説明,問題に対する対応)について計17項目で質問を行う.対象者は過去3日間もしくは7日間を振り返り,0~4の5段階で評価する.支障が大きいほど高い点数となる.患者版とスタッフ版の2種類のテンプレートが用意されている.
症例
8歳3か月女児.
病歴
無脾症候群,右室型単心室,共通房室弁,両大血管右室起始,肺動脈弁狭窄の診断で,9か月時に両側グレン手術,共通房室弁形成術が行われた.1歳0か月時に再度共通房室弁形成術を行ったが,心収縮不良のため1歳1か月時に冠動脈自己幹細胞移植が行われた.4歳3か月時での心臓カテーテル検査の結果,肺高血圧は認めないものの右室駆出率26%と心収縮不良があり,フォンタン手術のリスクが高いと判断され,心不全治療を行う方針となり,在宅酸素療法を開始した.学校生活管理指導表の指導区分はC管理で生活していた.同時期に転居に伴いA病院に紹介となり,外来通院を開始した.入院を要さず経過していたが,小学2年生の冬である8歳0か月時に感冒を契機に心不全の増悪を認め,入院管理となった.
発達
7歳0か月で行ったWISC-IVで,全検査IQ 107,言語理解指標129と平均~平均の上の水準であり,特に言語理解が優れているとの結果であった.
生活背景
学校は通常学級に通学し,徒歩で登校できていた.
家族背景
両親,妹の4人家族.母,母方祖母がミトコンドリア脳筋症と診断されている.
内服薬
カプトプリル15 mg/day,ジゴキシン0.05 mg/day,フロセミド12 mg/day,スピロノラクトン12 mg/day,アスピリン35 mg/day,クラリスロマイシン40 mg/day
入院時現症
身長115.9 cm(−1.6SD),体重16.9 kg(−2.3SD),血圧92/51 mmHg,心拍数111回/分,呼吸数30回/分,SpO2 82%(酸素1.5 L/分Nasal cannula(NC)),心音:整,胸骨左縁第3肋間を最強点とする全収縮期雑音LevineII/VI,呼吸音:清,腹部:平坦・軟,腸蠕動音減弱,末梢冷感軽度
入院時検査所見
血液検査:WBC 12,800/µL, Hb 17.5 g/dL, Plt 25.3万/µL, Alb 3.9 g/dL, AST 223 U/L, ALT 130 U/L, LDH 468 U/L, T-Bil 4.1 mg/dL, Cr 0.52 mg/dL, UN 21.1 mg/dL, Na 132 mmol/L, K 4.6 mmol/L, Cl 100 mmol/L, CRP 5.13 mg/dL, hANP 729 pg/mL, BNP 2,710 pg/mL
胸部Xp検査
心胸郭比66%,肺うっ血所見を認めた.
心臓超音波検査
右側相同,右室型単心室,共通房室弁,肺動脈弁狭窄,左上大静脈遺残,両側グレン手術後.右室心尖部はほぼ収縮認めず,右室はfractional area change 4%と心収縮は不良.共通房室弁逆流を中等度認めた.
入院後経過
頭痛,胸痛,嘔気などの身体症状は低心拍出に伴う諸症状と考え,入院後にドブタミン3.3 µg/kg/min,ミルリノン0.1 µg/kg/min,フロセミド2 mg/kg/dayの静注を開始した.利尿と共に,血清カリウム値が2.6 mmol/Lと低下を認めたため電解質の補正を行った.入院3日目にフロセミドの静注から内服に変更し,トリクロルメチアジド1.6 mg/dayの追加投与を行った.入院6日目に胸痛と呼吸困難の訴えがあり,High-flow nasal cannula(HFNC)を15 L/min FiO2 0.5で開始し,呼吸状態の改善を認めた.ベッド上での安静が続き,入院15日目から病棟歩行やストレッチなどのリハビリテーションを開始した.経過中にドブタミンの漸減を試みたが,血清BNP上昇と,胸痛,頭痛の頻度が増加したため,ドブタミンを増量し,アセトアミノフェン10 mg/kg/doseの頓服使用を開始した.心不全が増悪傾向にあり,緩和ケアの介入を要すると判断したため,入院19日目に担当医師から患児,両親へ病状の説明を行った.重症な心不全であり改善には時間がかかることを伝えたうえで,IPOSを使用して緩和ケアの評価を行う方針とした.IPOSは,緩和ケアの評価方法であると両親に説明し,患児へは困りごとを解決するための質問表であると説明した.
初回のIPOS評価
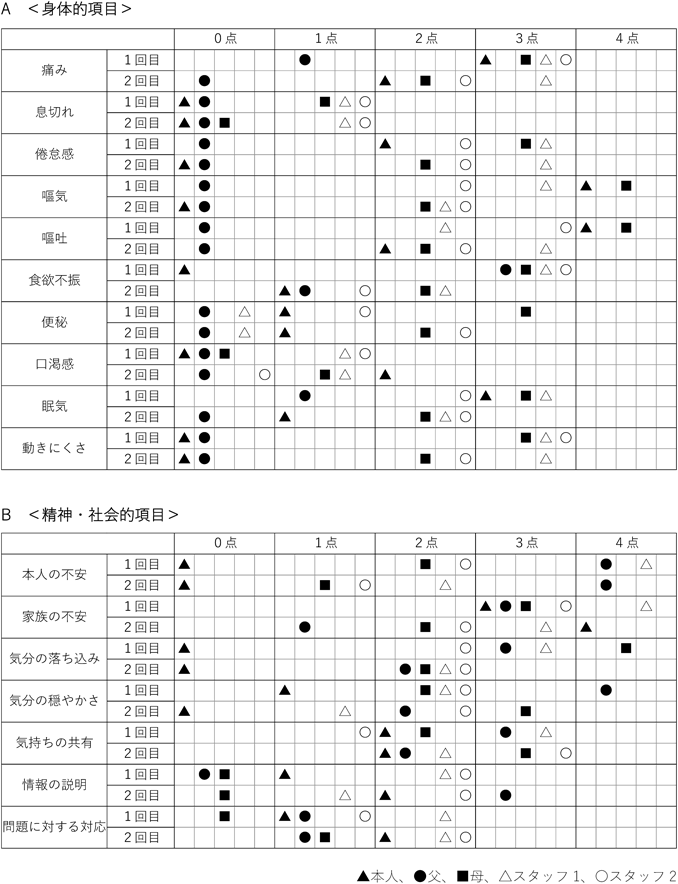
入院20日目に初回のIPOS評価を行った.IPOSは,直近の7日間を振り返る7日間版を使用した(Fig. 1)6).患児,両親,患児との関わりが深いスタッフ4名(担当医師2名,担当看護師2名)が回答した(Fig. 2A, B).回答者を選定するにあたり,特別な研修は条件としなかった.患児の評価は担当医師が口頭で質問し,一部代筆を行った.スコアリングは,IPOSに記載の通りの表現方法(全く支障がなかった=0点,耐えがたいほど支障があった=4点)を,全然困らなかった,我慢できないくらい困った,と表現を変更した.患者自身の評価は,20~30分程度かけて質問し記載を行った.患児が3点以上の高い点数を付けた項目は,「痛み,嘔気,嘔吐,眠気,家族の不安」であった.患児は,家族の不安に対して高い点数を記録した一方,自身の不安や落ち込みについては極端に低い点数を記録した.スタッフの平均では,「痛み,患者の不安,家族の不安」の項目で3点以上の高い点数を記録した.患児とスタッフ平均との差が3点以上の大きな乖離があった項目は,「食欲不振,動きにくさ,患者の不安,気分の落ち込み」で,いずれも患児の点数と比べてスタッフが高い点数を記録していた.母とスタッフの評価は,身体的,精神的苦痛の項目は大きな差異を認めなかった.面会時間が制限されていた父は,身体的項目に対する評価において,患児の評価と比較すると全体的に低い点数を記録した.
初回IPOS評価後の介入
小児循環器科医師,血液・腫瘍科医師,精神科医師,看護師,ソーシャルワーカー,心理士,の緩和ケアチームで多職種カンファレンスを開き,患児の訴えと医療スタッフの認識を共有した.
身体面への介入:「痛み」の点数が高く,鎮痛薬の使用が不十分である点が問題点にあがった.アセトアミノフェンの内服を頓服使用としていたが,1日1回の定期内服に変更し,症状出現前の鎮痛薬使用を心掛けた.また「眠気」に対し,夜間の入眠困難が原因と考え,ラメルテオンの内服を2 mg/dayから開始した.介入後,胸痛や呼吸困難を訴える頻度は減少し,表情はおだやかとなった.
精神面への介入:不安に対して,病状説明や予後についてどこまで知りたいか,知りたくないかを確認し,説明に取り入れた.IPOSを実施する過程で,母と衝突する時間が増えていると発言があり,終日同室であり母子が2人で過ごす時間が長いことへのストレスも問題点として考えられた.院内学級や病棟外のリハビリ室を利用して母子分離を進める方針としたが,全身状態の悪化により病棟外への移動が困難であり,リハビリ室への移動は叶わず,院内学級はベッドサイドでの授業を行うこととなった.母児同室を敢えて避けることで,母と児が衝突する時間は軽減された.
2回目のIPOS評価
入院45日目に,2回目のIPOS評価を行った.患児,両親,担当看護師2名が回答した(Fig. 2A, B).IPOSは7日間版を使用し,患児の評価は担当医師が口頭で質問し,一部代筆を行った.患児が評価した身体的項目に対するIPOSの点数は,「倦怠感,嘔気,眠気」で2点以上の改善を認め,治療介入により患児の身体的症状は改善を認めた.患児が3点以上の高い点数を付けた項目は,精神的項目の「家族の不安」のみであり,1回目と同様に自身の不安や落ち込みは低い点数を記録した.身体項目の「倦怠感,動きにくさ」,精神的項目の「気分の落ち込み」では,いずれも患児の点数と比べてスタッフがより高い点数を記録していた.母のIPOSの評価では,「嘔気,嘔吐,気分の落ち込み」の項目で2点以上の改善を認めた.社会的項目では患児,両親,スタッフ平均で大きな差を認めなかった.
2回目IPOS評価後の介入
評価結果をもとに再度多職種カンファレンスを行い,患児が現在困っている事柄や患児の希望を確認した.
身体面への介入:身体的項目での評価は,スタッフと患児に大きな差はなく,症状の改善があるため新たな介入は行わなかった.
精神面への介入:患児は,前回に引き続き「家族の不安」に高い点数をつけており,家族が心配していることを気にかける発言をしていた.また,祖母と妹との面会を希望したため,面会制限を解除し,祖母,妹との面会の機会を設けた.聞き取りの中で,嗜好品摂取を希望する発言が多かった.患児はカップ麺などの塩分の多い食品を好み,持ち込み食の制限解除で病状が悪化する懸念があったため,病棟での持ち込み食を一時禁止としていたが,患児が補食を希望した際はその都度医師が可否を判断し,極力緩和する方針とした.
2回目のIPOS介入以降の経過
入院50日目から浮腫の増悪を認め,胸痛,腹痛,呼吸困難を訴える頻度が増加し,入院70日目アルブミン製剤5%の持続投与を行ったが,症状の改善は認めなかった.入院72日目から激しい胸痛の出現を認め,アセトアミノフェンを20 mg/kg/doseへ増量した.持続鎮静について,さらに苦痛が増強した場合オピオイドを含む鎮静薬使用の検討を行ったが,重度の心機能低下があり,血圧低下による病状の急変を懸念し,まずはアセトアミノフェン,ヒドロキシジン塩酸塩の使用を継続した.入院81日目に激しい胸痛の訴えがあり,オピオイド持続投与の開始を検討したが,患児と家族を含めて相談のうえで投与は行わず,数時間内に徐脈となり同日死亡した.
小児慢性心不全の緩和ケアについて
小児慢性心不全における緩和ケアの現状
「緩和ケアの関与を行うことで親の希望を損なう可能性がある」と小児循環器科医は考える傾向にあるとの報告があり12),緩和ケアは治療による回復が望めない患者に行うものという従来の緩和ケアの考え方をしている医師が多いことが,積極的に緩和ケアが行われない要因の一つと考えられる.
慢性心不全患者への介入
慢性心不全患者には疼痛や倦怠感,食欲不振,不眠など多彩な身体症状・精神症状が出現することが知られている13).倦怠感が生じる要因の一つとして電解質異常があげられる.心不全の治療薬である利尿剤は,副作用として電解質異常を生じることがあり注意が必要である.本症例でも電解質補正を行い症状は改善したが,終末期では胸痛や倦怠感,呼吸困難の症状が増悪した.疼痛に対しては,まずはアセトアミノフェンの使用を検討し,鎮痛補助薬の使用を考慮した上で,同薬剤でも効果不十分の場合はオピオイドの使用を検討するとされている2).本症例でも疼痛に対してはアセトアミノフェンを使用し,一部改善が認められた.入院当初から呼吸困難を認めたが,心不全治療と呼吸補助を行うことで呼吸困難は改善傾向となり,入院当初はオピオイドの使用は検討しなかった.2回目のIPOS評価時点では呼吸困難の訴えはなく,介入は検討しなかったが,病状の悪化に伴い呼吸困難が再度増悪した.オピオイドを含む鎮静薬使用の検討を行うも,血圧低下による病状の急変を懸念して使用が躊躇された.また,苦痛を和らげるためにオピオイドの使用も選択肢にあることを患児に説明したところ,副作用に眠気があることを懸念して「自分らしく最後を迎えたい」と患児が使用しない事を希望したため,オピオイドはいったん使用せず,家族と会話をしながら時間を過ごした.本症例の患児は発達が良好で病識があり,家族,スタッフから見て「患児の意思決定能力は十分にある」と考えて意見を尊重した.小児の場合は発達段階や判断能力において差が大きいため,患者の成熟度や意向を把握し,子どもの自己決定権や事前の意向をどこまで考慮するべきか検討し,日常的に患者の性格や価値観を把握することが重要である14).
コントロールが困難な呼吸困難や疼痛に対してはオピオイドが有用とされ,低用量モルヒネの使用は循環動態に影響を及ぼすことなく呼吸困難の改善が期待できる15).一方,小児の心不全患者でモルヒネが使用された際の有害事象の有無や程度はほとんど知られていない.本症例においても,終末期の心不全患者へのオピオイド使用経験の蓄積がないことが使用を躊躇した一因となった.症状緩和のコントロールが困難で耐え難い苦痛がある場合は,持続鎮静やオピオイド導入も選択肢に入れる必要がある.
小児へのIPOSの使用について
IPOSの使用方法と妥当性
IPOSでは,17問の簡便な質問項目について,0~4点で評価を行う.一般的に数値評価スケールの使用可能年齢は8歳から,フェイススケールの使用は4歳から可能とされており16),視覚的な補助を用いることで学童期の小児での使用も可能であると考える.本症例は,精神発達が良好な8歳児であり,IPOSの質問内容を医療者が読み上げることで,患児への質問聴取がベッドサイドでも可能であった.2019年にリリースされたIPOS日本語版は成人においては信頼性の高いツールであり7),身体症状などの物理的な項目では妥当性と信頼性があるが,スタッフ版での心理社会的項目の評価には不十分とされている17).小児ではIPOSの使用報告はなく,妥当性は検討されていない.しかし今回,IPOS回答の介助を行うなかで,自身の現状の受け止め方や恐怖心の有無,病状説明に対して望むことを患児から直接聴取することができた.小児では,表現力や説明力が発展途上であるため,患者の言葉から具体的な苦痛の要素を十分に把握することが難しい場合がある.本人の表情や仕草,保護者の意見,理学所見を含めて多角的に評価を行っているが,患者自身で言語化できない場合でも,IPOSを用いることで,苦痛に感じている事柄を表出する機会を得られることが,IPOSの利用の利点だと考える.
IPOS評価結果の解釈と再評価について
初回のIPOS評価では,スタッフと母は「身体的項目」について共に高い点数を記載したが,患児は低い点数を記載した.患児はIPOSの回答を行うなかで,身体的,心理的な苦痛を認めないことで病気に抵抗していると受け取れる発言や,家族が心配していることを気にかける発言をしており,作為的に低い点数を記載した可能性があった.小児の疼痛は心理的,発達的な要因も影響するため,回答に至った心理的な背景や患者の性格を考慮し評価する必要がある.アセトアミノフェンの積極的使用や,眠剤を使用した睡眠コントロールなどにより身体的な苦痛緩和を行い,2回目のIPOS評価では患児と他者の両者で改善を認めた.身体症状の評価において,患児と母の評価は大きな差を認めなかったが,父の評価は0点が目立った.病院の感染対策の方針により父の面会時間が制限されていた背景があり,評価の正確さは患者と接する機会の多さに大きく依存する可能性がある.同様にスタッフ間のIPOSの点数についても,受け持った回数や当日の患者の状況によっても点数が乖離する可能性があり,適切な評価を行うためにはスタッフへの教育が必要だと思われる.
緩和ケア評価の再評価の時期については一定の基準はないが,過去の報告では手術などの介入前後で再評価が行われている18).本症例では,心不全に対する治療はすでに開始しており,苦痛の緩和に対する介入前後の評価として3週間程度で再評価を行った.2回目の評価後も2週間毎を目途に定期的な評価を行う予定であったが,患児の病状が悪化したため2回目の評価が最後となった.病状が悪化して苦痛が増している時も代理人の評価が可能であるIPOSを利用して緩和評価を検討できた可能性がある.IPOS再評価のタイミングについては議論の余地があるものの,当院では子どもの反応や病状の変化が見られた時や,介入後2~3週間が経過した時を再評価の目安としている.
緩和ケア評価として,IPOSを医療スタッフに対する緩和ケアのトレーニングに利用した報告19)がある.本症例では,IPOSの結果から患児の苦痛や重視する事柄を医療スタッフが認識し,その推移を経時的に評価して看護計画の内容に加えるなど,対応に変化がみられた.普段緩和ケアになじみのない医師や病棟スタッフが,緩和ケアにおいてアセスメントすべき事柄を認識でき,そのアセスメントに基づき介入を行うことで患児の苦痛が取り除かれた点で有用なツールであると考えられた.本稿を通じて緩和ケアの評価が全国に浸透し,小児心不全に対する緩和ケアのレベルアップが図られていくことを期待したい.
引用文献References
1) 大坂 巌,渡邊清高,志真泰夫,ほか:わが国におけるWHO緩和ケア定義の定訳—デルファイ法を用いた緩和ケア関連18団体による共同作成—.Palliative Care Research 2019; 14: 61–66
2) 日本循環器学会/日本心不全学会合同ガイドライン:2021年改訂版 循環器疾患における緩和ケアについての提言.一般社団法人日本循環器学会.https://www.j-circ.or.jp/cms/wp-content/uploads/2021/03/JCS2021_Anzai.pdf
3) 宮下光令,柴 信行,下川宏明:末期心不全の緩和ケアを考える.心臓2012; 2: 501–511
4) HEPT:心不全緩和ケアトレーニングコース.http://hept.main.jp/
5) 石井容子,宮下光令:【患者報告型アウトカム—患者の体験をケアに活かす—】がん看護において患者報告型アウトカムとして使われる主なツール IPOS.がん看護2020; 25: 624–629
6) 宮下光令:患者・医療者による緩和ケアの質の評価Integrated Palliative care Outcome Scale: IPOS(日本語版)使用マニュアルver0.6. IPOS(IPOS日本語版).http://plaza.umin.ac.jp/pos/IPOS_manual_ver0.6.pdf
7) Sakurai H, Miyashita M, Imai K, et al: Validation of the Integrated Palliative care Outcome Scale (IPOS). Jpn J Clin Oncol 2019; 49: 257–262
8) Hamatani Y, Iguchi M, Ikeyama Y, et al: Comprehensive symptom assessment using Integrated Palliative care Outcome Scale in hospitalized heart failure patients. ESC Heart Fail 2022; 9: 1963–1975
9) Rector TS, Kubo SH, Cohn JN: Patient’s self-assessment of their congestive heart failure: Content, reliability, and validity of a new measure, the Minnesota living with heart failure questionnaire. Heart Fail 1987; 3: 198–209
10) Wiklund I, Lindvall K, Swedberg K, et al: Self-assessment of quality of life in severe heart failure: An instrument for clinical use. Scand J Psychol 1987; 28: 220–225
11) 田村政近,大宮一人,山田純生:慢性心不全患者のための疾患特異的生活の質(QOL)尺度の開発.J Cardiol 2003; 42: 155–164
12) Balkin EM, Sleeper LA, Kirkpatrick JN, et al: Physician perspectives on palliative care for children with advanced heart disease: A comparison between pediatric cardiology and palliative care physicians. J Palliat Med 2018; 21: 773–779
13) Goodlin SJ, Wingate S, Albert NM, et al: PAIN-HF Investigators: Investigating pain in heart failure patients: The pain assessment, incidence, and nature in heart failure (PAIN-HF) study. J Card Fail 2012; 18: 776–783
14) 多田羅竜平:ICUにおける小児患者と緩和ケア.ICUとCCU 2022; 46: 101–106
15) Kawaguchi J, Hamatani Y, Hirayama A, et al: Experience of morphine therapy for refractory dyspnea as palliative care in advanced heart failure patients. J Cardiol 2020; 75: 682–688
16) von Baeyer CL: Children’s self-reports of pain intensity: Scale selection, limitations and interpretation. Pain Res Manag 2006; 11: 157–162
17) Sakurai H, Miyashita M, Morita T, et al: Comparison between patient-reported and clinician-reported outcomes: Validation of the Japanese version of the integrated palliative care outcome scale for staff. Palliat Support Care 2021; 19: 1–7
18) Pinheiro LC, McFatrich M, Lucas N, et al: Child and adolescent self-report symptom measurement in pediatric oncology research: A systematic literature review. Qual Life Res 2018; 27: 291–319
19) Collins SE, Witt J, Bausewein C, et al: A systematic review of the use of the palliative care outcome scale and the support team assessment schedule in palliative care. J Pain Symptom Manage 2015; 50: 842–853