リンパ管腫症(generalized lymphatic anomaly; GLA)は,中枢神経を除く全身の臓器にリンパ管組織が増殖する希少性難治性疾患で,小児・若年者に多く発症する1).胎生20週前のリンパ管形成期に起こる異常が原因とされているが,いまだ詳細な原因は不明である.浸潤臓器によって骨溶解や乳び胸,心嚢水,縦隔病変,腹水,肝脾臓浸潤,リンパ浮腫,血液凝固異常などの多彩な臨床症状を示す2).一方,ゴーハム病(Gorham-Stout disease; GSD)は全身の骨が溶解する疾患で,溶解した部位は血管やリンパ管組織に置換する3).乳び胸などの症状を呈する報告があり,臨床的にGLAとの区別が困難なことが多い4).これらは多彩な症状を呈し,社会的認知度も低く,特発性胸水などとして診断されていない症例も存在している可能性がある.
今回,3歳時に発熱・嘔吐を契機に心タンポナーデが見つかり緊急ドレナージを施行し,当時は細菌性心膜炎と診断したが,肺間質陰影の増強が改善せず徐々に易疲労感を認めるようになり,収縮性心膜炎との鑑別に難渋し,緊急ドレナージ術から6年後に骨病変を契機にGLA/GSD病の診断に至った症例を経験したので報告する.
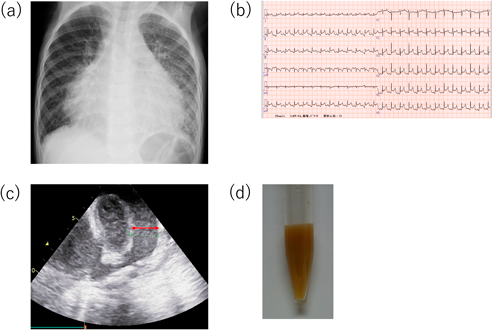
現在11歳の女児で,3歳時に発熱,嘔吐のため前医を受診した際,胸部X線で心拡大を,心エコー検査で心嚢液貯留を認めたため当院に緊急搬送となった.胸部X線で著明な心拡大を認め(Fig. 1a),心電図では広範囲の誘導でST上昇を認めた(Fig. 1b).心臓超音波検査で明らかな疣贅や有意な弁逆流は認めなかったが,大量の心嚢液貯留を認めた(Fig. 1c).呼吸は努力様であり,末梢冷感も著明で,呼びかけにも反応は乏しく心タンポナーデによるショックと診断した.緊急で心嚢ドレナージ術を行い,400 mLの膿性排液を認めた(Fig. 1d).排液の成分は,白血球を認めたが芽球は認めず,糖が2 mg/dLと低値を示し,乳びではなかった.また,心嚢液から化膿性連鎖球菌(Group A Streptococci; GAS)が検出された.インフルエンザウイルスなどの各種ウイルス抗原は全て陰性であり,腹部など他臓器の感染源検索も行ったが異常はなく,GASによる細菌性心膜炎と診断した.その他の原因検索に免疫能も調べたが,抗核抗体などの自己抗体は全て陰性であり,血清補体値や免疫グロブリン値,好中球貪食能や殺菌能などいずれも異常は認めなかった.術後経過は良好で,ガイドラインや過去の報告を参考に,抗生剤点滴加療を2週間行い退院,その後外来で6週間抗生剤内服加療を行った5, 6).
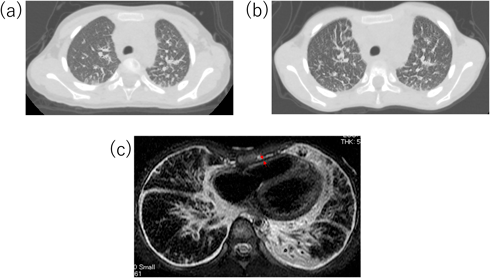
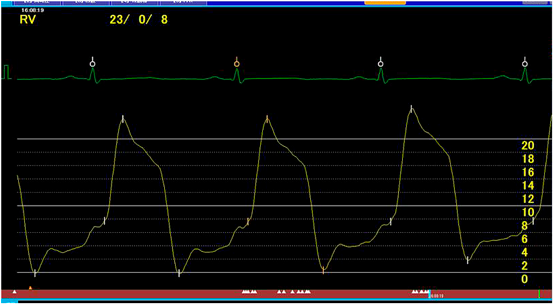
しかし,治療終了後も胸部X線で肺間質陰影の増強が改善せず,発症から3カ月後の胸部単純computed tomography(CT)検査で肺小葉間隔壁の肥厚を認めた(Fig. 2a).本人の自覚症状は特になく,肺線維化マーカーの上昇を認めず,心嚢液再貯留も認めなかったため,外来経過観察を継続した.外来経過観察中,下腿浮腫や肝腫大など右心不全症状は認めず,心臓超音波検査も繰り返し行われたが,心機能は良好で心嚢液の再貯留もなく,拡張障害も明らかでなかった.しかし,胸部X線所見は改善せず,発症後5年頃から徐々に易疲労感を認めるようになったため8歳時に胸部単純CT検査を再検したところ,肺小葉間隔壁の肥厚は悪化していた(Fig. 2b).心筋症の鑑別に心臓MRIを撮像し,心筋の肥厚や菲薄化は認めず遅延造影も陰性で心筋症は否定的であったが,心膜肥厚を認め(Fig. 2c),収縮性心膜炎が鑑別に挙がった.その精査のため,また心筋症の鑑別のため,9歳時に心臓カテーテル検査を行った.その時の圧データをTable 1に,右室圧曲線をFig. 3に示す.右室拡張末期圧の上昇を認めず,右室圧波形もdip and plateau型を示しておらず,収縮性心膜炎も否定的な所見であった.心筋生検も行ったが,錯綜配列などは認めず心筋症も否定された.
Table 1 Cardiac catheter examination at the age of 9 years| site | Pressure (mmHg) |
|---|
| LV | 88/10 |
| Ao | 76/52/63 |
| RV | 23/8 |
| MPA | 19/10/14 |
| RPA | 16/10/13 |
| RPAW | 8 |
| LPA | 20/9/14 |
| LPAW | 9 |
| SVC | 6/5/4 |
| RA | 9/9/5 |
| IVC | 5/5/4 |
| Ao, aorta; IVC, inferior vena cava; LPA, left pulmonary artery; LPAW, left pulmonary artery wedge; LV, left ventricle; MPA, main pulmonary artery; RA, right atrium; RPA, right pulmonary artery; RPAW, right pulmonary artery wedge; RV, right ventricle; SVC, superior vena cava |
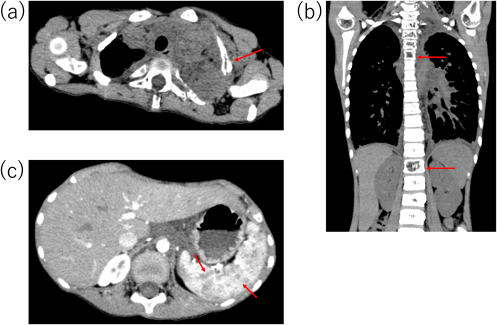
今後の治療方針を検討していたところ,心臓カテーテル検査後6カ月後頃から徐々に肋骨の突出が目立つようになり,圧痛も認めるようになった.造影CT検査を再検したところ,左第1・2肋骨の骨皮質欠損・骨溶解像(Fig. 4a)に加え,椎体の骨折(Fig. 4b),脾臓に多数の嚢胞状造影不良域(Fig. 4c)を認めた.特徴的な画像所見を有し,これまでの臨床経過と合わせてGLA/GSDの診断に至った.現在シロリムス内服治療を開始し約2年経過しているが,骨皮質は改善傾向で症状の増悪は認めていない.
今回,3歳時に心タンポナーデを発症し,当時は細菌性心膜炎と診断していたが,ドレナージ術後も肺間質陰影の増強が改善せず,9歳時に骨病変を機に希少疾患であるGLA/GSDの診断に至った1例を経験した.
GLA/GSDによる心嚢液貯留はこれまでほとんど報告がなく,我々が検索し得た限り2例のみ症例報告があった7, 8).Swelstadらは,基礎疾患のない31歳の症例に合併した乳び心嚢液を報告し,胸部CTで認めた特徴的な骨融解像からGSDの診断に至っているが7),我々の症例では乳び心嚢液を認めなかった.また,Koernerらは,我々の症例と同様に,心嚢液からGASが陽性となり,後にGLA/GSDのサブタイプであるKaposi肉腫様GLAの診断に至った4歳男児例を報告している7).この報告でも免疫能に関して詳細に調べられているが,我々の症例と同様に明らかな異常は認めなかったとされている.心膜炎とは異なるが,GASは感染性心内膜炎の起因菌としては非常に稀とされている一方,水痘感染後にGASによる重症感染症を発症することがある6).しかし,本症例や過去の報告7)でもそのような先行感染はなく,GASによる細菌性心膜炎を発症した原因は明らかにできなかった.
GLA/GSDは,中枢神経系を除く骨や胸部(肺,縦隔,心臓),腹部(腹腔内,脾臓),皮膚,皮下組織など全身臓器にびまん性に異常に拡張したリンパ管組織が浸潤する,原因不明の希少性難治性疾患で,国内の推定患者数は約100人と言われている9).男女差や遺伝性はなく,小児,若年者に多いと考えられている.骨溶解を起こすGSDも,骨病変だけでなく同様の内臓病変を持つ場合があるため,類縁疾患と考えられ,現時点では一つの疾患としてとらえられている.症状は病変の浸潤部位により,胸部に生じた場合は胸水,乳び胸,心タンポナーデ,心不全など,また肺浸潤による息切れ,咳,喘鳴,呼吸苦,慢性呼吸不全を起こす.胸部単純X線写真やCT検査では,びまん性に広がる肥厚した間質陰影や胸水貯留,胸膜肥厚,心嚢水を認める.また骨に生じると,骨溶解,骨欠損による疼痛や病的骨折などを起こす.腹部に生じると,腹水や,脾臓内およびほかの腹腔内臓器に多発性の嚢胞性リンパ管腫病変を認める9).2018年に改訂されたThe International Society for the Study of Vascular Anomalies(ISSVA)分類では,脈管異常は内皮細胞の増殖性変化を有する脈管性腫瘍と,内皮細胞の増殖を認めず脈管の構造異常を主体とする脈管奇形に大別される.脈管奇形のうちの単純型にリンパ管奇形が含まれ,そのなかにGLA/GSDは含まれる10).診断基準をTable 2に示す.(1)のa)~c)のうち一つ以上の主要所見を満たし,(2)の病理所見を認めた場合に診断する.病理検査が困難な症例は,a)~c)のうち一つ以上の主要所見を満たし,臨床的に除外疾患を否定できる場合に限り,診断可能とされている.本症例は病理検査を行っていないが,骨溶解,心タンポナーデの既往,脾臓のリンパ管腫症様病変と主要所見のa)~c)を全て満たし,これまでの経過からリンパ管造影などのさらなる画像検査は行っていないが,GLA/GSDと診断した.
Table 2 リンパ管腫症・ゴーハム病の診断基準| (1)主要所見 | a) | 骨皮質もしくは髄質が局在性もしくは散在性に溶解(全身骨に起こりうる) |
| b) | 肺,縦隔,心臓など胸腔内臓器にびまん性にリンパ管腫様病変,またはリンパ液貯留 |
| c) | 肝臓,脾臓など腹腔内臓器にびまん性にリンパ管腫様病変,またはリンパ液貯留 |
| (2)病理学的所見 | 組織学的には,リンパ管内皮によって裏打ちされた不規則に拡張したリンパ管組織よりなり,一部に紡錘形細胞の集簇を認めることがある. |
| 特記事項 | 除外疾患;リンパ脈管筋腫症などの他のリンパ管疾患や悪性新生物による溶骨性疾患,遺伝性先端骨溶解症,特発性多中心性溶骨性腎症,遺伝性溶骨症候群などの先天性骨溶解疾患. |
| リンパ管奇形(リンパ管腫)が明らかに多発もしくは浸潤拡大傾向を示す場合には,リンパ管腫症と診断する. |
本症例は3歳時に心タンポナーデを発症したが,心嚢液貯留の原因に,ウイルスや細菌による感染性,膠原病・悪性疾患・外傷・心膜切開後症候群などの非感染性がある.本症例は外傷の既往はなく,精査の結果,膠原病や悪性疾患も否定され,心嚢液からGASを認めたことや糖濃度が低い結果などより当初細菌性心膜炎と診断した.抗生物質治療が進んだ現在の先進国では細菌性心膜炎は稀な疾患であるが,いったん発症すると急速に心タンポナーデとなり,循環動態の破綻を来しうる重篤な疾患である11).心電図は広範な誘導におけるST上昇が特徴的であり12),本症例も同様の所見を認めた.今回感染症状で発症し,感染性心内膜炎(infective endocarditis; IE)も鑑別に挙げる必要があるが,修正Duke診断基準は満たさず,また,IEの起因菌としてGASは非常に稀である5, 6).以上より初診時は細菌性心膜炎と診断し,抗生剤治療を行ったが,治療終了後も胸部X線で肺間質陰影の増強が改善せず,心嚢ドレナージ後の収縮性心膜炎が鑑別に挙がった.
収縮性心膜炎は,心膜の肥厚が原因とされ,成人では4 mm以上の壁厚が肥厚と判定される13).心臓超音波検査における拡張障害や,心臓カテーテル検査における心内圧曲線でdip and plateauが特徴的とされる.dip and plateau波形は,ゼロ以下の拡張期下降から急峻な立ち上がりで拡張期plateauに続き,拡張期plateau圧は収縮期の3分の1を超えるとされている14).本症例は心膜肥厚を疑う所見を認め(Fig. 2),心臓超音波検査で拡張障害は明らかでなかったが,その時点ではGLA/GSD病は鑑別に挙がっておらず,病歴からも収縮性心膜炎の可能性が高いと考えられたため,心臓カテーテル検査を行った.しかし,心臓カテーテル検査でもdip and plateau型の心内圧曲線は認めず(Fig. 3),収縮性心膜炎は否定的であり,心筋生検も行ったが心筋症も否定された.
その後骨病変を機にGLA/GSDの診断に至った.厚生労働省難治性疾患克服研究事業のリンパ管腫症研究班が定めた「リンパ管腫症・ゴーハム病の診断基準」では,Table 2に示したように,主要臓器である骨,胸部,腹部のなかの一つ以上の臓器にリンパ管組織やリンパ液が貯留すること,および病理学的検査で鑑別すべき疾患を否定し,拡張したリンパ管内皮細胞を証明することによって診断可能であるが,病理検査がない場合でもほかの疾患を否定できれば臨床的に診断可能となっている15).また,診断基準となる必須項目の画像診断は胸部CTの特徴的所見とされており,本症例ではリンパ管造影を施行しなかった.本症例は心タンポナーデ発症から診断までに6年を要した.その間様々な検査を行ったが肺間質陰影増強の原因特定に至らず,今回病理検査は行っていないが収縮性心膜炎など他疾患も否定できたため,特徴的な画像所見と合わせ臨床的にGLA/GSDと診断した.
最後にGLA/GSDとGAS感染との関連に関して考察する.
我々が調べ得た限り,GLA/GSDとGAS感染を合併した報告は,本症例とKoernerらの報告7)の2例のみである.本症例は3歳時に細菌性心膜炎を発症し,当時の検査では乳び心嚢液を認めず,リンパ管障害を疑うことはできなかった.その後9歳時に骨病変を契機にGLA/GSDの診断に至っている.またKoernerらが報告した4歳男児例7)は,心タンポナーデ発症とほぼ同時期に骨病変を呈し,GLA/GSDのサブタイプであるKaposi肉腫様リンパ管腫症の診断に至っている.KoernerらもGAS感染とGLA/GSDの関連に関しては言及しておらず,我々の症例もGASによる細菌性心膜炎罹患後6年が経過してからGLA/GSD診断に至ったが,GAS感染がGLA/GSDの発病に関連しているのか,それとも細菌性心膜炎に罹患した後に偶然GLA/GSDを発病したのかは明らかにできなかった.
心タンポナーデに対するドレナージ術後の収縮性心膜炎との鑑別に難渋したが,特徴的な画像所見からGLA/GSDの診断に至った症例を経験した.心タンポナーデは小児循環器領域で時に遭遇する病態であるが,その鑑別に本症例のような希少疾患があることを知っておくことが重要である.
利益相反
著者およびすべての共著者において日本小児循環器学会が定める利益相反に関する開示事項はありません.
著者の役割
浅田大,森雅啓,松尾久実代は患者の診療に従事,データ集計を行った.
浅田大,石井陽一郎は論文原稿作成を行った.
石井陽一郎,青木寿明は,論文の重要な知的内容に関わる批判的校閲に関与した.
付記
匿名性を十分に確保したうえで,本報告に関するインフォームドコンセントを保護者から書面にて取得している.
引用文献References
1) 小関道夫,藤野明浩,松岡健太郎,ほか:リンパ管腫症・ゴーハム病.日本臨床2015; 73: 1777–1788
2) Blei F: Lymphangiomatosis: Clinical overview. Lymphat Res Biol 2011; 9: 185–190
3) Gorham LW, Wright AW, Shultz HH, et al: Disappearing bones: A rare form of massive osteolysis; report of two cases, one with autopsy findings. Am J Med 1954; 17: 674–682
4) Lala S, Mulliken JB, Alomari AI, et al: Gorham-Stout disease and generalized lymphatic anomaly: Clinical, radiologic, and histologic differentiation. Skeletal Radiol 2013; 42: 917–924
5) 2017年改訂版 感染性心内膜炎の予防と治療に関するガイドライン
6) 白井加奈子,土井庄三郎,森田華奈子,ほか:A群溶連菌による咽頭感染から感染性心内膜炎を発症した房室中隔欠損術後症例.心臓2015; 47: 748–753
7) Koerner T, Patel MD, Pai V, et al: Kaposiform lymphangiomatosis presenting with a Group A Streptococcus pericardial effusion. BMJ Case Rep 2022; 15: e246250
8) Swelstad MR, Frumiento C, Garry-McCoy A, et al: Chylotamponade: An unusual presentation of Gorham’s syndrome. Ann Thorac Surg 2003; 75: 1650–1652
9) Ozeki M, Fujino A, Matsuoka K, et al: Clinical features and prognosis of generalized lymphatic anomaly, kaposiform lymphangiomatosis, and gorham-stout disease. Pediatr Blood Cancer 2016; 63: 832–838
10) The International Society for the Study of Vascular Anomalies (ISSVA): ISSVA classification for Vascular Anomalies. https://www.issva.org/UserFiles/file/ISSVA-Classification-2018.pdf
11) Sagristà-Sauleda J, Barrabés JA, Permanyer-Miralda G, et al: Purulent pericarditis: Review of a 20-year experience in a general hospital. J Am Coll Cardiol 1993; 22: 1661–1665
12) Allen HD, Shaddy RE, Penny DJ, et al: Moss and Adam’s Heart disease in Infant, Children, and Adolescent. 8th ed., LWW, 2013: pp1350–1362
13) 日本小児循環器学会:小児・成育循環器病学.診断と治療社,2018, pp592–594
14) 小柳 仁,門間和夫,鈴木 紳:新・心臓カテーテル法.南江堂,pp180–182
15) 難治性血管腫・脈管奇形・血管奇形・リンパ管腫・リンパ管腫症および関連疾患についての調査研究班:血管腫・脈管奇形・血管奇形・リンパ管奇形・リンパ管腫症 診療ガイドライン2022