緊急心嚢ドレナージを要したコクサッキーウイルスA2性急性心膜炎の小児例A Case of Pediatric Pericarditis Caused by Coxsackievirus A2 Requiring Pericardial Drainage
滋賀医科大学 小児科学講座Department of Pediatrics, Shiga University of Medical Science
滋賀医科大学 小児科学講座Department of Pediatrics, Shiga University of Medical Science
急性心膜炎の原因は,感染性ではウイルス性が最も多いが,ウイルス性心膜炎で心タンポナーデを呈することは稀である.症例は生後11カ月時に心室中隔欠損症に対して心内修復術歴のある12歳男子.5日前に胃腸炎症状での受診歴があり,その後けいれんのため救急搬送された.低血圧性ショック状態で,心エコーで多量の心嚢液貯留と右室圧排像を認め,中心静脈圧は24 mmHgに上昇していた.心タンポナーデに伴う低心拍出症候群と診断し,心嚢ドレナージを行ったところ,血圧は上昇し,中心静脈圧は13 mmHgへ改善した.ロキソプロフェンと利尿薬の投与を開始し,心嚢液の再貯留を認めなかったため,入院14日目に退院した.入院時の血清コクサッキーウイルスA2 (CoxA2)抗体(NT法)が32倍で,3週間後の血清では128倍と4倍の上昇を認めたため,CoxA2性急性心膜炎と診断した.CoxA2性急性心膜炎の症例報告は前例がないため提示する.
Acute pericarditis is commonly caused by viral infections. However, cardiac tamponade associated with viral pericarditis is a rare condition. This paper reports the case of a 12-year-old boy with a history of intracardiac repair for a ventricular septal defect at 11 months of age. Five days prior to admission, he presented with symptoms of gastroenteritis followed by seizures, which necessitated emergency transport to the hospital. He was in hypotensive shock, and echocardiography revealed significant pericardial effusion with right ventricular collapse. The central venous pressure (CVP) was elevated to 24 mmHg. The patient was diagnosed with low cardiac output syndrome due to cardiac tamponade, and pericardial drainage was performed. The blood pressure recovered promptly, and the CVP decreased to 13 mmHg. Loxoprofen and diuretics were initiated, and no reaccumulation of pericardial effusion was observed. The patient was discharged on the 14th day of hospitalization. Serological tests revealed that the Coxsackievirus A2 (CoxA2) antibody titer was 1:32 at admission, and increased to 1:128 three weeks later (a fourfold increase), confirming the diagnosis of acute CoxA2 pericarditis. To our knowledge, this is the first case report of acute CoxA2 pericarditis.
Key words: pericarditis; Coxsackievirus A2
© 2025 特定非営利活動法人日本小児循環器学会© 2025 Japanese Society of Pediatric Cardiology and Cardiac Surgery
急性心膜炎の原因には感染性,自己免疫性,腫瘍性,外傷性などがあるが,小児では原因が同定できず診断に至らないことが多い1).成人も含め,過去にコクサッキーウイルスA2(coxsackievirus A2: CoxA2)性急性心膜炎と診断された症例の報告はない.この度,心タンポナーデのため心嚢ドレナージを要し,入院時と退院後のペア血清抗体価によりCoxA2と原因を特定できたウイルス性急性心膜炎の1例を経験したため報告する.
症例は12歳男児.心室中隔欠損症(ventricular septum defect: VSD)に対し生後11カ月で心内修復術を行われた.受診時定期内服薬はなく,直近1カ月以内のワクチン接種歴もなかった.
受診の21日前から全身倦怠感を認めていた.5日前に腹痛があり,4日前に嘔気を認め受診し,胃腸炎の診断で経過観察された.入院日,1分以内の全身性強直発作を認めたため前医へ救急搬送された際に,持続性の胃腸炎症状の鑑別を行う目的で心臓超音波検査を行われたところ,多量の心嚢液貯留を認めたため当院へ搬送となり,集中治療室へ入院した.
身長164.9 cm,体重47.5 kg,体温37.0度,脈拍数120回/分,血圧100/66 mmHg,呼吸数16回/分,SpO2 97–98%(経鼻酸素2 L/分),Glasgow Coma Scale E4V5M6,腹痛により苦悶様の表情を認めた.顔色不良で外頸静脈は怒張していた.心音は整で心雑音は認めず,心膜摩擦音を聴取しなかったが,胸部圧痛を認めた.肝臓は季肋下に4 cm触知し,末梢冷感を認めた.
入院時の血液検査で代謝性アシドーシスを認めた.D-dimerは10.2 µg/mLと高値,CK-MBは3.0 ng/dLと軽度高値,トロポニンIは299 pg/mLで高値,BNPは374 pg/mLに上昇していた.ASO,リウマチ因子,甲状腺刺激ホルモンに異常を認めなかった.感染症検査として,多項目ポリメラーゼ連鎖反応(polymerase chain reaction: PCR)パネル検査を行ったがいずれも陰性だった.βDグルカンや結核菌特異的インターフェロンγ検査は陰性,その他提出していた血液学的検査で,CoxA2-IgG抗体と,CoxA9-IgG抗体が32倍(NT法)と後日判明した.胸部X線写真では心胸郭比(cardiothoracic ratio: CTR)59%と心拡大および肺うっ血像を認めた(Fig. 1A).心電図検査では,VSD術後から認めていた完全右脚ブロック波形を認め,全体的にやや低電位だったが,過去の心電図と比較してST部分の変化は認めなかった(Fig. 1B).心臓超音波検査では心臓前面に4 cm程度の心嚢水貯留を認め,右室は圧排されていた(Fig. 1C, D).
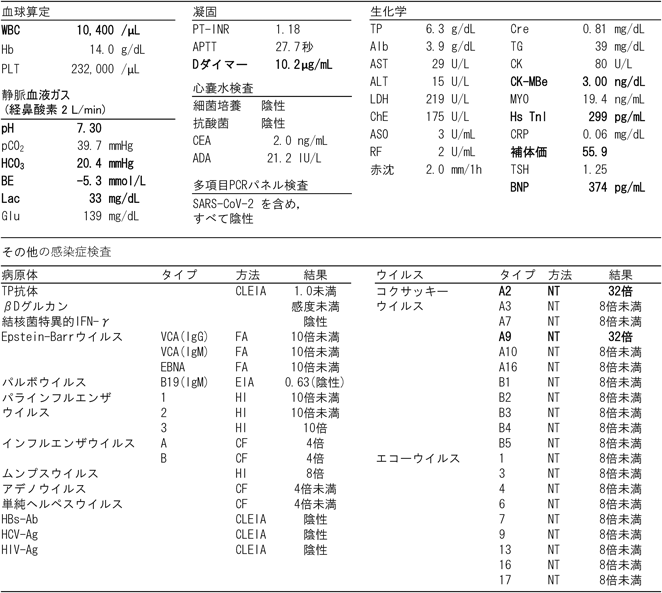 |
| 夜間の入院であり,各種抗体価は入院翌日の血清で検査.ADA:アデノシンデアミナーゼ,CF:補体結合反応,CLEIA:化学発光酵素免疫測定法,EIA:酵素抗体法,FA:蛍光抗体法,HI:赤血球凝集抑制法,HsTnI:高感度トロポニンI,MYO:ミオグロビン,NT:中和反応. |
A:胸部X線写真半坐位撮像.59%と心拡大を認め,肺うっ血像を認めた.B:心電図.術後より完全右脚ブロックを認めていた.過去と比較して明らかなST変化を認めなかった.C:心臓超音波検査左室短軸像.右室の前面に3 cm程度の心嚢水貯留を認めた.D:心臓超音波検査四腔断面像.心尖部に3 cm程度の心嚢水貯留を認めた.LA:左心房,LV:左心室,PE:心嚢水,RV:右心室.
当院集中治療室に入院し,心エコーで上記所見を得たため急性心膜炎により心タンポナーデを呈していると診断し,動脈ライン,中心静脈ラインを確保したうえで,静脈麻酔,局所麻酔下にエコーガイド下心嚢ドレナージを行った.心嚢液は無色透明で,細菌培養,抗酸菌培養は陰性,CEA 2.0 ng/mL,ADA 21.2 IU/Lだった.また,得られた心嚢液検体は,地域の衛生研究所へウイルス分離依頼を行ったが,エンテロウイルス,ライノウイルス,アデノウイルス,パレコウイルス,RSウイルス,ヒトメタニューモウイルス,ボカウイルス,パラインフルエンザウイルス,ヒトコロナウイルス,インフルエンザウイルスを検出しなかった.心嚢液180 mLを除水した時点で収縮期血圧は120 mmHg台へ上昇し,中心静脈圧は24 mmHgから13 mmHgへ改善した.非ステロイド性抗炎症薬としてロキソプロフェン180 mg/日を,利尿薬としてフロセミド80 mg/日およびスピロノラクトン50 mg/日を開始し,入院2日目には集中治療室を退室した.入院7日目には胸部X線写真のCTRが42%まで改善し,以後心嚢液の再貯留を認めなかった(Fig. 3).入院11日目の心臓造影MRI検査では心筋内に遅延造影所見を認めなかった.ロキソプロフェンは合計5日間で終了し,利尿薬を漸減した状態で入院14日目に退院した.入院時から21日後に採取した血清でCoxA2抗体(NT法)が128倍と4倍の上昇を認めたため,CoxA2性急性心膜炎と診断した.1年間のフォローアップで心嚢液の再貯留や収縮性心膜炎を認めなかった.
小児の急性心膜炎の多くで病因を特定できず,報告される施設によっても異なるが,特発性と診断されることが最多で37~68%に及ぶ1, 2).現在この特発性とされている症例の多くはウイルス性,またはウイルス感染後と推定される1).また,小児の急性心膜炎で,ウイルス性または特発性と診断された症例の17.7%で心嚢穿刺または心膜切開術が施行されたが,心タンポナーデをきたした症例は2.0%と少なかった2).
本症例の初期症状は胃腸炎症状と胸部圧痛であり,心電図上の変化は過去のものと比較して認めず,心膜摩擦音も聴取しなかった.心膜炎は臨床診断であり,胸痛,心膜摩擦音,心電図異常,心嚢水貯留の4項目のうち2項目を満たした際に診断するが,2023年の心膜炎のレビューにおいて心電図異常は60%とされている1).また,Abdel-Haqらの心膜炎患者32例の報告では,心膜摩擦音は19%で聴取した3).本症例のように心膜摩擦音や,心電図上の平常時と比較した変化がなくても心膜炎の可能性はある1).
コクサッキーウイルスはピコルナウイルス科エンテロウイルス属に分類される一本鎖(+)RNAウイルスである.ヒトに感染性のあるエンテロウイルス属は遺伝子型による分類では,ヒトエンテロウイルスA種,B種,C種,D種に分類され,110以上のエンテロウイルスが同定されている4).抗原性の違いによって血清型の分類をすると,エンテロウイルスはポリオウイルス群,コクサッキーウイルスA群,B群,エコーウイルス群,エンテロウイルス群に分類されるが,コクサッキーウイルスA群とB群に関しては生後すぐのマウスに投与した際の病原性で命名されたものであり,AあるいはBが種を意味しているわけではない.心筋炎や心膜炎を発症することが特徴的なコクサッキーウイルスはヒトエンテロウイルスB種のうちコクサッキーウイルスB1~6,およびA9に多い5, 6).CoxA2はヒトエンテロウイルスA種に分類され,通常はヘルパンギーナなどの上気道炎を起こすウイルスである5).既報として,同じヒトエンテロウイルスA種に属するCoxA4で心筋炎を来した成人例が1例報告されており7),CoxA2に似たエンテロウイルスが便から検出された致死性心筋炎の10歳女児例が報告されている8).また,新生児マウスモデルにおいてCoxA2が心臓障害を引き起こすことが示唆された報告がある9).しかし,ヒトにおいては,CoxA2によって心膜炎,心タンポナーデを来した症例の報告は我々の検索した範囲では前例がなかった.本症例の心嚢液からウイルスが分離されなかった点に関しては,保健所等でのウイルス分離培養検査ではコクサッキーウイルスA群の分離は困難であることが知られており,急性期と回復期の血清で中和抗体が4倍以上に上昇していれば間接的に証明できるとされるため,本症例はCoxA2性急性心膜炎と診断した5, 6).
本症例では,VSDの術後であることが影響している可能性は否定できない.心筋梗塞,外傷,心膜切開術の数日から数カ月後に心膜炎を起こすことがあり,心膜切開後症候群と呼ばれる10).心膜切開後症候群患者の血中にはアクチンとミオシンに対する抗体が存在することから,心臓由来の抗原が循環中に放出され,心臓組織に対する抗体が産生されることで炎症が誘発される自己免疫学的なメカニズムが提唱されている11).我々の検索した範囲内ではいずれも1年以内に起こっており,術後10年以上経過して発症した報告はなかった.前述のとおりCoxA2でも心膜炎を起こす可能性は示唆されており,手術歴が本症例に影響を及ぼした可能性は低いと考える.
本症例は,CoxA2による小児急性心膜炎の初報告例であり,心タンポナーデにより緊急心嚢ドレナージを要した.過去に報告のないウイルスにおいても心膜炎を引き起こすことはあり,十分な血清学的なウイルス検査を行うことで適切な診断が可能となりうる.
緊急ドレナージを要したCoxA2による急性心膜炎の1例を経験した.CoxA2による急性心膜炎の報告は過去にないが,稀と言われているコクサッキーウイルスA群でも心膜炎を起こしうるため,心膜炎と診断した場合には,血清学的なウイルス感染の検索を積極的に行うべきである.
発表に際し,保護者から論文掲載についての承諾を書面で得ています.
日本小児循環器学会の定める利益相反に関する開示事項はありません.
井口貴文は本症例の診療,論文作成に携わった.星野真介,沢田有里,高島光平,藤田聖実,古川央樹は,本症例の診療,論文の監査に携わった.
本報告は,第127回日本小児科学会 総会・学術集会で「緊急心嚢ドレナージを要したコクサッキーウイルスA2性急性心膜炎の小児例」として発表した.
1) Shahid R, Jin J, Hope K, et al: Pediatric pericarditis: Update. Curr Cardiol Rep 2023; 25: 157–170
2) Shakti D, Hehn R, Gauvreau K, et al: Idiopathic pericarditis and pericardial effusion in children: Contemporary epidemiology and management. J Am Heart Assoc 2014; 3: e001483
3) Abdel-Haq N, Moussa Z, Farhat MH, et al: Infectious and noninfectious acute pericarditis in children: An 11-year experience. Int J Pediatr 2018; 2018: 5450697
4) Xie Z, Khamrin P, Maneekarn N, et al: Epidemiology of enterovirus genotypes in association with human diseases. Viruses 2024; 16: 1165
5) 藤本嗣人:【コロナ禍去って今こそ必要なエンテロウイルスの知識】エンテロウイルスとは(総論).小児科2024; 65: 5–10
6) 幾瀬 樹,大宜見力:臨床医のための微生物学講座 エンテロウイルス(コクサッキーウイルス,エコーウイルス,エンテロウイルス),コロナウイルス.医のあゆみ2024; 289: 591–596
7) Yamamoto H, Isogai J: Transient constrictive pericarditis following coxsackievirus A4 infection as a rare cause of acute mediastinitis: A case report. Heliyon 2023; 30: e19555
8) Bending JW, O’Brien PS, Muir P, et al: Enterovirus sequences resembling coxsackievirus A2 detected in stool and spleen from a girl with fatal mayocarditis. J Med Virol 2001; 64: 482–486
9) Wu Z, Zhu S, Qian J, et al: Analysis of miRNAs involved in mouse heart injury upon Coxsackievirus A2 infection. Front Cell Infect Microbiol 2022; 12: 765445
10) 奥田奈緒,今中秀光,網野祐美子,ほか:心膜切開後症候群に対してアスピリンが有用であった小児症例.日集中医誌2012; 19: 433–434
11) Malik J, Zaidi SMJ, Rana AS, et al: Post-cardiac injury syndrome: An evidence-based approach to diagnosis and treatment. Am Heart J Plus 2021; 12: 100068
This page was created on 2025-04-25T10:19:07.004+09:00
This page was last modified on 2025-07-01T15:09:00.000+09:00
このサイトは(株)国際文献社によって運用されています。