動脈管動脈瘤(ductus arteriosus aneurysm: DAA)は動脈管が嚢状または管状に拡張を来す疾患である.動脈管の大動脈側が開存している動脈管憩室が進行性に拡大して瘤化すると考えられている1, 2).成人例は稀であるが,周囲構造への圧迫だけでなく,瘤破裂,血栓塞栓症,感染などの致死的合併症があるため早期の治療介入が必要である1, 2).治療法としては外科治療が施行されてきたが1, 3),近年ステントグラフトの報告もある4, 5).閉鎖栓を用いた経皮的閉鎖術の報告はほとんどなく,Amplatzer™ Duct Occluder(ADO)を用いた閉鎖報告はない.
56歳のDAA症例に対してADOを用いて経皮的閉鎖術を施行した.低侵襲かつ有用な治療オプションと思われるので報告する.
症例
56歳,男性
現病歴
20歳頃に近院で動脈管開存と診断されたが,短絡量が少ないため治療適応にならなかった.その後通院を自己中断していた.54歳からII度高血圧の診断で降圧薬の内服を開始した.55歳時の健康診断で弓部大動脈瘤が疑われ,同院を受診した.造影CT像でDAA(瘤最大径39 mm,大動脈側入口部径5.6 mm,肺動脈側流出部径2.2 mm)と診断され,治療目的に当科に紹介された.瘤破裂の危険があるため,早期の介入治療を計画し,経皮的動脈管閉鎖術目的に入院した.
既往歴
緑内障,II度高血圧,高脂血症
家族歴
特記なし
生活歴
機会飲酒,喫煙なし
内服薬
アムロジピン10 mg/日,アテノロール25 mg/日,アトルバスタチン10 mg/日
来院時現症
身長160 cm,体重69.3 kg,体表面積1.73 m2,心拍数66/分,血圧127/80 mmHg,SpO2 97%(室内気),心音は整で心雑音は聴取せず,嗄声や嚥下障害は認められなかった.
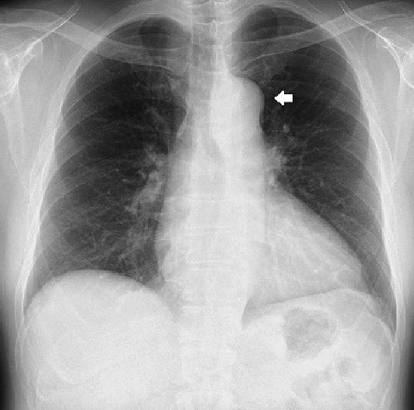
胸部X線
心胸郭比53%,左側大動脈弓陰影の突出を認めた(Fig. 1).
12誘導心電図
心拍数79/分,正常洞調律,QRS電気軸正常
心臓超音波検査
左室拡張末期径47 mm,左室駆出率70%,有意な弁逆流なし,腹大動脈パルスドプラ脈波 正常波形
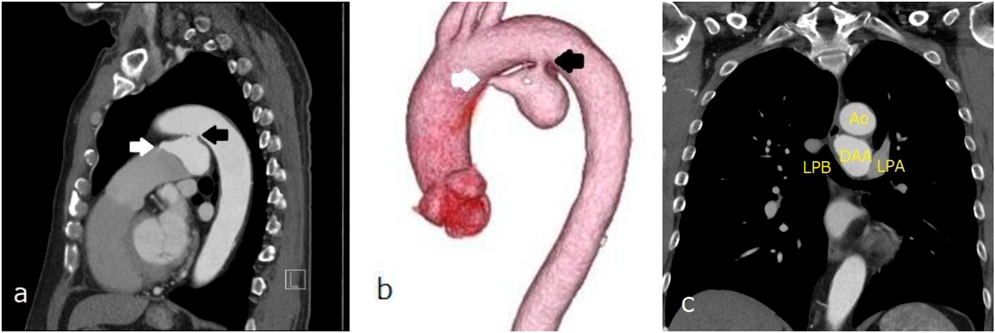
胸部造影CT
大動脈弓小彎側に入口部(径5.6 mm)をもつ最大径39 mの嚢状に拡大したDAAを認め,肺動脈側に出口部(2.2 mm)をもつ.大動脈解離なし.DAAは左主気管支と接触しているが圧排なし(Fig. 2).
入院後経過
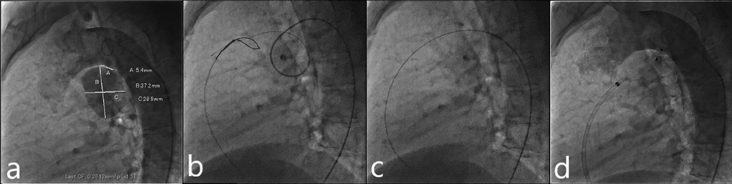
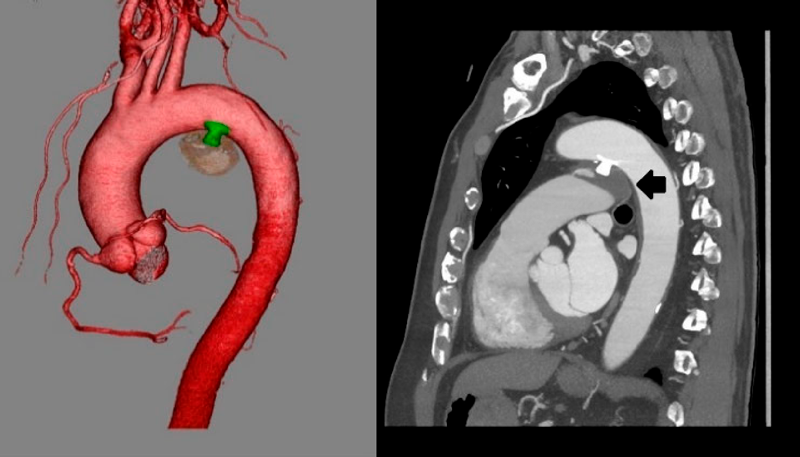
入院翌日に経皮的動脈管閉鎖術を施行した.局所麻酔後,右大腿静脈に6 Fr 11 cm sheath(Medikit Inc., Tokyo),右大腿動脈に5 Fr 11 cm sheath(Medikit Inc., Tokyo)を留置した.カテーテル検査の結果Qp/Qsは1.05,肺血管抵抗係数は0.57 Wood unit·m2.大動脈造影でDAAが造影され,瘤入口部径は5.4 mm,瘤最大径は28.9×37.2 mm,瘤流出部径は2.2 mmであった(Fig. 3a).5 Frジャドキンス型右冠動脈用(JR)カテーテル(Hanaco Medical, Saitama, Japan)を逆行性に進めて瘤入口部にかけて,そこから0.035̋Radifocus guidewire 260 cm(Terumo Inc., Tokyo)を瘤内へ進めて,1ループさせて主肺動脈まで進めた.続いて,順行性に進めて主肺動脈に留置した6 Fr wedge pressure catheter(Gadelius Medical, Kanagawa, Japan)から15 mm径の6 Fr Amplatz goose neck snare (Medtronic plc., Ireland)を進めて,Radifocus guidewire先端を把持して(Fig. 3b)右大腿静脈のsheath外まで引き出した.瘤内のループを伸ばして,大腿静脈–DAA–大腿動脈のwire loopを作成した(Fig. 3c).DAAの大動脈側入口部径が5.4 mmであったため,ADO 12 mm/10 mm(Abbott Structural Heart, Plymouth, MN, USA)を同部に留置した:右大腿静脈のsheathを抜去し,7 Fr Amplatzer™ TorqVue 180 (Abott, Pylmouth, MN, USA)を下行大動脈まで進めた.ADOのRetention skirtを展開して瘤入口部にかけて,デバイスボディを瘤内に展開した.留置後の大動脈造影では閉鎖栓突出による大動脈の狭窄はなく,遺残短絡はごく少量であった(Fig. 3d).特に合併症は認めず,治療翌日からアスピリン100 mgの内服を開始し,退院した.治療後の経過は良好で,術後1カ月の心臓超音波検査で遺残短絡は消失し,術後3カ月の胸部造影CT像で瘤内はほぼ血栓化していた(Fig. 4).
DAAは正期産児の8.8%に認められ,ほとんどが無治療で消退し,予後は良好である6).一方,成人期DAAは稀な疾患であり,動脈管の閉鎖過程において,肺動脈側の閉鎖に続く大動脈側の閉鎖遅延のため,動脈管が憩室として遺残し,これが次第に拡張して囊状動脈瘤を形成する疾患である3).本症例は肺動脈への交通が残存していたが,多くは肺動脈端が閉鎖している4).瘤化の原因としては,動脈管は大動脈や肺動脈よりも弾性線維に乏しく,中膜の粘液性変化もあるので7),体血圧を受けて徐々に拡大していくと考えられている2, 8).高齢,喫煙,男性,高血圧が動脈硬化性病変として影響している可能性もある1, 5).
成人期DAAは初めは無症状であるが,周囲構造を圧迫すると嗄声,咳嗽,呼吸苦,胸部痛,嚥下障害などが生じる.血痰,喀血は気管や食道への瘤穿破のサインである.合併症には破裂,解離,感染,塞栓症がある1–3, 5, 9).DAAの48%が瘤の合併症により死亡したという報告もあり1),DAAは放置すると致死率が高い疾患である.死亡例の瘤の最小サイズは4×3 cmと報告されている1).本症例は無症状であったが,破裂や塞栓症などの合併症のリスクを考慮して早期に治療介入した.
成人期DAAの治療に関しては,胸骨正中切開または左側開胸による開胸手術が一般的であり,閉鎖栓を用いた経皮的閉鎖術の報告はほとんどない.開胸手術では人工心肺を用いた瘤切除,交通孔の直接閉鎖もしくはパッチ閉鎖,人工血管置換が施行されるているが1, 3, 5),皮膚切開の範囲が大きく,血胸,乳び胸や反回神経損傷などのリスクがある.また,動脈硬化による石灰化を伴っている場合は血管壁の脆弱性から直接閉鎖は難易度が高くなる.近年,大動脈ステントグラフト内挿術(Thoracic endovascular aneurysm repair: TEVAR)も施行されているが4, 5),22 Fr程度の大口径sheathを用いるため通常カットダウン法によるアプローチが必要となる.また,重大な合併症に脳梗塞や脊髄虚血による対麻痺が挙げられる.
一方,閉鎖栓を用いた閉鎖術は大腿動脈または大腿静脈から6~7 Fr sheathを用いて施行可能であり,出血量は少なく,入院期間も短い低侵襲な治療法である.18×14 mmとそれほど大きくはないDAAの中にAmplatzer™ vascular plug II (AVPII)を留置した報告はあるが10),ADOを用いた閉鎖報告は本報告が初と思われる.本症例のDAAは最大径28.9×37.2 mmと大きいが,大動脈からの流入部径は5.4 mmとそれほど太くはなく,また肺動脈への流出部が残存していたので,大腿動脈–DAA–大腿静脈ワイヤーループが作成可能であり,順行性に瘤入口部をADOを用いて閉鎖できた.肺動脈への流出部を閉鎖した場合は,動脈瘤内に血液が流入する圧負荷が持続して瘤がさらに拡大する危険があるので,大動脈側を閉鎖する必要がある.また,瘤流出部が閉塞している場合はADOを留置できないので,AVPIIや,径が大きい場合は心房中隔欠損閉鎖用の閉鎖栓を逆行性に瘤流入部に留置する手段が考えられる.また,瘤内をコイルで閉鎖する方法もありうるが,大きな瘤を閉鎖する場合は多くのコイルが必要になり,また手技時間も長くなると予想されるので,閉鎖栓を用いた閉鎖が望ましい.
閉鎖栓留置後の抗凝固・抗血小板療法に関するガイドラインはないが,瘤入口部をADOなどの閉鎖栓で閉鎖した場合,大動脈側は通常の動脈管を閉鎖した場合と同様なので薬剤は不要と思われる.しかし,瘤内で生じた血栓が肺動脈へ流れて肺塞栓を来す可能性があるので,血栓化・内膜化が進むまでの間は抗血小板薬の使用が望ましいと思われる.本症例では1年間アスピリンを使用した.