患者背景(Table 1)
HH合併の内臓錯位症候群・単心室患者は13例(12%)で,男児7例,女児6例であった.全例が生後早期の胸腹部CTにて胸腔内に胃泡突出を認めたことからHHと診断された.10例に静脈還流異常(total anomaly of pulmonary vein connection: TAPVC)を合併した(Ia 2例,Ib 2例,IIb 4例,III 1例,Ia+IIb 1例).なお右側相同の症例においては,共通肺静脈腔を形成し心房に接続する場合にTAPVC(IIb)と診断した.生下時にPVOを認めた2例を含む4例がTAPVC修復術を施行された.TAPVC修復術後3例が再狭窄を来し再手術を必要とした.7例が不整脈既往(上室性頻拍4例,心房頻拍1例)を有した.
Table 1 Patients with hiatal hernia| Case | Sex | Cardiac diagnosis | TAPVC | TAPVC repair | PVO | Cause of PVO | Operation for HH | Prognosis |
|---|
| 1 | F | SRV CAVV PS TAPVC(IIb) RAI | + | − | − | − | + | Achieved Fontan |
| 2 | M | SRV CAVV Pulmonary atresia
bil SVC TAPVC(Ib) SVT RAI | + | + | + | Post TAPVC repair
Compressed by HH | + | Waiting for BDG |
| 3 | F | SRV CAVV non confluent PA
TAPVC(IIb) AT RAI | + | − | + | Compressed by HH | + | Death
(Perioperative death) |
| 4 | M | SRV CAVV PS TAPVC(IIb) RAI | + | − | + | Compressed by HH | + | Achieved Fontan |
| 5 | M | SRV CAVV PS cAVB RAI | − | − | + | Compressed by HH | + | Achieved Fontan |
| 6 | F | SRV CAVV PS bil SVC TAPVC(Ia)
SVT RAI | + | + | + | Post TAPVC repair | + | Achieved Fontan |
| 7 | M | SV CAVV AS CoA bilSVC RAI | − | − | − | − | − | Death |
| 8 | F | SRV CAVV PS bil SVC
TAPVC(Ib) SVT RAI | + | + | + | PVO since birth | − | Achieved Fontan |
| 9 | F | SRV CAVV PA bilSVC
TAPVC(IIb) RAI | − | − | − | − | − | Achieved Fontan |
| 10 | M | SRV CAVV PS bil SVC TAPVC(Ia)
common PV atresia RAI | + | − | + | PVO since birth | − | Death |
| 11 | M | SV CAVV PA TAPVC(Ia+IIb)
SVT RAI | + | − | − | − | − | Achieved Fontan |
| 12 | M | SRV CAVV PA RAI | − | − | − | − | − | Achieved Fontan |
| 13 | F | SRV CAVV non confluent PA
bil SVC TAPVC(III) SVT RAI | + | + | + | Post TAPVC repair | − | Death |
| AS, aortic stenosis; AT, atrial tachycardia; BDG, bidirectional Glenn; bil SVC, bilateral superior vena cava; cAVB, complete atrioventricular block; CAVV, common atrioventricular valve; CoA, coarctation of the aorta; HH, hiatal hernia; PA, pulmonary artery; PAPVC, partial anomalous pulmonary venous connection; PS, pulmonary stenosis; PV, pulmonary vein; PVO, pulmonary vein obstruction; RAI, right atrial appendage isomerism; S(R)V, single (right) ventricle; SVT, supraventricular tachycardia; TAPVC, total anomalous pulmonary venous connection. |
HH修復術施行6例のHH手術周術期の経過(Table 2)
HH 13例中6例がHH修復術適応と判断され手術が施行された.HH修復術施行時,月齢は9.2±5.5ヵ月,体重は6.2±1.9 kgであった.HH修復術適応は,内科治療抵抗性胃食道逆流1例,HHによる肺静脈圧排を疑った4例,総肺静脈還流異常修復前の左房後方スペース確保目的1例であった.滑脱した胃による肺静脈圧排を疑った4例の詳細を示す.症例2はTAPVC術後に共通肺静脈腔-左房吻合部の血流加速を認め,共通肺静脈腔の後方から滑脱した胃の圧排が寄与している可能性が否定できなかったためHH修復術を行った.症例3・4は胸部CTで,滑脱した胃で圧排されている肺静脈径の狭小化を認めたため,HH修復術適応と判断した.症例5は心臓超音波検査で滑脱した胃の付近に位置する共通肺静脈腔から心房への流入血流が経時的に加速していることより,HH修復術の適応とした.HH手術時期は胃食道逆流を適応とした1例を除く5例で両方向性グレン手術(bidirectional Glenn: BDG)前であった.
Table 2 The data of patients receiving HH operation| Case | Age | Body weight (kg) | Circulation at HH operation | Operation indication | Approach | Operation | Reoperation | Prognosis |
|---|
| 1 | 1 y
5 m | 9.5 | BDG | To improve digestive symptoms | Unknown | ・HH operation | Duodenal stenosis
→Pyloroplasty | Alive
Improved digestive symptoms |
| 2 | 1 y
3 m | 7.5 | SPS
Post TAPVC repair | To release PV compression | Laparoscopy | ・Diaphragmatic plication
・Fundoplication
・Gastrostomy | — | Alive
Recurrent PVO |
| 3 | 7 m | 4.7 | SPS | To release PV compression | Laparoscopy | ・HH operation
・Gastrostomy | —
(Duodenal stenosis) | Death |
| 4 | 7 m | 5.5 | SPS+PAB | To release PV obstruction | Laparoscopy | ・HH operation
・Fundoplication | ・Drainage of intraabdominal abscess
・Gastrostomy | Alive
Improved PVO |
| 5 | 3 m | 5.0 | Pre BDG | To release PV compression | Laparoscopy | ・HH operation
・Repair of malrotation | Duodenal stenosis
→Gastroduodenal bypass | Alive
Improved PV compression |
| 6 | 6 m | 4.9 | SPS
Post TAPVC repair | To secure a space for TAPVC repair | Laparoscopy
→Laparotomy | ・HH operation
・Fundoplication
・Repair of malrotation
・Gastroduodenal bypass | — | Alive |
| BDG, bidirectional Glenn; HH, hiatal hernia; PAB, pulmonary artery banding; PV, pulmonary vein; SPS, systemic to pulmonary shunt; TAPVC, total anomalous of pulmonary vein connection. |
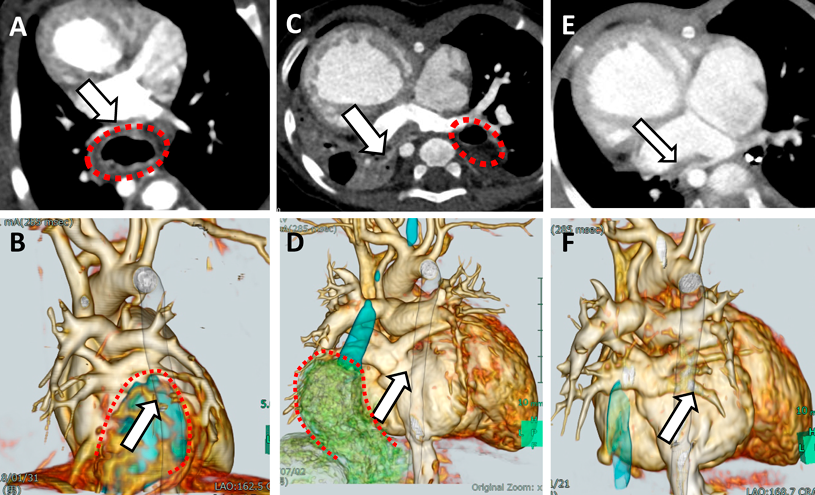
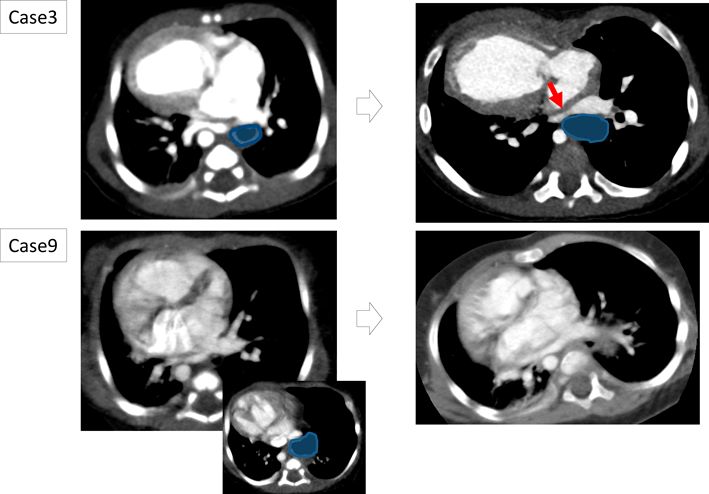
HH手術施行6例中肺静脈圧排が疑われHH手術を行った4例は,いずれも胸部CT検査で滑脱した胃による肺静脈圧排解除が確認された.そのうちの1例(症例4)の画像を提示する(Fig. 1).出生時の胸部CTで滑脱した胃が右下肺静脈を圧排しており(Fig. 1A, B),5ヵ月時の胸部CTで右下肺静脈閉塞を来していた(Fig. 1C, D).この段階での滑脱した胃による直接的な右下肺静脈圧排はないものの,以前認められた右下肺静脈圧排や,滑脱した胃による胸腔内容量の減少,心臓の位置変化が右下肺静脈閉塞の要因として否定できなかったことに加え,その時点で滑脱した胃が接していた左下肺静脈が圧排され閉塞することが危惧されたためHH修復術の適応とされた.HH修復術施行後の胸部CTでは左肺静脈圧排が解除されたのみならず,右肺静脈閉塞も改善していた(Fig. 1E, F).また,重度の胃食道逆流によりHH手術の適応となった1例は,術前から行っていたEDチューブによる経管栄養を術後に離脱することができ,左房後方スぺース確保目的にHH手術を行った1例ではTAPVC修復術を施行可能となった.
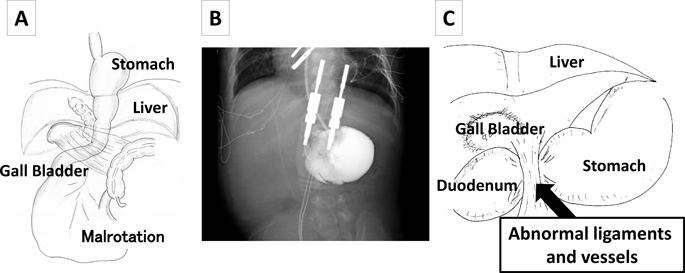
術後合併症として十二指腸狭窄合併が3例に認められた.症例5(Fig. 2)では,十二指腸狭窄解除術における術中所見で血管の走行異常があった.靭帯に覆われた肝動脈が十二指腸前面を走行しており(十二指腸前肝動脈),滑脱していた全胃を腹腔内に還納したことにより十二指腸が異常靭帯と十二指腸前肝動脈に圧排されて狭窄を来していた.また症例6では,滑脱した全胃を腹腔内に還納後,十二指腸前方に総胆管が走行することが判明した.開腹手術に移行し十二指腸バイパス術を追加することにより,総胆管による十二指腸狭窄を回避した.
HH手術施行6例中1例(症例3)が周術期に死亡した.この症例は右室性単心室,主肺動脈低形成を伴う肺動脈閉鎖に難治性心房頻拍を合併した重症例であった.HH修復術後に十二指腸狭窄を併発し麻痺性イレウスが遷延した.経静脈栄養のための中心静脈カテーテル挿入手技に伴う全身麻酔導入直後に徐脈となり,蘇生処置に反応せず死亡している.
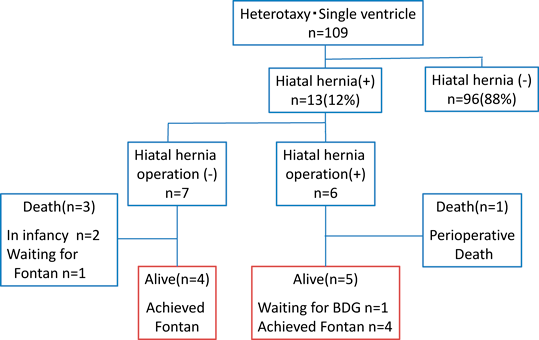
長期予後について(Fig. 3)
観察期間中,HH手術施行例のうち1例(症例3, HH手術周術期死亡),未施行例のうち3例(症例7, 10, 13)が死亡していた.症例7は腸回転異常を合併し,1歳7ヵ月Fontan手術待機中に死亡,剖検で回盲部から右側結腸の壊死性腸炎と確定診断され,HHとの関連は否定的であると判断された.症例10は1a型の総肺静脈還流異常合併例であり,HHとは無関係の肺静脈狭窄のため出生直後より高度のチアノーゼが持続し日齢2に死亡した.また症例13は単心室に肺動脈低形成を伴い日齢5に総肺静脈還流異常修復,肺動脈形成,シャント手術を行ったが,胸水や上室性不整脈の制御に難渋し,術後2ヵ月で啼泣を契機とする循環不全により死亡した.剖検では肺静脈閉塞やシャント閉塞は認めず循環不全の原因は不明であった.HH手術未施行の死亡例3例の死因はいずれもHHとの明らかな関連はなかった.
HH手術施行例のうち4例,未施行例のうち4例がFontan手術に到達していた.HH手術施行例と未施行例のFontan手術到達年齢(35(28–53)か月vs 43(33–72)か月p=0.49),Fontan手術後約6か月での心臓カテーテル検査時のSaO2(94.7(93.4–95.5)vs 95.2(89.9–95.6)% p=0.69),心係数(2.78(1.98–2.84)vs 3.68(2.57–4.09)L/min/m2 p=0.2)肺血管抵抗(1.56(1.28–2.53)vs 1.39(0.95–2.39)woods/unit/m2 p=0.69),PA Index(261.2(200.7–335.3)vs 217.5(202.7–279.9)mm2/m2 p=0.49)に有意差はなかったが,同カテーテル検査での中心静脈圧はHH手術施行例で有意に低かった(8 vs 12 mmHg p=0.03)(Table 3).
Table 3 The data of patients after Fontan procedure | Hiatal hernia operation (+)
n=4 | Hiatal hernia operation (−)
n=4 | p value |
|---|
| Age at Fontan operation (months) | 35 (28–53) | 43 (33–72) | 0.49 |
| Cardiac catheterization | | | |
| SaO2 (%) | 94.7 (93.4–95.5) | 95.2 (89.9–95.6) | 0.69 |
| CVP (mmHg) | 8 (6–9) | 12 (11–14) | 0.03 |
| C.I (L/min/m2) | 2.78 (1.98–2.84) | 3.68 (2.57–4.09) | 0.2 |
| RpI (wood/unit/m2) | 1.56 (1.28–2.53) | 1.39 (0.95–2.39) | 0.69 |
| PA index (mm2/m2) | 261.2 (200.7–335.3) | 217.5 (202.7–279.9) | 0.49 |
| C.I, cardiac index; CVP, central venous pressure; PA index, pulmonary artery index; RpI, pulmonary vascular resistance index; SaO2, arterial oxygen saturation. |
HH手術未施行例で,生後早期に死亡した症例10, 13以外の長期に経過を追えた症例においては,観察期間中にHHと関連するPVOは認めなかった.HH手術施行例のうち症例2がHH手術施行後にPVOを繰り返した.この症例はTAPVC術後であり,HH術後に滑脱した胃からの圧排がなくなった状態でもPVOが出現した.このことからPVOの原因はHHのみならずTAPVC術後の吻合部狭窄が関与していた可能性も示唆された.
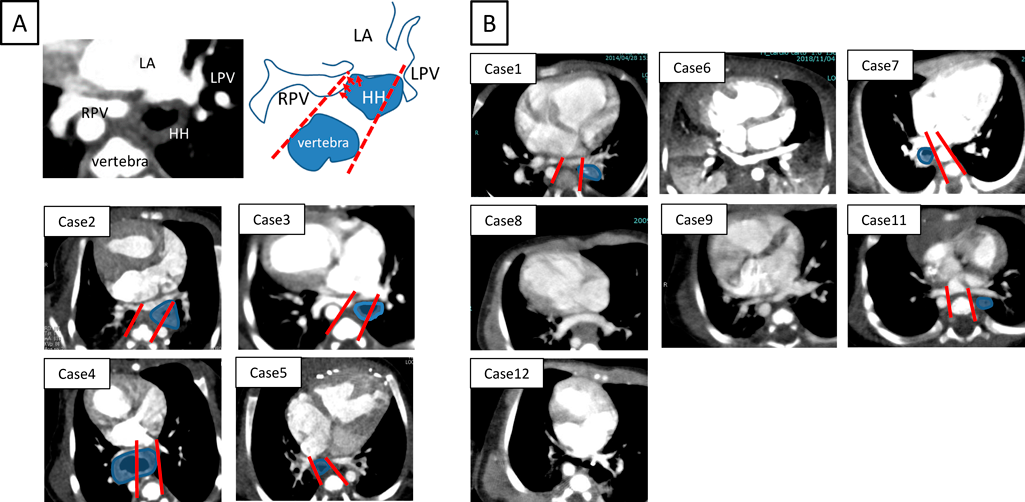
滑脱した胃と肺静脈との位置関係(Figs. 4, 5)
胸部CT画像における滑脱した胃と肺静脈との位置関係の相違を,肺静脈圧排例と非圧排例で観察し比較した.13例全例において肺静脈は共通肺静脈腔を形成し心房に接続していた.肺静脈圧排群(症例2, 3, 4, 5)では,①滑脱した胃の先進部が共通肺静脈腔と同じ高さに達している,②滑脱した胃は必ず心房椎体間に位置し,肺静脈を後方から圧排している,といった特徴を有していた.なお,下行大動脈は肺静脈圧排に関与していなかった.一方で肺静脈非圧排群では,①滑脱した胃の先進部が共通肺静脈腔の高さに達していない例(症例6, 8, 9, 12)と,②滑脱した胃の先進部が共通肺静脈腔の高さに達していても,共通肺静脈腔よりも末梢に位置している例(症例1, 7, 11)があった.肺静脈圧排群と非圧排群の特徴は,椎体の両縁から左右の肺静脈開口部へそれぞれ線を引き,その線の間に滑脱した胃が含まれるかどうかでより明確に判断できた(Fig. 4A).肺静脈圧排群では滑脱した胃は同線の間に位置した(Fig. 4A).一方で非圧排群では,滑脱した胃は同線外側に位置するか,肺静脈心房開口部とは同じCT断面で観察されず肺静脈開口部よりも腹側に位置していた(Fig. 4B).
また,肺静脈圧排群のうち症例3, 4, 非圧排群のうち症例8, 9, 12では経時的な漏斗胸の増悪を認めた.肺静脈圧迫群である症例3, 4は漏斗胸の進行に伴い肺静脈圧排が持続していたが,非圧排群である症例8, 9, 12は漏斗胸の増悪にもかかわらず肺静脈圧排の出現はなかった.Fig. 5に肺静脈圧排群である症例3,非圧排群である症例9の経時的変化を示す.漏斗胸は滑脱した胃による肺静脈圧排の増幅要因として影響していた.
内臓錯位症候群におけるHHの合併率は不明だが,無脾症候群では14.3%に合併するとされ5),本研究でも内臓錯位症候群・単心室患者の12%と極めて近い合併率を示した.
当院でのHH修復術施行6例中5例(83%)が,滑脱した胃と肺静脈の空間的関与を適応とした.肺静脈関連の適応でHH手術を施行した5例のうち周術期死亡が1例あり,HH手術後もPVOを繰り返した例が1例あったが,3例は肺静脈の状況が改善しFontan手術まで到達している.一方で,滑脱した胃による肺静脈の圧排なく,HH修復術適応外と判断されたのは7例であった.うち3例はHHとは関連のない死因で死亡しているが,生存4例は全例Fontan手術に到達している.HH手術施行,未施行にかかわらず,Fontan手術に到達した例は良好なFontan循環を維持しており,肺静脈関連合併症も認めなかった.以上より当院におけるHH外科治療戦略は妥当であると考えられた.また,胸部CTにおける滑脱した胃と肺静脈の位置関係の観察から,左右肺静脈心房開口部と椎体の両縁を結ぶ直線の間に滑脱した胃が存在する場合は肺静脈圧排リスクがより高い可能性が示唆された.これは椎体と心臓との間の狭い空間に肺静脈開口部と滑脱した胃が一直線に並ぶことを意味しており,漏斗胸の進行などで胸郭前後径が小さくなった場合に,より肺静脈圧排群と非圧排群の差が明確になることと矛盾しないと考える.内臓錯位症候群では生後早期の胸骨正中切開を要する手術に伴う漏斗胸の進行や房室弁逆流による心拡大の進行がしばしば認められるため,滑脱した胃と肺静脈との位置関係を観察することは,経時的な変化の予測にも有用である.
HHによる肺静脈圧排は,成人で少数の報告がある.Naoumらは,成人正常心の巨大HH30例のうち滑脱した胃による肺静脈圧排を左右それぞれ37/40%に認めたと報告した2).Saorayaらは滑脱した胃による肺静脈圧排が血栓形成から,腎動脈塞栓を引き起こした1例を報告した3).一方,小児および内臓錯位症候群における肺静脈圧排については現在(2023年12月)までに報告がない.本報告は内臓錯位症候群小児例におけるHHの肺静脈圧排について,介入適否から予後まで詳細に検討した初めての報告である.右心バイパス手術適応例では肺静脈狭窄は重大な予後規定因子であり6, 7),その機序のひとつに,周辺臓器からの圧排が挙げられている8).本研究によってHHの肺静脈圧排が小児患者においても認められ,特に単心室患者においては重要視するべき有害事象であることが示唆された.そのため,当院では,HH合併例で滑脱した胃が肺静脈を圧排している所見が得られた場合,肺循環における懸念事項を排除するという目的で,BDG施行前にHH修復術を積極的に行う方針をとっている.
一方で未修復のHHの存在が長期的な肺静脈圧排リスクであるか否かには議論の余地がある.当院でHH修復術適応外と判断された症例のうち,生存例は観察期間中にHH関連の合併症なく良好なFontan循環を維持している.よって本研究では,このコホートにおけるHHに対しての全例的な介入は妥当ではなく,画像所見を参考とし症例ごとにHH修復術適応を検討すべきであることも示唆された.
本研究ではこのコホートにおけるHH修復術後合併症にしばしば十二指腸狭窄を認めることが示された.HH修復術施行例6例中3例(症例1, 3, 5)で術後十二指腸狭窄を合併し,うち2例(症例1, 5)で十二指腸狭窄に対する再手術を要した.いずれも術前検査では十二指腸狭窄を指摘されておらず,滑脱した胃を腹腔内に還納したことにより術後顕在化した.症例1の狭窄機転の詳細は不明であるが,症例5では異常靭帯・血管(前十二指腸肝動脈)の存在が十二指腸狭窄の原因であり,腹腔内臓器の異常を合併しやすい内臓錯位症候群に9, 10)特徴的な合併症と考えられる.Miyakeらは,右側相同・単心室患者でHH根治手術を施行した6例中4例で再手術を要し,うち2例が術後十二指腸狭窄によるものであったと報告した4).この術後十二指腸狭窄は術前検査では予想が困難であるが,術中滑脱した胃を腹腔内に還納した後に腹腔内をよく観察することに加え,術後通過障害を疑う所見があった場合には十二指腸狭窄の可能性を念頭において対応することが重要であると考えられる.また,内臓錯位症候群は対称肝合併率が高く,心不全による肝腫大を来しやすいため,腹腔内の手術操作の難易度が高い11).そのため腹腔鏡手術よりも開腹手術が適している症例もあり,より安全で確実な術野確保が必要となる.術後管理として,単心室循環においては水分管理に特に配慮する必要があり,チアノーゼや心不全の強い症例では,創治癒遅延も念頭に置かなければならない.また,内臓錯位症候群の中で,いわゆる「無脾症」と呼ばれる症例は易感染性がある12)ことから術後感染症にも十分注意が必要である.以上のように内臓錯位症候群におけるHH修復術は,手術時に特別な配慮が必要であることに留意しなければならない.また,このコホートにおける手術適応は必ずしも胃食道逆流ではないことより,噴門形成術を同時に行った症例は限られていた.噴門形成術の適応は術前に胃食道逆流がある場合に加え,術後胃食道逆流が出現した際に再手術を行うことが血行動態的に高リスクであると考えられる場合に検討している.
本研究の限界として,内臓錯位症候群におけるHHの有病率が低く症例数が少ないこと,後方視的な検討であることがあげられる.また,滑脱した胃の心血管圧排評価を空腹時にしか行っていない.HHでは食事摂取により胃が拡張し,空腹時には認められなかった心血管圧排が顕在化することが知られており,GnanenthiranらはHHを有する成人32例で300 gの米摂取により滑脱した胃の左房圧排が顕在化することを報告した13).空腹時の評価のみでも画像上有用な所見は得られたが,食事摂取時画像の評価を行うことが,手術適応決定の一助になる可能性がある.