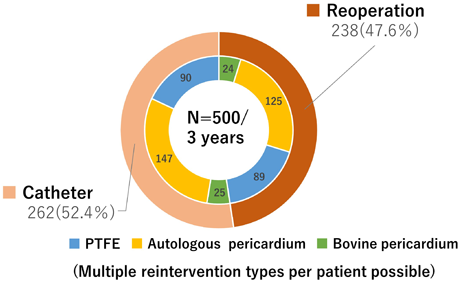
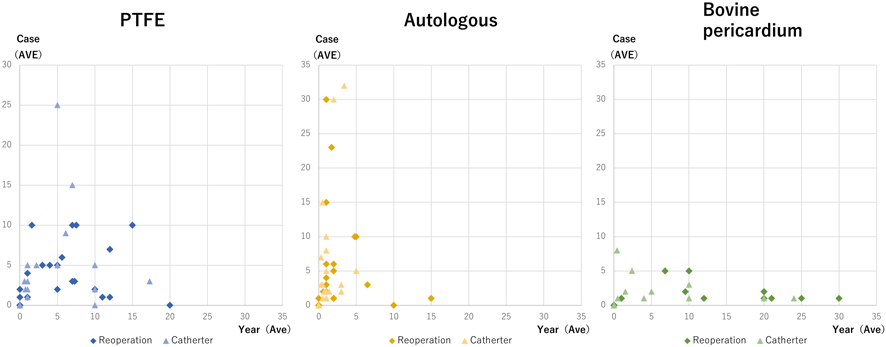
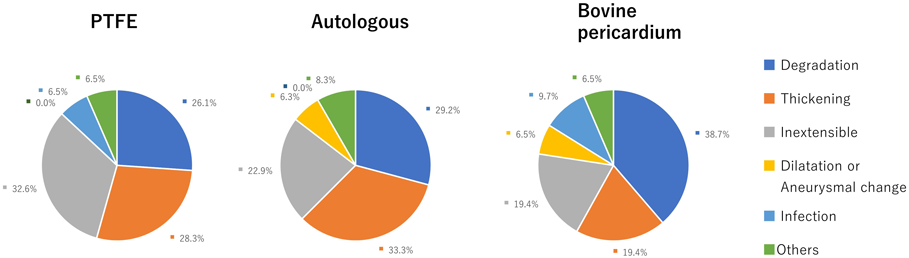
日本小児循環器学会アンケートを活用した右室流出路–肺動脈領域における術後再治療介入の調査および医療費の試算National Survey by the Japanese Society of Pediatric Cardiology and Cardiac Surgery for an Overview of Re-Interventions after Surgical Reconstruction of the Right Ventricular Outflow Tract and/or Pulmonary Artery and an Estimation of Their Medical Cost
1 大阪医科薬科大学病院小児心臓血管外科Department of Pediatric Cardiovascular Surgery, Osaka Medical and Pharmaceutical University Hospital ◇ Takatsuki, Osaka, Japan
2 大阪医科薬科大学病院小児科Department of Pediatric, Osaka Medical and Pharmaceutical University Hospital ◇ Takatsuki, Osaka, Japan
3 東京都立小児総合医療センター循環器科Department of Cardiology, Tokyo Metropolitan Children’s Medical Center ◇ Tokyo, Japan
4 日本小児循環器学会臨床試験委員会Clinical Trials Committee, Japanese Society of Pediatric Cardiology and Cardiac Surgery (JSPCC)