日本の新生児医療は世界でも新生児死亡率,特に極低出生体重児の死亡率が低い.海外の多くと異なり,日本では多くの新生児科医が自ら心臓超音波検査(心エコー)を施行し,循環を評価し,早期より積極的に循環管理を行っていることが日本の優れた成績と関連していることが示唆されている1).
出生という胎内から胎外への移行に際しては,呼吸・循環動態の大きな変化が生じる.児は出生直後から呼吸を開始し,胎盤循環から肺呼吸を土台にした循環へと移行し,静脈管,動脈管,卵円孔が閉鎖する.その変化に対応するために,胎児期より様々な準備が始まっていることが知られている2, 3).
しかし,病的新生児や早産児ではその準備が不十分なまま出生する.出生後の循環への適応不全の病態を適切に評価し,介入することで,早産児の生命予後だけでなく,脳室内出血などの合併症の減少につながっている可能性がある4).しかし,28週未満の超早産児における合併症回避にはさらなる改善の余地がある5).そこで,本稿では,新生児のさらなる予後改善への土台となることを目的として,先天性心疾患を伴わない新生児に対してNICUの中で行われている心機能・循環動態評価について概観した.
出生に際し,胎盤循環を接続した低圧系の胎児循環から,肺循環が確立した新生児循環へ大きく変化する.
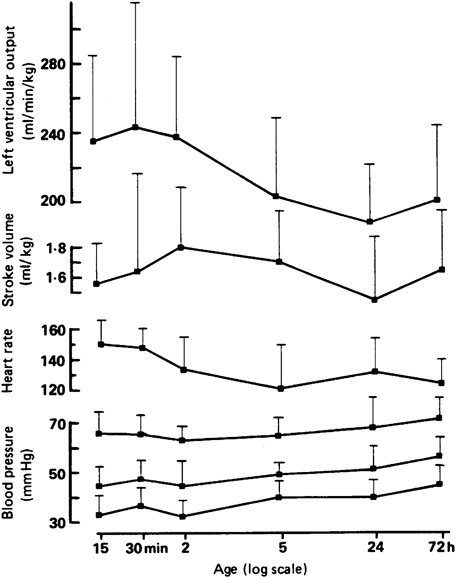
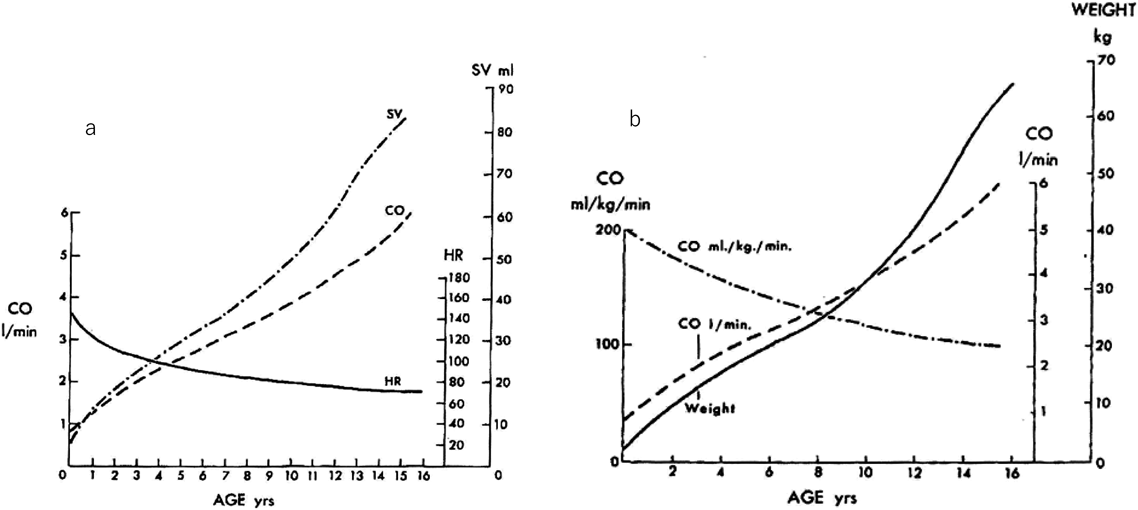
出生に伴い肺血管抵抗は低下し,肺血流は著明に増加する.左室には肺血流量の増加(Fig. 1)により急速に容量負荷がかかり,胎盤循環の消失により圧負荷がかかる2).左室はこの変化に適応する必要がある.胎児期に肺動脈から大動脈に流れていた動脈管は,出生後の肺血管抵抗の低下に伴い大動脈から肺動脈方向へと血流方向が逆転し,正常ではやがて閉鎖に向かう.この変化により左房,左室への容量負荷が増加し,ピークを越える.Rudolphによれば,出生前の満期の羊胎仔における左右心室の総心拍出量は約450 mL/min/kg,右室心拍出量は300 mL/min/kg,左室心拍出量は150 mL/kg/minとされている.しかし,出生直後の左室拍出量は300~425 mL/min/kgであるので,左室拍出量と右室心拍出量の合計は600~850 mL/kg/minに増加する.出生後の総心拍出量は胎児期から30~80%,左室拍出量は2~3倍程度に増加する9).出生後に右室拍出量の総心拍出量に占める割合は減少するが,右室拍出量自体は増加する9).出生後に心拍出量が増加する理由は不明である10).またヒトにおける出生後の左室拍出量も,出生30分で250 mL/kg/minであり,72時間に向けて200 mL/kg/minまで減少する(Fig. 2)11).このように新生児は出生直後に高心拍出量の時期があり,そして成人と比較して,血圧は低いが,心拍数が多く,体重あたりの心拍出量が多い(Fig. 3)9).くわえて,新生児の未熟な心筋では,負荷の増加へ対応域が狭い12–14).
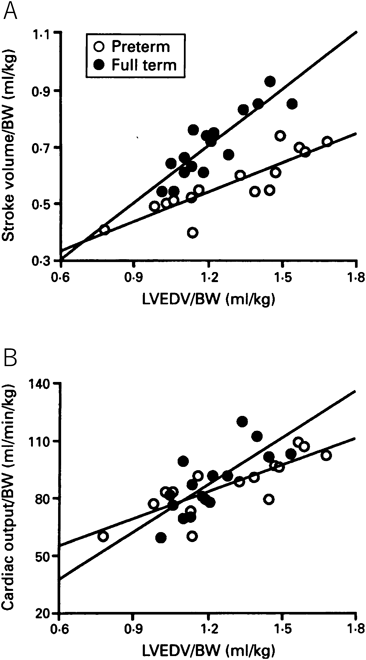
さらに早産児の心臓では,成熟児と比較して,前負荷(左室拡張末期容積)の増大に対する一回拍出量の増大が少ない.心拍出量は一回拍出量に心拍数を乗じたものであり,心拍出量では早産児と成熟児の差は少なくなる(Fig. 4).しかし成熟児と比較して早産児では回帰直線の傾きはやや緩く,前負荷増大に際しての心拍出量の増加はやや乏しいことがうかがわれる15, 16).
新生児では心機能評価の際には皮膚を含めた組織の脆弱性について考慮する必要がある.たとえば24週未満の早産児では,表皮が薄いため通常,あるいは未熟児用の心電図電極でも皮膚損傷を来し,感染症から,生命に危険が及ぶこともある17).このため我々の施設では,トレックスガーゼ@などの非固着性保護シートを電極と皮膚の間に挟み皮膚への接着を予防し,皮膚の保護を図っている.
さらに,血圧測定において新生児では血圧が低いため,ゼロ点をしっかりと合わせる必要がある.そして,生後早期の新生児では動脈ラインとして末梢動脈以外に臍帯動脈を使用できる.必要時にはいずれかを確保して血圧を連続的にモニタリングする.いずれも確保困難な際は,皮膚損傷に注意しながらマンシェットを用いた非観血的血圧測定を行う.高心拍数や循環が不安定な場合には,非観血的に測定した血圧は,臍動脈での計測に比して低値となりやすい18, 19).安定した循環では,適切なサイズのカフを使用して非観血的に測定した平均血圧は,観血的に測定した平均血圧をよく反映する20).
特に超早産児では検査時間を可及的に短くする必要がある.児に直接接触している時間は児へのストレスであり,全身状態に影響を与え得る.呼吸循環管理を要する早産児では,生後の安定した状態の確保・維持に鎮静を要することもある.鎮静中は血圧低下など血行動態が変化し得るため,鎮静が適切かを併せ評価する.成熟児の心エコー検査は,哺乳後の入眠時に行えば鎮静薬を使用するより生理的な状態で評価できる.検査に鎮静が必要なのは詳細・正確な心エコー評価が必要な手術前などごく一部に限られ,心エコー検査のみを目的とした鎮静は行わないことが多い.
新生児の心機能評価法は,成人と同様に多くの方法がある.そのなかで新生児の心機能評価は,その簡便性,即時性,得られる情報の多さから心エコーによるものが中心となる.ここでは,心エコーを中心に新生児で頻用される心機能評価方法について述べる.
前負荷
生理学の基本である心室圧容積関係では,前負荷は左室拡張末期容積で表される21).代用として左室拡張末期径を測定すれば,身長からの予測径を算出でき22),それに対する% of normalを計算することにより前負荷を簡便に評価できる21).
中心静脈圧(central venous pressure: CVP)は前負荷の指標として参考にされる.新生児におけるCVPを下大静脈(inferior vena cava: IVC)径から推定する方法が複数,報告されている23–25).IVC径のみ自体で十分な精度でCVPを予測できる報告は見いだせない24, 25).SatoらはIVCの短径/長径比とCVPの正相関,すなわちCVPが上昇すると楕円形が円形に近づくことを挿管・人工呼吸中を含む新生児で報告している23).HrudaらはIVC縦径の変化率が陽圧換気中でない児でのみCVPと相関したが,陽圧換気下では相関はみられなかったと報告している24).これに対し同様のIVC縦径の変化率が陽圧換気中でも極めて高いCVPとの相関を有するという報告もあり,これまでの報告は一定しない25).IVC径の計測の検者間誤差は大きいと推測されるがその検討は十分ではなく,新生児でCVPを知りたい状況はほぼ陽圧換気中であることを考慮すると,①CVP推定にIVC径自体の有用性は低い,②IVCの短径/長径比,縦径変化率はCVP推定に有用性が期待されるが,陽圧換気中において十分に確立されているとは言えない.その認識のもと,IVC径をCVP評価に用いる際は参考にとどめ,慎重に使用するのが大切と考える24).
後負荷
心室圧容積関係では,後負荷は収縮末期血圧(平均動脈圧で代用される)を一回拍出量で除した実効動脈エラスタンスで表される21).実効動脈エラスタンスは1 mLを拍出するのに必要な収縮末期圧であり,同じ一回拍出量ならば平均動脈圧が高いほど,同じ平均動脈圧ならば一回拍出量が小さいほど,高くなる.もし平均動脈圧が高くて壁運動が低下していれば,壁応力を計算するまでもなく後負荷の上昇を指摘できる.
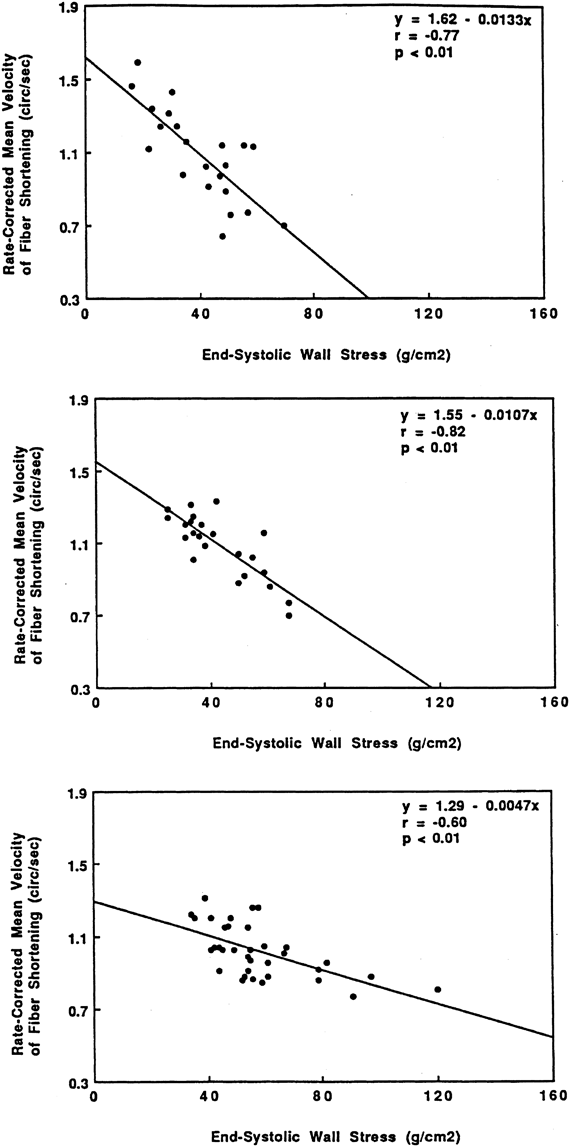
極低出生体重児における循環管理におけるストレス・速度関係の知見が近年蓄積されてきている4, 26).ストレス・速度関係で横軸に用いられる壁応力は後負荷の指標の一つであり,①収縮末期圧が上昇するほど,②収縮末期の壁厚/内径比が小さくなるほど(ストレッチされるほど)上昇する.壁応力は臍帯結紮の瞬間以降も生後48時間にかけて上昇を示す(Fig. 5).その一因としてこの同じ時間帯に体血圧が上昇することが挙げられる.この体血圧の上昇は,動脈管の閉鎖,体内の神経液性因子の変化,胎盤由来のプロスタグランジンの減少をはじめ,多くの変化の結果と考えられる.
極低出生体重児では,脳室内出血や肺出血を起こしている児の壁応力が起こしていない児に比較し,高値となっていることが報告された4).左室の負荷上昇が肺出血のみならず,脳室内出血と関連するという興味深い観察は以下のような注意深い解釈を要する.脳室内出血の多くは体静脈うっ血によると考えられるが,左室と体静脈うっ血の関連として,左室収縮能の低下があれば右室収縮能の低下も併存するかもしれない.また,心室連関により左室拡張末期圧の上昇は右室拡張末期圧を上昇させ得る.左房圧が上昇すれば肺動脈圧は上昇し,右室後負荷の上昇につながる.さらに左房圧の上昇は,卵円孔を介して左房から右房への短絡血流を増加させる.このように左室の負荷上昇は,体静脈うっ滞に影響を与え得る.また,収縮末期壁応力は①収縮末期圧が上昇するほど,②収縮末期の壁厚/内径比が小さくなるほど上昇する.収縮末期の壁厚/内径比が収縮末期に小さくなるということは,収縮末期径の増加を示唆する.収縮末期径の増加は,壁運動の低下や,前負荷(拡張末期容積)の増大によって生じる.したがって壁応力は後負荷指標の一つではあるが前負荷や収縮性の影響を多分に受ける.壁応力の増大が示されたなら,その中身について,すなわち血圧,前負荷,収縮性についてもあわせて考えることが正しい評価・介入につながる.これについては次項でも述べる.
心収縮能
駆出率,短縮率,心拍補正左室平均円周短縮速度(rate-corrected mean velocity of fiber shortening: mVcfc)がよく用いられている.駆出率は心室容積の変化割合,すなわち拡張末期容積に対する一回拍出量の割合であり,成人の心不全の分類(駆出率が低下した,あるいは保持された)に使用され,心室のエネルギー効率とも関連する.短縮率は心室径の変化割合である.これらの算出は比較的容易で直感的に理解しやすいため,現在でも頻用される.しかし,駆出率や短縮率は負荷の影響を大きく受けるため,使用にあたっては負荷を考慮に入れて収縮能を評価する必要がある.たとえば同じ収縮能であっても,後負荷が上昇するだけで駆出率が低下することは心室圧容積関係により明らかである21).生後は生理的に肺高血圧が残存するため左室は丸くなく,M-modeのみによる駆出率や短縮率が必ずしも正確に容積変化を反映しないが,わかりやすく簡便なため臨床的には有用であり,頻用されている27, 28).
mVcfcは短縮率をRR間隔と駆出時間で調整したものであり,mVcfc自体が収縮能というよりは,駆出率や短縮率と同様,壁運動指標の一つと考えられる.ストレス・速度関係(Fig. 6)はmVcfcを壁応力と組み合わせて評価するものであり,負荷の程度と,心筋が負荷に見あって収縮できるかを評価する29).ストレス・速度関係はNICUでも非侵襲的に定量でき,ある時点の循環動態やその経時変化の評価に有用である.日本の新生児領域でストレス・速度関係が普及することにより,心室の負荷・負荷に見合った壁運動といった生理的な視点が得られたことは歴史的に意義深いと著者らは考える.ストレス・速度関係はFig. 6のように右下がりの関係であり,壁応力の上昇とともにmVcfcで表される壁運動は低下する.壁運動(mVcfc)が低下している場合に壁応力が低ければ(ストレス・速度関係の左下)収縮性の低下が存在するため,その原因と対策を探り,必要があれば強心薬を考慮する.壁運動が低下し壁応力が高ければ(ストレス・速度関係の右下),問題点の主体は負荷の増大である.負荷を減じることにより壁運動は改善し得る(ストレス・速度関係の左上方向への変化・改善).前項に記載したように壁応力の解釈には注意を要し,左室の大きさも評価したうえで,前負荷・後負荷のどこに問題があるのかを考える.介入が必要ならば,利尿薬・血管拡張薬・動脈管開存症に対する薬物療法といった減負荷治療の中で何が最適かを考える必要がある4).
心室拡張能
心室の拡張能は拡張早期の弛緩と跳ね返り(elastic recoil),および拡張期後半の心筋の硬さ(stiffness)で規定される30).すなわち拡張早期の拡張能は,収縮末期からの等容性の弛緩期に心室圧がいかに速やかに低下するか,拡張期後半は血液流入により拡張期心室圧がいかに上昇してしまうか,で評価される.しかしこうした拡張能評価は通常の心臓カテーテル検査を行っても難題である.心エコーでは,さらに難しい.左室流入波形のE波(拡張早期),A波(拡張後期),および房室弁輪の移動速度を組織ドプラ法で計測したe′波(拡張早期),a′波(拡張後期)を測定し,拡張能が推測されてきた.e′は拡張早期の長軸方向の心筋組織の運動速度であるため弛緩時定数と,E/e′は左室充満圧と関連する31)指標として用いられてきた30).これらの指標は新生児でも計測され,評価の参考とされる(Table 1)32–39)が,新生児では侵襲的評価によって検証されておらず,その妥当性は不明である.したがってその評価は参考にとどめるべきである.成人でもE/e′が左室充満圧と相関がみられない状況が数多く報告され,小児でも緩い相関が認められる40)のみである.これらの心エコーの計測には前負荷・後負荷依存性や計測角度の問題があるのに加え,右心では呼吸の影響も大きい.
Table 1 Tissue Doppler reference values| Reference and TDI mode | Index | Location |
|---|
| Left lateral | Septum | Right lateral |
|---|
| Lee et al.33) cTDI | | | | |
| GA<28 weeks | Systolic peak (s′) (cm/s) | 1.8 (0.7) | | 2.8 (0.9) |
| First 24 h | Diastolic peak (cm/s) | 2.3 (1.1) | | 4.1 (1.6) |
| Displacement (mm) | 1.9 (0.9) | | 3.3 (1.2) |
| Joshi et al.34) cTDI | | | | |
| Premature (≤34 weeks) and mature (≥38 weeks) | Systolic peak (s′) (cm/s) | 2.4 (0.9) | 2.9 (0.9) | 4.4 (1.1) |
| Within first 72 h | Early diastolic peak (e′) (cm/s) | 4.9 (2.4) | 4.7 (2.3) | 6.2 (2.7) |
| Late diastolic peak (a′) (cm/s) | 2.9 (1.0) | 3.7 (1.1) | 5.8 (1.3) |
| Displacement (mm) | 3.9 (1.7) | 4.7 (1.2) | 7.5 (1.9) |
| Saleemi et al.35) pwTDI | | | | |
| GA 24–27 weeks | Systolic peak (s′) (cm/s) | 3.5 (1.0) | | |
| 48 h of age | Early diastolic peak (e′) (cm/s) | 3.8 (0.9) | | |
| Late diastolic peak (a′) (cm/s) | 4.3 (1.0) | | |
| GA 28–31 weeks | Systolic peak (s′) (cm/s) | 3.8 (0.8) | | |
| 48 h of age | Early diastolic peak (e′) (cm/s) | 3.9 (1.0) | | |
| Late diastolic peak (a′) (cm/s) | 4.2 (0.7) | | |
| GA 32–35 weeks | Systolic peak (s′) (cm/s) | 4.7 (1.2) | | |
| 48 h of age | Early diastolic peak (e′) (cm/s) | 4.8 (1.2) | | |
| Late diastolic peak (a′) (cm/s) | 5.2 (0.9) | | |
| Breatnach et al.36) | | | | |
| GA<29 weeks | Systolic peak (s′) (cm/s) | 2.8 (0.9) | 2.4 (0.6) | 3.6 (0.9) |
| First 24 h (see paper for further time points) | Early diastolic peak (e′) (cm/s) | 3.6 (1.4) | 2.8 (0.8) | 3.9 (1.3) |
| Late diastolic peak (a′) (cm/s) | 4.0 (1.5) | 3.9 (1.1) | 3.9 (1.1) |
| Ciccone et al.37) pwTDI | | | | |
| GA 31–36 weeks | Systolic peak (s′) (cm/s) | 5.4 (0.8) | 4.5 (1.4) | 5.5 (0.9) |
| Days 3–4 | Early diastolic peak (e′) (cm/s) | 7.6 (1.2) | 2.7 (0.7) | 6.2 (1.3) |
| Late diastolic peak (a′) (cm/s) | 7.5 (1.3) | 6.5 (0.7) | 9.4 (1.1) |
| GA 37–41 weeks | Systolic peak (s′) (cm/s) | 5.6 (0.8) | 5.1 (0.4) | 6.1 (0.9) |
| Day 3–4 | Early diastolic peak (e′) (cm/s) | 7.9 (1.2) | 6.1 (0.8) | 7.9 (1.1) |
| Late diastolic peak (a′) (cm/s) | 7.5 (1.3) | 6.7 (0.8) | 9.5 (1.1) |
| Negrine et al.38) pwTDI | | | | |
| GA<30 weeks | Systolic peak (s′) (cm/s) | 3.7 (0.6) | | 5.0 (0.6) |
| First 24 h | Early diastolic peak (e′) (cm/s) | 4.2 (0.8) | | 4.2 (1.1) |
| Late diastolic peak (a′) (cm/s) | 5.4 (2.2) | | 7.3 (1.1) |
| GA 30–36 weeks | Systolic peak (s′) (cm/s) | 4.3 (0.7) | | 5.9 (0.9) |
| First 24 h | Early diastolic peak (e′) (cm/s) | 5.7 (1.4) | | 6.2 (1.0) |
| Late diastolic peak (a′) (cm/s) | 6.0 (1.9) | | 7.7 (1.8) |
| Term | Systolic peak (s′) (cm/s) | 5.3 (1.0) | | 6.9 (1.2) |
| First 24 h | Early diastolic peak (e′) (cm/s) | 6.4 (1.2) | | 7.3 (1.1) |
| Late diastolic peak (a′) (cm/s) | 7.1 (1.8) | | 8.1 (1.6) |
| Mori et al.39) pwTDI | | | | |
| Term | Systolic peak (s′) (cm/s) | 5.3 (0.9) | 3.7 (0.6) | 6.2 (1.1) |
| First 24 h | Early diastolic peak (e′) (cm/s) | 7.5 (1.5) | 5.0 (1.0) | 7.5 (1.4) |
| Late diastolic peak (a′) (cm/s) | 6.2 (1.4) | 4.9 (1.0) | 9.2 (1.6) |
| Peak systolic (s′), early diastolic (e′), and late diastolic (a′) velocities and displacement of the AV-valve plane in premature and mature neonates. Pulsed-wave (pwTDI) and color-coded tissue Doppler (cTDI) indices (mean (standard deviation)). GA, gestational age; pwTDI, pulsed-wave (pw TDI). Modified from Nestaas E et al.32) with permission. |
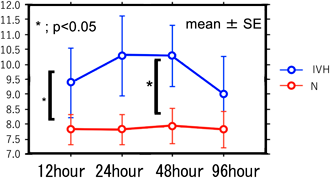
そうした限界はあるものの,新生児でもこれらの指標が呼吸症状41–43),脳室内出血例44)(Fig. 7),予後45)と関連するとの報告がある.これらの指標が拡張能の何を表すか・表さないかは不明であるが,臨床上有用な情報が得られる可能性はあるかもしれない.
ドプラ法を用いない拡張能指標である左房容積はより直接的に拡張能を反映する可能性がある.左房容積を体表面積で除した左房容積係数が,成人では拡張能評価に使用されている46).一方で左室拡張能が一定のもとでは,左房容積は容量負荷の程度を反映するため,動脈管開存症の病勢評価に有用性が見込まれる.動脈管開存症では肺血流量が増加し,その血流は左房に還流するからである.反対に同程度の容量負荷ならば,左房容積は左室拡張能,特に左室stiffnessと関連する.
左房容積の指標としては,左房大動脈径比(LA/Ao比)と,左房容積自体が挙げられる.動脈管手術を行わなかった早産児の日齢3の計測でLA/Aoは1.21±0.20,左房容積/出生体重は0.57±0.26(mL/kg)と報告されている47).これらの指標は症候性動脈管開存症で有意に大きいことが報告されている48, 49).LA/Ao比は左房径を大動脈径で除して正規化しているため体格依存性がなく,使用しやすい45, 47, 48).しかし,LA/Ao比も左房容積も,卵円孔を介した心房間左右短絡のため拡張能低下・容量負荷の程度を過小評価する可能性がある.また,両者ともに検者間誤差が非常に大きい50).したがって心エコー指標の測定の標準化が今後の課題である.心エコーでは,得られた指標だけでなく2D画像そのものを診ることが重要と考える.脳室内出血と静脈うっ滞の関連が考えられている43)ことから,新生児の容量負荷と拡張能の関連は重要と考えられ,さらなる知見の集積が期待される.
血圧
心室圧容積関係では,収縮末期圧(平均血圧で代用される)と一回拍出量は,ある前負荷(拡張末期容積)のもと,①負荷に依存しにくい収縮性の指標である収縮末期エラスタンスと②後負荷を表す実効動脈エラスタンスの関係で決まる.これを心室血管統合関係という.つまり収縮末期圧も一回拍出量も,循環調節の結果で決まるという考え方である.血圧は体格により標準値が異なる51).かつては早産児では血圧維持が循環管理の目標であったこと,現在では組織循環が保たれていれば低血圧を許容し得るというpermissive hypotensionの概念が広まってきたことは先述した8).ただし,平均血圧(から中心静脈圧を減じたもの)は体血管抵抗と心拍出量を乗じたものであり,極度に血圧が低下すれば心拍出量や臓器血流は維持できないはずである.組織循環を維持するために絶対的に必要な血圧も存在すると思われる.今後の検討を期待したい.
心拍出量
心臓が一分間に拍出する血液量である.心収縮能障害や,先天性血管疾患による高心拍出量心不全に際してはその病態把握に有用である.新生児の心拍出量の測定は,超音波法とインピーダンス法とが頻用される(Table 2)52).
Table 2 Assessment methods of Cardiac Output and intravascular volume| Method | Hemodynamic variables | Limitations | Invasiveness and monitoring frequency | Applicability |
|---|
| Neonatologist performed echocardiography(NPE) | CO, vena cava superior flow, shunts, structural and functional abnormalities Left ventricular enddiastolic volume Vena cava collapsibility | Intensive trainingIntra-/interobserver variability 20% Error in assessment of VTI (angle of insonation) and CSA | Non-invasive Intermittent | Clinical use (absolute values of CO) Preload assessmentlimited for clinical use |
| Transcutaneous doppler (USCOM®) | CO | Large interobserver variabilityError in assessment of VTI (angle of insonation) and CSA No anatomical verification of sample area Low precision | Non-invasive Intermittent | Limited clinical use (trend monitoring) |
| Thoracic electrical bio-impedance (ICON®, NICOM®) | CO | Influenced by position of surface electrodes, changes in tissue water content (pulmonary edema, pleural effusion), alterations in heart rate and motion artifacts | Non-invasive Continuous | Clinical use (trend monitoring) |
| Arterial pulse contour analysis (APCA) | CO PPV, SVV, HRV | Influenced by changes in vascular compliance, vasomotor tone, medication, irregular heart rate, and motion artifactsInfluenced by physiological aliasingFrequent calibration necessary | Invasive Continuous | Research setting Research setting |
| TPTD | CO Hemodynamic volumes (GEDV, ITV) | Use of ice-cold saline Thermistor-tipped catheter needed Arterial (femoral) and central venous catheter needed Fluid overload after multiple injections | Invasive Continuous | Only >3 kg Research setting |
| TPUD | CO, shunt detection andquantification Continuous CO Hemodynamic volumes (TEDV, CBV, ACV) EVLW | Arterial and central venous catheter needed Risk of fluid overload after multiple injections | Invasive Intermittent Continuous measurement possible (APCA) | Clinical use (absolutevalues of CO) APCA as trend monitoring Research setting |
| Stop flow method Plethysmographvariability index | Mean systemic filling pressure Perfusion index Fluid responsiveness | Venous and arterial access in the same extremityInfluenced by physiological factors (higher thoracic and arterial compliance and low tidal volumes compared to adults) and physiological aliasing | Invasive Intermittent Non-invasive Continuous | Research setting Research setting |
| ACV, active circulating volume; CBV, central blood volume; CO, cardiac output; CSA, cross-sectional area; EVLW, extra vascular lung water; GEDV, global end-diastolic blood volume; HRV, heart rate variability; IDF, incident dark field imaging; ITBV, intrathoracic blood volume; NIRS, near infrared spectroscopy; OPS, orthogonal polarization spectral; PPV, pulse pressure variation; SDF, sidestream darkfield imaging; SVV, stroke volume variation; TEDV, total end-diastolic volume; TPTD, transpulmonary thermodilution; TPUD, transpulmonary ultrasound dilution; VTI, velocity-time integral. Modified from from Vrancken SL et al. 52) with permission. |
早産児
早産児は,生後の循環への移行の適応に十分な成熟が必ずしも得られておらず,適応障害から循環不全を来す症例が存在する53).壁応力が高値である早産児において,少量のニトログリセリンの静脈投与により脳室内出血や肺出血が減少する可能性が示唆されている4).ニトログリセリンは動静脈の拡張作用を有し,動脈拡張による血圧の低下(後負荷の軽減),静脈拡張による静脈プールの増加による前負荷軽減(うっ血の軽減)の両者により壁応力は低下し得る.脳静脈のゆらぎの改善との関連も示唆されている54).血管拡張薬の使用は,投与前にすでに低血圧がある際は危険であること,動脈管拡張のリスクがあることを念頭に置き,必要性を吟味する.今後,どのような投与対象でニトログリセリンが有効かを前方視的検討で同定する必要がある4, 53, 54).
壁応力が十分に低く管理されていても,脳室内出血を来す症例が存在する4, 53, 54).
脳室内出血を来す症例では上大静脈の血流の減少が認められるとの報告55)や,内大脳静脈の揺らぎが大きい症例で脳室内出血が多いとの報告54)があり,静脈うっ血の回避を意識した管理の必要性が指摘されている.
双胎間輸血症候群(Twin-to-twin transfusion syndrome; TTTS)
一絨毛膜性二羊膜性双胎(monochorionic- diamniotic 双胎;MD双胎)は双胎で胎盤を共有するため,胎盤上の吻合血管を通じ,胎児間で血流の不均衡を生じやすい.現在,内分泌仮説によりTTTSの病態が説明されている56).胎児期に施行される胎児鏡下レーザー凝固術(fetoscopic laser photocoagulation for communicating vessels: FLP)により新生児期に循環不全を発症する児は減少してきている57, 58).
しかし,FLPの適応から外れたMD双胎でも,出生後に循環不全を発症する症例がいる.出生前には循環不全を発症しないと予想された症例の中にも,出生後に循環不全を発症する症例がある59).こうした出生後の循環不全を出生前に予測する確立された方法はない.しかし,出生時の臍帯血BNP(brain natriuretic peptide)が出生後の循環不全を予測できるとの報告もあり,今後の検討が望まれる60).循環不全は大児と小児では循環状態が大きく異なり,適切な循環評価と管理が必要である.大児では,胎内での容量負荷と心筋肥厚が生じており,極端に低い壁応力と過大な心拍出量が観測されることが多い.また,ナトリウム利尿ペプチドの過剰により,出生後に多尿をきたし,循環血液量の減少が生じる.そして,胎内では小児で分泌され移行したレニン・アンジオテンシン・アルドステロンが出生後は供給されなくなるため,大児では血圧を保ちにくい.これらに対応するため,大児に対しては適切な容量負荷と,供給が途絶えたレニン・アンジオテンシン・アルドステロンのかわりに血管収縮薬を必要とすることが多い.小児では,胎内では容量負荷が少なく,出生後は胎児期と比して容量負荷がかかる.心筋壁は薄く,壁応力は上昇しやすい.胎内から引き続く腎機能障害によって出生後も乏尿をきたしやすい.貧血も合併する.これらが複合し,小児においては容量負荷に適応しにくい.動脈管開存症など容量負荷がかかる病態を適切に評価し,多彩な病態を管理する必要がある61, 62).
早産児動脈管開存症
動脈管開存症は呼吸・循環を悪化させる重要な疾患である.脳室内出血や肺出血のリスクであり,生命および神経学的予後に影響を与える.このため,適切・適時の介入・非介入の決定のため,その重症度評価が重要である.日本の34施設のNICUで前方視的に行ったPLASE研究では,動脈管結紮術の予測に,動脈管径と左肺動脈拡張末期速度というシンプルで計測しやすい指標が最も有用であった47, 48, 63).これらの指標は,本総説で記述してきた左室拡張末期径,左房容積,LA/Ao比よりも優れていたという結果であり,興味深い.より本質的と考えられる指標でも,測定誤差が大きな指標50)では多施設・多数の検者間における互換性が懸念される.手術適応の判断も施設ごと,患者ごとに個別に決定され,一律の判断基準ではないことも多施設研究を難しくさせている.しかし,実臨床では動脈管手術を適応とする理由も,不安定な血行動態,栄養が進まない・腸管障害,腎障害,呼吸障害などと多岐にわたる48)ため,動脈管手術の適応は個々の症例で最終判断する必要があり,個々で負荷と機能の評価が必要である.
引用文献References
1) Isayama T: The clinical management and outcomes of extremely preterm infants in Japan: Past, present, and future. Transl Pediatr 2019; 8: 199–211
2) Klopfenstein HS, Rudolph AM: Postnatal changes in the circulation and responses to volume loading in sheep. Circ Res 2018; 42: 839–845
3) Rudolph AM: The changes in the circulation after birth their importance in congenital heart disease. Circulation 1970; 41: 343–359
4) Toyoshima K, Kawataki M, Ohyama M, et al: Tailor-made circulatory management based on the stress-velocity relationship in preterm infants. J Formos Med Assoc 2013; 112: 510–517
5) Siffel C, Kistler KD, Sarda SP: Global incidence of intraventricular hemorrhage among extremely preterm infants: A systematic literature review. J Perinat Med 2021; 49: 1017–1026
6) Bozkurt B, Coats AJ, Tsutsui H, et al: Universal Definition and Classification of Heart Failure A Report of the Heart Failure Society of America, Heart Failure Association of the European Society of Cardiology, Japanese Heart Failure Society and Writing Committee of the Universal Definition of Heart Failure. J Card Fail 2021; 27: 387–413
7) Dempsey EM, Barrington KJ: Treating hypotension in the preterm infant: When and with what: A critical and systematic review. J Perinatol 2007; 27: 469–478
8) Dempsey EM, Hazzani FA, Barrington KJ: Permissive hypotension in the extremely low birthweight infant with signs of good perfusion. Arch Dis Child Fetal Neonatal Ed 2009; 94: F241–F244
9) Rudolph AM: Perinatal and postnatal pulmonary circulation, in Congenital Disease of the Heat Clinical-Physiological Considerations. 3rd ed. Wiley-Blackwell, 2009, pp87–114
10) 稲村 昇: 胎児循環生理.日小児循環器会誌2016; 32: 451–461
11) Winberg P, Jansson M, Marions L, et al: Left ventricular output during postnatal circulatory adaptation in healthy infants born at full term. Arch Dis Child 1989; 64: 1374–1378
12) Crepaz R, Pitscheider W, Radetti G, et al: Age-related variation in left ventricular myocardial contractile state expressed by the stress velocity relation. Pediatr Cardiol 1998; 19: 463–467
13) Kimball TR, Daniels SR, Khoury P, et al: Age-related variation in contractility estimate in patients ≤20 years of age. Am J Cardiol 1991; 68: 1383–1387
14) 片山博視:End-systolic wall stressから見た先天性心疾患の非侵襲的心機能評価の検討.東女医大誌1990; 60(1): 69–81
15) Takahashi Y, Harada K, Ishida A, et al: Left ventricular preload reserve in preterm infants with patent ductus arteriosus. Arch Dis Child Fetal Neonatal Ed 1994; 71: F118–F121
16) Bussmann N, Breatnach C, Levy PT, et al: Early diastolic dysfunction and respiratory morbidity in premature infants: An observational study. J Perinatol 2018; 38: 1205–1211
17) 八田恵利:新生児の皮膚ケアハンドブック.メディカ出版,2013, pp8–13
18) Meyer S, Sander J, Gräber S, et al: Agreement of invasive versus non-invasive blood pressure in preterm neonates is not dependent on birth weight or gestational age. J Paediatr Child Health 2010; 46: 249–254
19) Emery EF, Greenough A: Non-invasive blood pressure monitoring in preterm infants receiving intensive care. Eur J Pediatr 1992; 151: 136–139
20) Dionne JM, Bremner SA, Baygani SK, et al: International Neonatal Consortium: Method of blood pressure measurement in neonates and infants: A systematic review and analysis. J Pediatr 2020; 221: 23–31.e5
21) 増谷 聡:エコーで診る心機能(一般小児科医~小児循環器医の基本).日小児科学会誌2018; 122: 601–609
22) Nagasawa H: Novel regression equations of left ventricular dimensions in infants less than 1 year of age and premature neonates obtained from echocardiographic examination. Cardiol Young 2010; 20: 526–531
23) Sato Y, Kawataki M, Hirakawa A, et al: The diameter of the inferior vena cava provides a noninvasive way of calculating central venous pressure in neonates. Acta Paediatr 2013; 102: e241–e246
24) Hruda J, Rothuis EGM, van Elburg RM, et al: Echocardiographic assessment of preload conditions does not help at the neonatal intensive care unit. Am J Perinatol 2003; 20: 297–304
25) Mugloo MM, Malik S, Akhtar R: Echocardiographic inferior vena cava measurement as an alternative to central venous pressure measurement in neonates. Indian J Pediatr 2017; 84: 751–756
26) Osborn DA, Evans N, Kluckow M: Left ventricular contractility in extremely premature infants in the first day and response to inotropes. Pediatr Res 2007; 61: 335–340
27) 豊島勝昭,川滝元良,佐藤義朗,ほか:極低出生体重児における左室壁応力・心筋短縮速度の経時的変化と肺出血・脳室内出血・脳室周囲白質軟化症の関連性について.未熟児新生児誌2002; 14(2): 45–52
28) 大手信之,石津智子,泉 知里,ほか:循環器超音波検査の適応と判読ガイドライン.日本循環器学会
29) Toyono M, Harada K, Takahashi Y, et al: Maturational changes in left ventricular contractile state. Int J Cardiol 1998; 64: 247–252
30) 増谷 聡,先崎秀明:先天性心疾患における左室拡張障害の意義とその基本評価.日小児循環器会誌2016; 32: 277–290
31) Hirose A, Khoo NS, Aziz K, et al: Evolution of left ventricular function in the preterm infant. J Am Soc Echocardiogr 2015; 28: 302–308
32) Nestaas E, Schubert U, de Boode WP, et al: European Special Interest Group ‘Neonatologist Performed Echocardiography’ (NPE): Tissue Doppler velocity imaging and event timings in neonates: A guide to image acquisition, measurement, interpretation, and reference values. Pediatr Res 2018; 84 Suppl 1: 18–29
33) Lee A, Nestaas E, Liestøl K, et al: Tissue Doppler imaging in very preterm infants during the first 24 h of life: An observational study. Arch Dis Child Fetal Neonatal Ed 2014; 99: F64–F69
34) Joshi S, Edwards JM, Wilson DG, et al: Reproducibility of myocardial velocity and deformation imaging in term and preterm infants. Eur J Echocardiogr 2010; 11: 44–50
35) Saleemi MSH, El-Khuffash A, Franklin O, et al: Serial changes in myocardial function in preterm infants over a four week period: The effect of gestational age at birth. Early Hum Dev 2014; 90: 349–352
36) Breatnach CR, El-Khuffash A, James A, et al: Serial measures of cardiac performance using tissue Doppler imaging velocity in preterm infants <29weeks gestations. Early Hum Dev 2017; 108: 33–39
37) Ciccone MM, Scicchitano P, Zito A, et al: Different functional cardiac characteristics observed in term/preterm neonates by echocardiography and tissue doppler imaging. Early Hum Dev 2011; 87: 555–558
38) Negrine RJS, Chikermane A, Wright JGC, et al: Assessment of myocardial function in neonates using tissue Doppler imaging. Arch Dis Child Fetal Neonatal Ed 2012; 97: F304–F306
39) Mori K, Nakagawa R, Nii M, et al: Pulsed wave Doppler tissue echocardiography assessment of the long axis function of the right and left ventricles during the early neonatal period. Heart 2004; 90: 175–180
40) Masutani S, Saiki H, Kurishima C, et al: Assessment of ventricular relaxation and stiffness using early diastolic mitral annular and inflow velocities in pediatric patients with heart disease. Heart Vessels 2014; 29: 825–833
41) Kozák-Bárány A, Jokinen E, Saraste M, et al: Development of left ventricular systolic and diastolic function in preterm infants during the first month of life: A prospective follow-up study. J Pediatr 2001; 139: 539–545
42) Çetinkaya M, Bostan Ö, Köksal N, et al: Early left ventricular diastolic dysfunction in premature infants born to preeclamptic mothers. J Perinat Med 2011; 39: 89–95
43) Okumura K, Slorach C, Mroczek D, et al: Right ventricular diastolic performance in children with pulmonary arterial hypertension associated with congenital heart disease. Circ Cardiovasc Imaging 2018; 7: 491–501
44) 横山岳彦,田中太平,村松幹司,ほか:極低出生体重児の脳室出血例における心臓拡張能.日周産期・新生児会誌2010; 46: 593
45) Tao K, Hara Y, Ishihara Y, et al: Cesarean section predominantly affects right ventricular diastolic function during the early transitional period. Pediatr Neonatol 2019; 60: 523–529
46) Nagueh SF, Smiseth OA, Appleton CP, et al: Houston, Texas; Oslo, Norway; Phoenix, Arizona; Nashville, Tennessee; Hamilton, Ontario, Canada; Uppsala, Sweden; Ghent and Liège, Belgium; Cleveland, Ohio; Novara, Italy; Rochester, Minnesota; Bucharest, Romania; and St. Louis, Missouri: Recommendations for the evaluation of left ventricular diastolic function by echocardiography: An update from the american society of echocardiography and the european association of cardiovascular imaging. Eur Heart J Cardiovasc Imaging 2016; 17: 1321–1360
47) Masutani S, Isayama T, Kobayashi T, et al: PLASE (Patent ductus arteriosus and left atrial size evaluation in preterm infants) study group investigators: Ductus diameter and left pulmonary artery end-diastolic velocity at 3 days of age predict the future need for surgical closure of patent ductus arteriosus in preterm infants: A post-hoc analysis of a prospective multicenter study. J Cardiol 2021; 78: 487–492
48) Toyoshima K, Isayama T, Kobayashi T, et al: Patent ductus arteriosus, left atrial size evaluation in preterm infants (PLASE) study group investigators: What echocardiographic indices are predictive of patent ductus arteriosus surgical closure in early preterm infants? A prospective multicenter cohort study. J Cardiol 2019; 74: 512–518
49) Martins F de F, Rios DI, Resende MHF, et al: Relationship of patent ductus arteriosus size to echocardiographic markers of shunt volume. J Pediatr 2018; 202: 50–55.e3
50) 甘利昭一郎,諫山哲哉,裕子岩見,ほか:新生児科医による心エコー静止画上の計測の検者間信頼性.日周産期・新生児会誌2017; 29: 373–382
51) 清悟志賀:極低出生体重児における出生後動脈血圧の基準値に関する研究.日周産期・新生児会誌1996; 32: 493–503
52) Vrancken SL, van Heijst AF, de Boode WP: Neonatal hemodynamics: From developmental physiology to comprehensive monitoring. Front Pediatr 2018; 6: 87
53) 豊島勝昭,渡辺達也,川滝元良,ほか:Stress-Velocity関係を指標として循環管理した在胎23, 24週の超早産児の検討.日周産期・新生児会誌2005; 41: 535–542
54) Ikeda T, Amizuka T, Ito Y, et al: Changes in the perfusion waveform of the internal cerebral vein and intraventricular hemorrhage in the acute management of extremely low-birth-weight infants. Eur J Pediatr 2014; 174: 331–338
55) Kluckow M, Evans N: Low superior vena cava flow and intraventricular haemorrhage in preterm infants. Arch Dis Child Fetal Neonatal Ed 2000; 82: F188–F194
56) Mahieu-Caputo D, Muller F, Joly D, et al: Pathogenesis of twin-twin transfusion syndrome: The renin-angiotensin system hypothesis. Fetal Diagn Ther 2001; 16: 241–244
57) Quintero R, Morales W, Allen M, et al: Staging of twin-twin transfusion syndrome. J Perinatol 1999; 19: 550–555
58) Sago H, Hayashi S, Saito M, et al: The outcome and prognostic factors of twin–twin transfusion syndrome following fetoscopic laser surgery. Prenat Diagn 2010; 30: 1185–1191
59) 横山岳彦,本田義信,川瀬昭彦,ほか:羊水過多過少による双胎間輸血症候群の診断基準を満たさない一絨毛膜二羊膜性双胎の急性期障害と長期予後.日周産期・新生児会誌2017; 53: 966–973
60) 横山岳彦,長柄俊佑,粟屋梨沙,ほか:循環障害を来したMD双胎の尿量についての検討.日周産期・新生児会誌2017; 53:522
61) 横山岳彦:双胎間輸血症候群を発症した小児側における左室拡張末期容量と左室心筋重量の推移.日周産期・新生児会誌2019; 55: 492
62) 矢内里紗:循環障害を伴った,一絨毛膜二羊膜(MD)双胎におけるrenin値の検討.日周産期・新生児会誌2021; 57(suppl): 184
63) Masutani S: Left ventricular end-diastolic dimension for the assessment of the pulmonary to systemic flow ratio in congenital heart diseases. Circ J 2021; 86: 136–137
64) Ishiguro A, Sasaki A, Motojima Y, et al: Randomized trial of perfusion-based circulatory management in infants of very low birth weight. J Pediatr 2022; 243: 27–32.e2