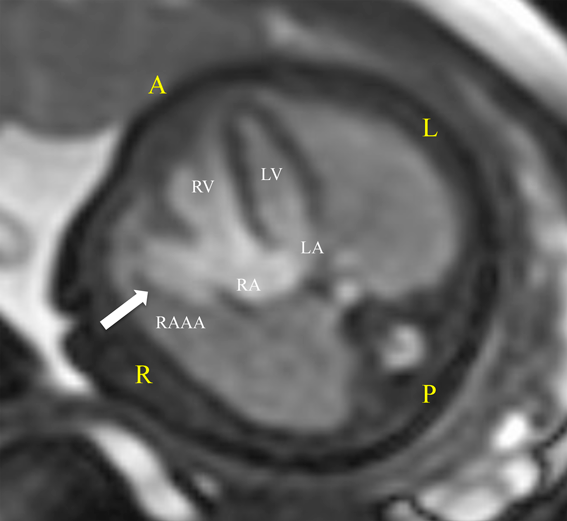
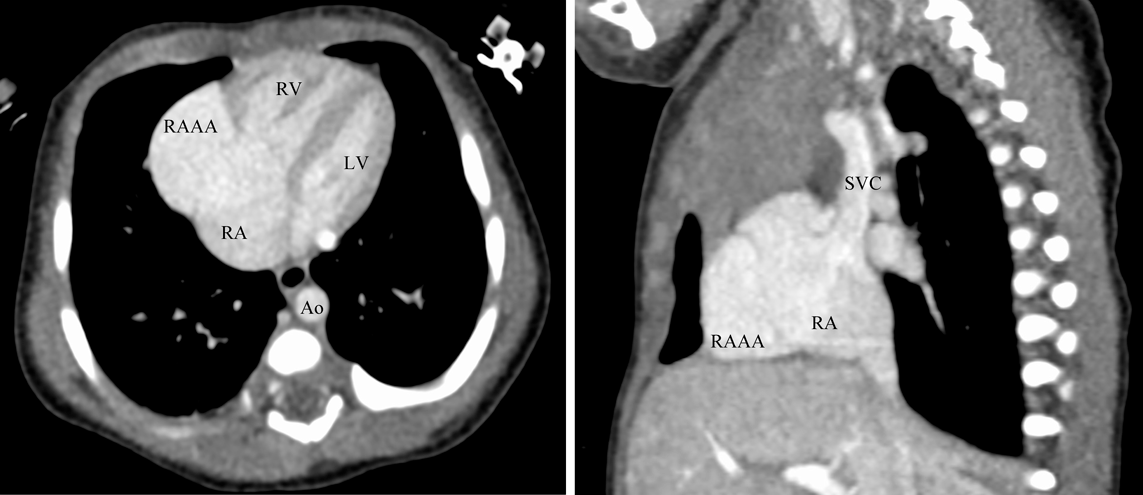
胎児期に診断し,無治療で経過観察できている先天性右心耳瘤の一例A Case of Congenital Right Atrial Appendage Aneurysm Diagnosed Prenatally and Followed-Up Without Treatment
1 旭川医科大学小児科Department of Pediatrics, Asahikawa Medical University ◇ Hokkaido, Japan
2 網走厚生病院小児科Department of Pediatrics, Abashiri-Kosei General Hospital ◇ Hokkaido, Japan