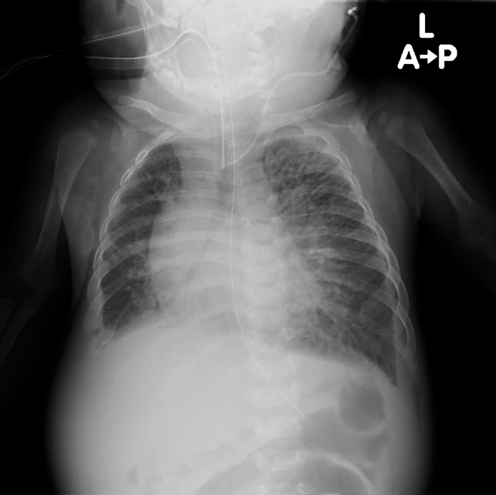
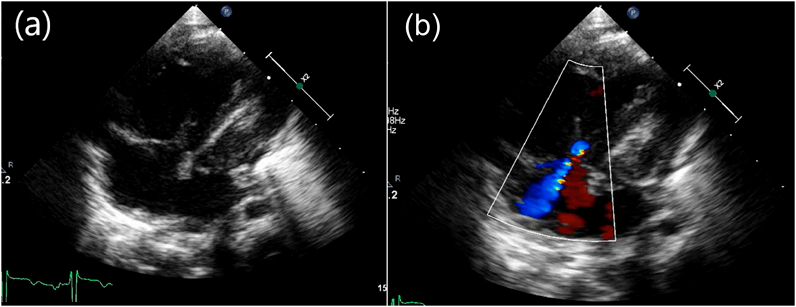
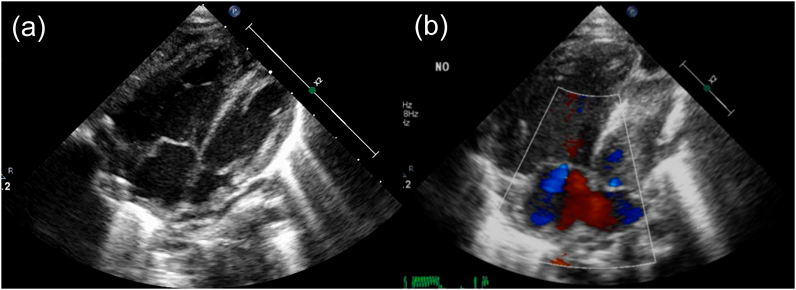
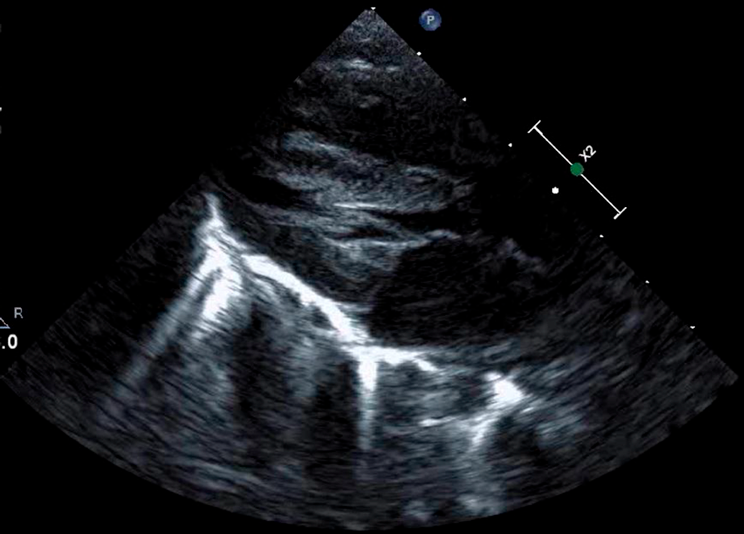
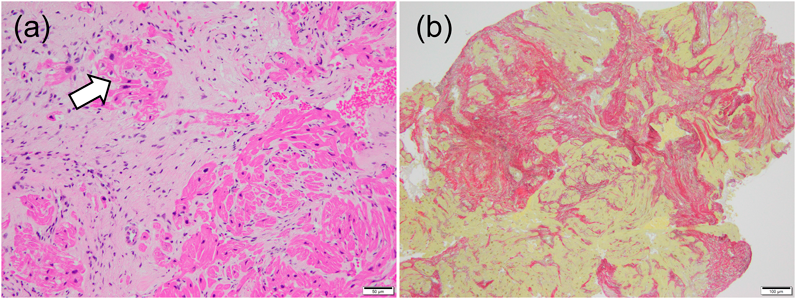
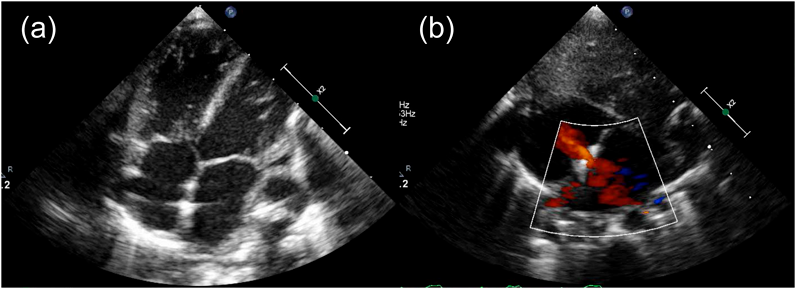
肥大型心筋症を合併した心房中隔欠損症に対して開窓付閉鎖術が奏功した1例Fenestrated Closure of an Atrial Septal Defect for Left Ventricular Diastolic Dysfunction in an Early Infant with Hypertrophic Cardiomyopathy
1 兵庫県立こども病院 循環器内科Departments of Cardiology, Hyogo Prefectural Kobe Children’s Hospital ◇ Hyogo, Japan
2 兵庫県立こども病院 小児集中治療科Pediatric Critical Care Medicine, Hyogo Prefectural Kobe Children’s Hospital ◇ Hyogo, Japan