症例
16歳男性
診断
先天性完全房室ブロック
主訴
特記症状なし
現病歴
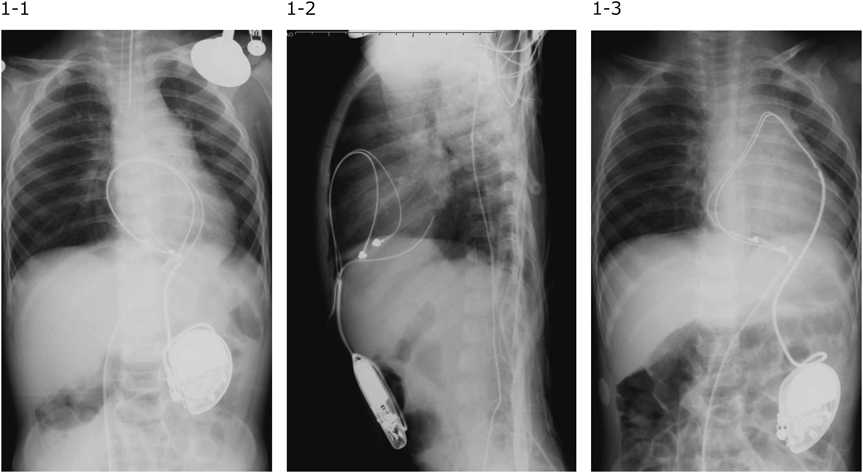
母体抗SS-A/SS-B抗体陽性であり,生後2か月時に徐脈を指摘され先天性完全房室ブロックと診断された.1歳で心外膜リード恒久ペースメーカー植込み術を行われ,心外膜リード(Medtronic 4968)は心前面に撓みを設け留置された(Fig. 1-1, 1-2).挿入翌日の胸部X線正面像ではリードの位置が変化していたが,経過観察された(Fig. 1-3).VVI 65 bpm,学校生活管理区分Dで管理され,患児は無症状であった.9歳時に心エコーにて最大流速2.4 m/秒の肺動脈弁上狭窄を指摘され,リードによる圧迫が疑われた.なお,運動負荷心電図で有意なST変化や胸痛はなく,心筋虚血は否定的と判断された.肺動脈弁上狭窄が最大血流速度3.6 m/秒まで進行したため,心臓カテーテル検査を計画された.
入院時現症
体重50 kg,身長161 cm,血圧113/72 mmHg,心拍数65回/分,SpO2 99%(室内気),心音整,胸骨左縁第2肋間収縮期駆出性雑音Levine 3/6,腹部・四肢に特記すべき所見なし.
血液検査
BNP<5.8 pg/mL, CK 155 IU/L,その他特記事項なし.
胸部X線
心胸郭比46%,うっ血なし,正面像で心外膜リードは心陰影の内側に偏位し,側面像で右室心尖部の電極から心背側に向かってループを形成していた(Fig. 2).
心電図
心拍数65回/分(ペースメーカー調律),完全左脚ブロック,QRS幅0.20秒,QTc 0.47, ST-T変化なし(Fig. 3-1).
運動負荷心電図(Bruceプロトコール)
負荷開始後より接合部調律で心拍上昇,最大負荷stage5(17.1 METS),最高心拍数134回/分,負荷終了後約1分30秒でペースメーカー調律主体となりII, III, aVF誘導で0.2 mVの上行型ST低下及びaVR誘導で0.3 mVの水平型ST上昇あり,同ST変化は回復後期(4~5分)に改善,心室性期外収縮1拍,検査中に胸痛の訴えなし.
心臓超音波検査
左室拡張末期径44 mm,左室壁運動異常なし,僧帽弁輪及び肺動脈弁上において壁外より高輝度構造物による圧排あり,推定右室収縮期圧60 mmHg,肺動脈弁上流速3.5 m/秒,僧帽弁輪流入速度1.5 m/秒.
入院後経過
心外膜リードによる心絞扼を疑い,一般的な血行動態評価・造影に加え冠動脈造影を予定した.室内気で覚醒下に検査を開始した.血行動態評価では,中心静脈圧は平均12 mmHgと高く,右室圧83/18 mmHg,左室圧106/16 mmHgと右室収縮期圧及び両心室拡張末期圧が上昇し,心係数1.9 L/min/m2であった.左室造影に移行するため,5 Frピッグテールカテーテルを左室に挿入し,両上肢を挙上した.この際,心室性期外収縮が散発したが,カテーテル位置の調整でも完全には消失せず,造影準備をしつつ様子を見た.テスト造影を行ったところ,突然患児が気分不良を訴え,直後に意識消失を来した.肢誘導心電図モニターで,接合部調律の高度徐脈から心停止に至った.即座にカテーテルを左室より抜去し,心臓マッサージを開始した.約2分間の心臓マッサージ後の心電図モニターでは,ペースメーカースパイクは確認されるものの心室筋の応答はなく,30~40回/分の接合部調律による自己脈を示した.この時点で患児の意識は回復し,大腿動脈圧は79/47 mmHgであった.約5分間の経静脈的一時右室ペーシングの後,ペースメーカー調律へ復帰し,循環も維持された.直後のペースメーカーチェックでは閾値を含めカテーテル検査前と変化はなかった.なお,意識消失直前の心電図では,左室へのカテーテル挿入後,両上肢を挙上する約5分間に心室性期外収縮が頻発し(Fig. 3-3),その後II, III, aVF誘導の0.4 mVのST低下,aVR誘導の0.3 mVのST上昇が出現(Fig. 3-4),約30秒の間に急速に増悪し,ペーシング不全,徐脈から心停止に至っていた(Fig. 3-5).
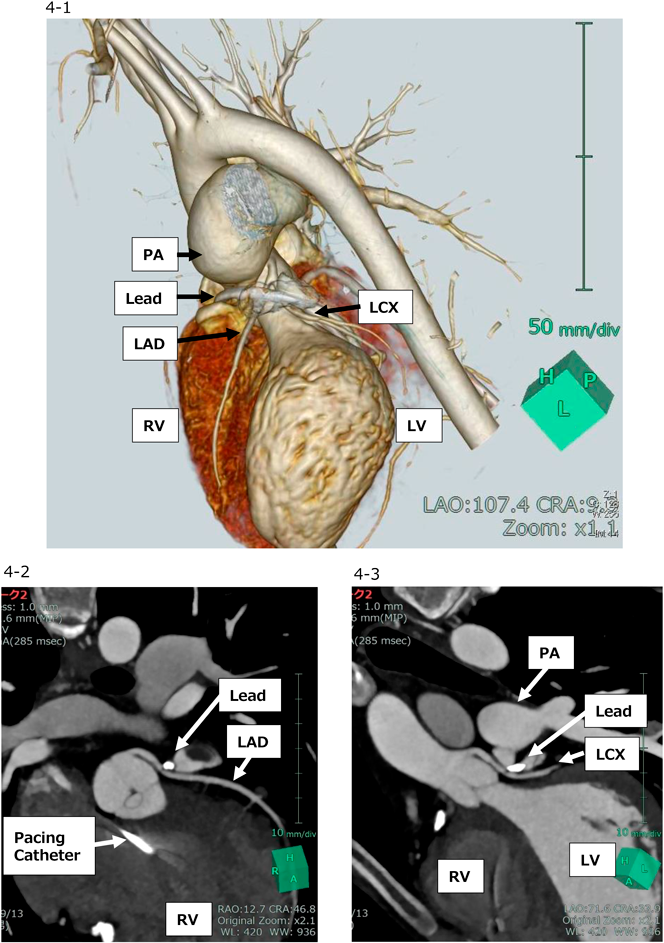
直後に撮像した心臓CTでは,心外膜リードは腹壁から心背側の左房室間溝を上行し,左冠動脈前下行枝及び回旋枝分岐直後の部位と接していた(Fig. 4-1, 4-2, 4-3).上肢挙上や心室性期外収縮によって冠血流が変化し今回のイベントに至ったものと考え,緊急リード抜去術を行う方針とした.
術中所見としては,心外膜リードは房室間溝に沿って食い込み,左冠動脈前下行枝近位部(segment 6)及び左回旋枝近位部(segment 11)や肺動脈幹を圧迫していた.リード硬化及び冠動脈との癒着は強く,人工心肺使用・心停止下に剥離を行い,冠動脈圧排及び肺動脈弁上狭窄の十分な解除が得られた.新たに心外膜リードを右房・右室に縫着し,ペースメーカー設定をDDDへ変更した.
小児期に留置された心外膜リードが成長に伴って引き起こす心絞扼は2020年5月までに25例が報告されている.無症状のまま診断され,早期のリード交換手術により絞扼が解除された8例は全例生存しているのに対し,16例の有症状例においては6例が死亡している(Table 1).6例中突然死は4例あり,うち3例は症状出現後急速にショックに陥っていた2, 4, 6).我々の経験した症例でも検査時の心停止を初発症状とした.無症状であっても心絞扼は突然死リスクであると認識し,症状出現前に治療介入を行うことが重要である.
Table 1 Characteristics of previously reported death cases| Case | Age at diagnosis of CS | Age at PMI | Bradycardia required PMI | Symptom | Site of CS | Treatment | Ref. |
|---|
| 1 | 10 months | Newborn (No detail) | Congenital heart block | Edema CAG→VF | LAD, LCX | Lead removal | 3) |
| 2 | 6 years | 8 months | Surgical AV block | Chest pain Syncope Abdominal discomfort | Posterior aspect of left apex | None | 4) |
| 3 | 7 years | No detail | Congenital heart block | Chest pain after aggressive physical exertion collapse | LCX | None | 1) |
| 4 | 13 years | 1 month | Complete heart block | Sudden death | LAD | None | 2) |
| 5 | 20 years | Infant | Surgical AV block | Syncope | LAD, LCX | PCI | 5) |
| 6 | 29 years | 14 days | Congenital complete heart block | Short of breath Chest pain Malaise | LCA, RCA | None | 6) |
| AV block, atrioventricular block; CAG, coronary angiography; CS, cardiac strangulation; LAD, left anterior descending coronary artery; LCX, left circumflex coronary artery; PCI, percutaneous coronary intervention; PMI, pacemaker implantation; RCA, right coronary artery; VF, ventricular fibrillation |
本症例は,運動負荷心電図検査では心筋虚血が疑われなかったが,心臓カテーテル検査中に虚血を誘因とする重大イベントを生じた.文献上は,労作時胸痛を訴え運動負荷心電図検査で有意なST変化を認めた例がある7).一方,運動負荷試験で異常なしとされ2か月後に急性心筋梗塞を発症した例5)及び運動耐用能に問題なしとされていたにもかかわらず労作後胸痛を訴え突然死した例1)も報告されている.慢性冠動脈疾患診断ガイドライン8)では,運動負荷心電図は冠動脈狭窄の検出感度は70%前後であり,冠危険因子に基づいた判定の重要性が述べられている.さらに,左脚ブロック例におけるST下降は冠動脈疾患の判定基準にならないとされ8),イベント予測が困難な可能性が高い.本症例の運動負荷心電図でのST変化は,上行型で負荷終了後数分の間に改善したため,非特異的と判断していた.しかし,イベント発生時に酷似した心電図変化であり,結果的には冠虚血との関連を否定できない.また,冠動脈造影は運動負荷心電図と相補的に用いられるが,本例のような重大イベント発生を考慮すると,診断はより低侵襲の心臓CTが望ましい.Mahらは,心絞扼における心臓CTの感度を100%と報告している2).
Carrerasらは,胸部X線正面像・側面像で心絞扼を疑う所見として,心房・心室リードが後方にループし,心陰影を囲い込む所見をclassic patternと名付け報告した(感度57%)1).既報例にもペースメーカー留置術後早期にリード変位を生じた例があり10),術後急性期の胸部X線正面像・側面像を慎重に評価する必要がある.本症例の胸部X線は初回手術退院時からclassic patternに合致する所見を呈しており,遅くとも肺動脈弁上狭窄を指摘された9歳時ないし11歳でのジェネレーター交換時には心臓CTを行い,リード交換を行うべきであった.
本症例の心停止は左室へのカテーテル挿入,上肢挙上,頻回心室性期外収縮に続いて突発的に生じた.これら物理的要因のうち,上肢挙上は同姿位でのCT撮像時に症状がないこと及びLAD, LCXとも高度狭窄には至っていないことから要因とは考えにくい.期外収縮頻発後,数分でST変化が生じ心停止に至っており,左室拡張末期容積増大に伴う冠動脈圧排の増強及び心筋虚血が閾値上昇を来したものと推察する.発症時心電図におけるaVR誘導でのST上昇は,左脚ブロックを示す心電図において左主幹部灌流域の虚血や3枝病変を示唆すると報告されており9),広範囲の虚血から急速な経過を辿ったことを裏付けるものであった.