2017年に当院で心臓カテーテル検査・治療を受けた患者のうち,正面および側面像のみを使用した262例に対しTable 1に示した年齢ごとの変換係数にDAPを掛けることで算出された実効線量(effective dose: ED)3, 4)とDAPおよびDAP/BW,月齢との関係についてPearsonの積率相関分析を行った.
Table 1 Conversion formula of dose area product to effective dose and coefficient by age |
|---|
| 0–1w | 1–5w | 5w–6mo | 6mo–2yr | 2–5yr | 5–10yr | 10–15yr | 15–21yr |
|---|
| PA | 0.01151 | 0.01184 | 0.01034 | 0.00465 | 0.00348 | 0.0026 | 0.00162 | 0.00117 |
| Lat | 0.02456 | 0.02476 | 0.02142 | 0.01019 | 0.00708 | 0.00526 | 0.00321 | 0.00214 |
| DAP, dose area product; ED, effective dose; k, coefficient by age |
2008年4月から2019年6月までの15歳未満の小児を対象とし,心房中隔欠損(ASD)閉鎖術(A群)107例,末梢肺動脈へのバルーン血管形成術(BAP; B群)117例,体肺側副血管に対するコイル塞栓術(C群)395例,診断カテーテル(D群)1,918例,カテーテルアブレーション(R群)220例について現在使用しているアンギオ装置を導入した2008から2011年を期間①,カテーテルアブレーションにおける心腔内エコーによるジオメトリー作成や,3D rotational angiography(3DRA)を開始した2012から2016年を期間②,ASDに対し心臓磁気共鳴画像(CMR)によるenface imagingを開始した2017から2019年を期間③とし,撮影装置は全ての期間でAxiom artis dBA(Siemens社)のみを使用した.透視パルスは期間③の前半までは7.5パルス/秒で行っていたが,期間③の後半からは4パルス/秒で行った.撮影フレームは静脈系が7.5~15フレーム/秒,心室や動脈系が15~30フレーム/秒,デバイス留置あるいはバルーン拡張などの治療操作記録7.5フレーム/秒を基本とし,体格や年齢を考慮して術者が決定した.従来の被ばくに関するデータ(照射時間[FT],空気カーマ値[AK],DAP)に加え,DAP/BWについて後方視的に比較検討を行った.A群,B群,C群ではほぼ全例で治療前に診断カテーテルを行っており,被ばくに関するデータは診断カテーテルに要したものも合わせて検討した.患者背景および被ばくに関するデータについては,正規性の検定を行ったのち,連続変数は平均値(±標準偏差)または,中央値[四分位範囲]で表記し,三群間の比較をKruscal–Wallis検定で行い,有意差を認めた際に,Holm法で調整した多重比較を追加で行った.割合の比較はカイ2乗検定で行った.B群については介入病変数,3DRA施行例,主要体肺動脈側副血行(major aortopulmonary collateral artery: MAPCA)症例についても検討し,DAP/BWに影響を与える因子について重回帰分析を行った.D群については,年代ごとの疾患構成と被ばく線量との関係についても検討した.また,両側p値0.05未満を統計学的有意差ありとした.統計解析にはJMP Ver14.0.0を使用した.
本研究は当施設の倫理委員会の承認を得た(倫理委員会承認番号:33).
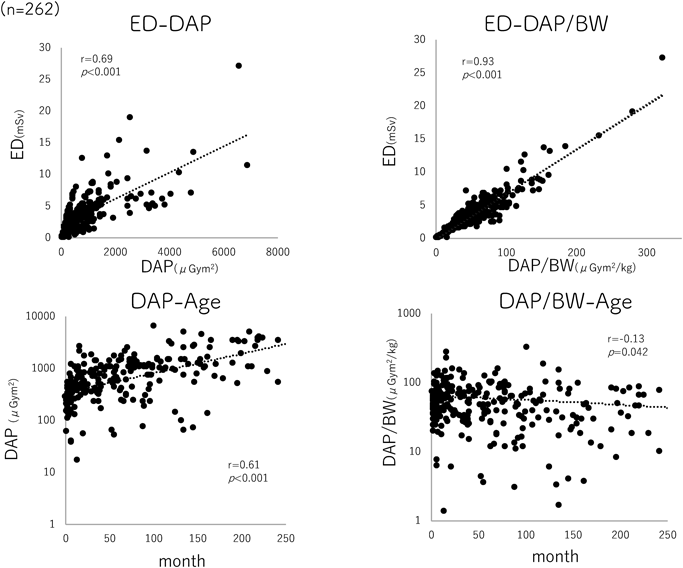
最初に,被ばく線量モニタリングとしてのDAP/BWの有用性の検討として,EDとDAPおよびDAP/BW,月齢との関係をFig. 1に示した.EDはDAP/BWと強い相関関係を示し(r=0.93,p<0.001),DAPは月齢と相関関係にあったが(r=0.61, p<0.001),DAP/BWは月齢との相関はなかった(r=−0.13, p=0.042).
続いて,年代別の心臓カテーテル治療ごとの被ばく線量に関する検討結果を以下に示す.
患者背景
患者背景をTable 2に示した.A群,B群では期間ごとに性別,年齢,体格とも差は認めなかったが,C群,R群は年代ごとに性差を認めた.C群,D群では期間③で年齢が高く,その影響で体重,体表面積も大きかった.また,年代が進むとともにD群の割合が減少しカテーテルインターベンションの割合が増加した.
Table 2 Patients characteristics| Variable | Statistic/Level | Period 1(n=949) | Period 2(n=1,208) | Period 3 (n=600) | p |
|---|
| Group A (n=107) | n | 33(3.5%) | 47(3.9%) | 27(4.5%) | |
| Sex | Male/Female | 23/10 | 33/14 | 15/12 | 0.39 |
| Age(year) | Median [IQR] | 8.7 [5.2–11.3] | 7.3 [6.2–10.0] | 7.5 [5.6–13.0] | 0.89 |
| Body Weight(kg) | Median [IQR] | 24.1 [17.1–36.3] | 22.2 [18.6–29.2] | 23.1 [18.2–35.4] | 0.78 |
| Body Surface Area(m2) | Median [IQR] | 0.93 [0.71–1.24] | 0.84 [0.76–1.06] | 0.91 [0.74–1.29] | 0.70 |
| Group B (n=117) | n | 30(3.2%) | 51(4.2%) | 36(6.0%) | |
| Sex | Male/Female | 11/19 | 27/24 | 16/20 | 0.35 |
| Age(year) | Median [IQR] | 3.7 [1.9–6.1] | 2.9 [1.4–7.4] | 3.6 [2.1–7.0] | 0.85 |
| Body Weight(kg) | Median [IQR] | 12.6 [9.3–18.3] | 11.0 [7.9–19.4] | 10.8 [8.5–17.9] | 0.94 |
| Body Surface Area(m2) | Median [IQR] | 0.56 [0.43–0.77] | 0.51 [0.39–0.78] | 0.50 [0.42–0.77] | 0.98 |
| Group C (n=395) | n | 104(11.0%) | 179(14.8%) | 112(18.7%) | |
| Sex | Male/Female | 53/51 | 67/112 | 39/73 | 0.03‡ |
| Age(year) | Median [IQR] | 1.6 [1.0–2.7] | 1.9 [1.2–3.2] | 1.9 [1.9–7.5] | 0.032† |
| Body Weight(kg) | Median [IQR] | 9.2 [7.7–10.7] | 8.9 [7.2–11.5] | 9.8 [8.2–13.8] | 0.021†‡ |
| Body Surface Area(m2) | Median [IQR] | 0.43 [0.37–0.49] | 0.43 [0.36–0.52] | 0.46 [0.39–0.60] | 0.027†‡ |
| Group D (n=1,918) | n | 723(76.2%) | 836(69.2%) | 359(59.8%) | |
| Sex | Male/Female | 400/323 | 478/358 | 211/148 | 0.53 |
| Age(year) | Median [IQR] | 2.3 [0.6–6.2] | 2.9 [0.6–7.0] | 4.0 [1.3–8.3] | <0.001*†‡ |
| Body Weight(kg) | Median [IQR] | 10.4 [6.4–18.5] | 11.9 [6.7–20.1] | 14.4 [8.6–22.6] | <0.001*†‡ |
| Body Surface Area(m2) | Median [IQR] | 0.47 [0.33–0.75] | 0.53 [0.34–0.79] | 0.61 [0.41–0.89] | <0.001†‡ |
| Group R (n=220) | n | 59(6.2%) | 95(7.9%) | 66(11.0%) | |
| Sex | Male/Female | 35/24 | 37/58 | 35/31 | 0.03* |
| Age(year) | Median [IQR] | 11.2 [5.8–14.4] | 11.9 [7.2–15.6] | 11.8 [7.5–16.8] | 0.27 |
| Body Weight(kg) | Median [IQR] | 31.5 [19.4–47.8] | 35.7 [21.0–49.4] | 38.1 [23.3–52.5] | 0.36 |
| Body Surface Area(m2) | Median [IQR] | 1.12 [0.72–1.44] | 1.22 [0.82–1.44] | 1.29 [0.90–1.53] | 0.34 |
| IQR, interquartile range; Significant difference in multiple comparisons(corrected for the holm method): *, period 1 and 2; †, period 1 and 3; ‡, period 2 and 3 |
手技ごとの被ばくに関するデータの変化
従来の被ばくに関するデータの結果をTable 3, DAP/BWの結果をFig. 2に示した.欠損値は期間①; 5.8%,②; 5.7%,③; 3.5%だった.A群では,FTは年代とともに増加傾向だったが(① vs ②: p=0.021,① vs ③: p<0.001,② vs ③: p=0.0023),AK, DAPは年代ごとに差は認めなかった.一方でDAP/BWは期間③で低く,期間②と③の間に有意差を認めた(② vs ③: p=0.037).B群は全てのパラメーターにおいて期間③で高い傾向にあり,DAP/BWは期間①と②,期間①と③で有意差を認めた(AK:① vs ③: p<0.001, FT:① vs ③: p=0.0025,② vs ③: p=0.0032, DAP:① vs ③: p=0.004, DAP/BW:① vs ②: p=0.014,① vs ③: p<0.001,).年代ごとの変化の詳細については後述する.C群では,AK, FTは期間③で高かったが(AK:① vs ③: p=0.0013,② vs ③: p=0.0025, FT:① vs ②: p=0.0043,① vs ③: p<0.001,② vs ③: p=0.001),DAP, DAP/BWは差を認めなかった.D群は全てのパラメーターで期間③で高い傾向にあり,DAP/BWは期間①と②,①と③の間で有意差を認めた(AK:① vs ②: p<0.001,① vs ③: p<0.001,② vs ③: p<0.001, FT:① vs ②: p<0.001,① vs ③: p<0.001,② vs ③: p=0.001, DAP:① vs ②: p<0.001,① vs ③: p<0.001,② vs ③: p<0.001, DAP/BW:① vs ②: p<0.001,① vs ③: p<0.001).R群では,年代とともに全てのパラメーターが減少傾向で,DAP/BWは有意に減少していた(AK:① vs ②: p=0.0093,① vs ③: p<0.001,② vs ③:p=0.0016, FT:① vs ②: p<0.001,① vs ③: p<0.001,② vs ③: p=0.0015, DAP:① vs ②: p=0.0021,① vs ③: p=0.0039, DAP/BW:① vs ②: p=0.006,① vs ③: p<0.001,② vs ③: p=0.0075).
Table 3 Comparisons of conventional parameters by period in each group| Variable | Statistic/Level | Period 1 | Period 2 | Period 3 | p |
|---|
| Group A | | | | | |
| AK (mGy) | Median [IQR] | 19.5 [10.0–45.3] | 18.0 [14.0–26.0] | 20.0 [14.0–26.0] | 0.72 |
| FT (min) | Median [IQR] | 12.0 [8.6–17.1] | 15.2 [12.3–20.0] | 20.0 [16.7–27.0] | <0.001*†‡ |
| DAP (μGym2) | Median [IQR] | 302 [183–529] | 300 [225–474] | 243 [157–456] | 0.55 |
| Group B | | | | | |
| AK (mGy) | Median [IQR] | 177.5 [118.0–212.0] | 203.0 [133.0–422.0] | 277.5 [169.0–428.0] | 0.0081† |
| FT (min) | Median [IQR] | 39.0 [27.5–54.4] | 43.2 [29.4–51.8] | 51.5 [41.0–72.4] | 0.0025†‡ |
| DAP (μGym2) | Median [IQR] | 967 [685–1275] | 1174 [778–2523] | 1567 [798–2632] | 0.016† |
| Group C | | | | | |
| AK (mGy) | Median [IQR] | 92.0 [68.0–131.8] | 96.0 [66.0–142.0] | 116.5 [79.5–184.8] | 0.0019†‡ |
| FT (min) | Median [IQR] | 34.5 [24.0–46.0] | 40.0 [28.3–53.3] | 48.6 [34.1–68.0] | <0.001*†‡ |
| DAP (μGym2) | Median [IQR] | 596 [384–831] | 554 [375–942] | 672 [461–1078] | 0.068 |
| Group D | | | | | |
| AK (mGy) | Median [IQR] | 63.0 [41.0–95.0] | 75.0 [51.0–125.6] | 102.5 [59.0–178.8] | <0.001*†‡ |
| FT (min) | Median [IQR] | 13.0 [8.5–19.1] | 15.5 [10.8–23.0] | 16.5 [11.1–26.5] | <0.001*†‡ |
| DAP (μGym2) | Median [IQR] | 433 [229–715] | 504 [278–908] | 646 [339–1202] | <0.001*†‡ |
| Group R | | | | | |
| AK (mGy) | Median [IQR] | 203.0 [100.5–335.0] | 102.0 [71.0–153.0] | 65.0 [19.0–136.0] | <0.001*†‡ |
| FT (min) | Median [IQR] | 23.6 [16.2–35.0] | 13.3 [10.3–20.9] | 8.1 [4.4–16.1] | <0.001*†‡ |
| DAP (μGym2) | Median [IQR] | 1856 [792–2901] | 980 [557–1587] | 690 [212–1443] | 0.0065*† |
| AK, air kerma; DAP, dose area product; FT, fluoroscopy time; IQR, interquartile range; Significant difference in multiple comparisons (corrected for the holm method): *, period 1 and 2; †, period 1 and 3; ‡, period 2 and 3 |
B群における年代ごとの変化
次に,B群における病変数と,MAPCA症例,3DRA施行の有無による被ばく線量の変化について述べる.それぞれの年代の特徴をTable 4に示した.1回のセッションで介入する病変数,MAPCAを有する症例の割合は年代とともに増加傾向だった.期間②より開始した3DRAの件数は増加傾向だった.年代ごとの被ばくに関するデータの比較をTable 5に示した.MAPCA症例ではDAPは年代ごとに差は認めなかったが,AK, FTは期間③で高い傾向にあり,(AK:① vs ③: p=0.009,② vs ③: p=0.0068, FT:① vs ③: p=0.0013),DAP/BWは年代とともに有意に増加した(DAP/BW:① vs ③: p<0.001,② vs ③: p=0.017).MAPCAのない例では全てのパラメーターで年代ごとの差はなかった.従来の二方向からの造影(2DA)のみで施行した例では,DAPは年代ごとに差を認めなかったが,AK, FT, DAP/BWは増加傾向だった(AK:① vs ③: p=0.0018, FT:① vs ③: p=0.0071,② vs ③: p=0.0017, DAP/BW:① vs ③: p=0.0042).3DRAを施行した例では有意差を認めなかったものの,DAP/BWは期間③で低下傾向だった.その他のパラメーターは差を認めなかった.期間②,③で2DAと3DRAのDAP/BWの比較をしたところ,それぞれの期間で有意差は認めなかったものの,期間②では3DRAのほうが高かったのに対し,期間③では3DRAのほうが低かった.
Table 4 Detailed characteristics of patients in group B in each period| Variable | Statistic | Period 1 (n=30) | Period 2 (n=51) | Period 3 (n=36) | p |
|---|
| Age(years) | mean[IQR] | 3.6[1.9–6.1] | 2.9[1.4–7.4] | 3.6[2.1–7.0] | 0.85 |
| Lesion number | 1 | 16(53.3%) | 19(37.3%) | 8(22.2%) | 0.033† |
| ≥2 | 14(46.7%) | 32(62.7%) | 28(77.8%) |
| MAPCA | + | 15(50%) | 26(51.0%) | 23(63.9%) | 0.41 |
| − | 15(50%) | 25(49.0%) | 13(36.1%) |
| Angiography | 2DA | 30(100%) | 43(84.3%) | 23(63.9%) | <0.001*†‡ |
| 3DRA | 0(0%) | 8(15.7%) | 13(36.1%) |
| IQR, interquartile range; MAPCA, major aortopulmonary collateral artery; 2DA, two dimensional angiography; 3DRA, three dimensional rotational angiography; Significant difference in multiple comparisons (corrected for the holm method): *, period 1 and 2; †, period 1 and 3; ‡, period 2 and 3 |
Table 5 Comparisons of radiation exposure parameters by period in group B| Variable | Statistic/Level | Period 1 | Period 2 | Period 3 | p |
|---|
| MAPCA+ | | | | | |
| AK (mGy) | Median [IQR] | 181.0 [119.0–212.0] | 187.5 [132.5–282.3] | 293.0 [175.0–480.0] | 0.0069†‡ |
| FT (min) | Median [IQR] | 33.9 [30.5–48.3] | 45.1 [37.8–51.6] | 60.7 [42.2–81.2] | 0.017† |
| DAP (μGym2) | Median [IQR] | 1128 [724–1281] | 1160 [730–2242] | 2051 [873–2827] | 0.062 |
| DAP/BW (μGym2/kg) | Median [IQR] | 75.7 [48.7–101.9] | 100.6 [74.3–126.9] | 128.7 [101.9–201.1] | <0.001†‡ |
| MAPCA− | | | | | |
| AK (mGy) | Median [IQR] | 174.0 [104.0–225.0] | 266.0 [126.0–547.5] | 205.0 [125.5–399.0] | 0.12 |
| FT (min) | Median [IQR] | 41.0 [24.0–60.0] | 34.0 [26.7–54.8] | 46.5 [36.1–62.0] | 0.14 |
| DAP (μGym2) | Median [IQR] | 931 [530–1171] | 1190 [723–2929] | 1477 [551–1764] | 0.095 |
| DAP/BW (μGym2/kg) | Median [IQR] | 93.7 [64.4–106.0] | 131.5 [73.5–215.7] | 94.6 [68.3–143.7] | 0.21 |
| 2DA | | | | | |
| AK (mGy) | Median [IQR] | 177.5 [118.0–212.0] | 184.0 [119.0–401.0] | 303.0 [172.0–569.0] | 0.0013† |
| FT (min) | Median [IQR] | 39.0 [27.5–54.4] | 43.2 [29.5–57.0] | 58.3 [39.5–73.4] | 0.015†‡ |
| DAP (μGym2) | Median [IQR] | 967 [685–1275] | 1125 [671–2105] | 1519 [705–4078] | 0.10 |
| DAP/BW (μGym2/kg) | Median [IQR] | 76.8 [50.5–103.0] | 100.5 [70.6–141.4] | 121.5 [75.9–183.3] | 0.015† |
| 3DRA | | | | | |
| AK (mGy) | Median [IQR] | | 292.5 [209.5–696.5] | 265.0 [163.0–377.0] | 0.28 |
| FT (min) | Median [IQR] | | 38.2 [29.6–51.1] | 47.8 [42.6–66.8] | 0.082 |
| DAP (μGym2) | Median [IQR] | | 1964 [1515–3746] | 1924 [860–2763] | 0.43 |
| DAP/BW (μGym2/kg) | Median [IQR] | | 139.4 [110.8–192.2] | 104.9 [94.5–183.7] | 0.38 |
| AK, air kerma; DAP, dose area product; FT, fluoroscopy time; IQR, interquartile range; MAPCA, major aortopulmonary collateral artery; Significant difference in multiple comparisons (corrected for the holm method): *, period 1 and 2; †, period 1 and 3; ‡, period 2 and 3 |
DAP/BWに影響を与える因子について検討するため,年齢,病変数,MAPCAの有無,3DRA施行の有無について検討した.単変量解析では病変数,3DRA施行の有無で有意差を認めたが(Table 6),重回帰分析ではDAP/BWに影響を与える因子は病変数のみだった(Table 7).
Table 6 Univariate analysis of DAP/BW in group B| Variable | Statistic[n] | DAP/BW(μGym2/kg) | IQR | p |
|---|
| Age(years) | <1 [21] | 86.7 | 70.6–125.9 | 0.30 |
| ≥1 [96] | 104.4 | 71.8–165.3 |
| Lesion number | 1 [43] | 94.3 | 57.6–131.4 | 0.021 |
| ≥2 [74] | 109.3 | 80.2–174.8 |
| MAPCA | + [64] | 103.5 | 75.7–139.6 | 0.96 |
| − [53] | 100.9 | 70.3–164.0 |
| Angiography | 2DA [96] | 97.8 | 69.6–134.6 | 0.044 |
| 3DRA [21] | 120.9 | 98.2–183.7 |
| DAP/BW, dose area product/body weight; IQR, interquartile range; MAPCA, major aortopulmonary collateral artery; 2DA, two dimensional angiography; 3DRA, three dimensional rotational angiography |
Table 7 Multiple regression analysis of DAP/BW in group B| Variable | | B | β | 95% CI | p |
|---|
| Age(years) | | −1.21 | −0.06 | −4.77–2.36 | 0.50 |
| Period | 2 | 8.44 | 0.09 | −9.43–0.09 | 0.35 |
| 3 | 16.42 | 0.17 | −4.65–0.17 | 0.13 |
| Lesion number | | 16.29 | 0.21 | 2.17–30.41 | 0.024 |
| MAPCA | | −6.46 | −0.09 | −20.04–7.11 | 0.35 |
| 3DRA | | 5.85 | 0.06 | −13.14–24.85 | 0.54 |
| B, partial regression coefficient; β, standard partial regression coefficient; CI, confidence interval; MAPCA, major aortopulmonary collateral artery; 3DRA, three dimensional rotational angiography |
D群における疾患構成の変化
D群における年代別の診断名をTable 8に示した.年代とともに,ASDや心室中隔欠損症(VSD)などといった単純な疾患の割合が減少した.DAP/BW(μGym2/kg)についてASD・VSDと,その他の疾患を比較したところ,ASD・VSDは36.2[27.8–47.7]だったのに対し,その他の疾患では45.8[32.7–66.5](p<0.001)だった.
Table 8 Diagnoses of group D in each period| Diagnosis | Period 1 (n=723) | Period 2 (n=836) | Period 3 (n=359) | p |
|---|
| Kawasaki Disease | 30(4.1%) | 60(7.2%) | 44(12.3%) | <0.001*†‡ |
| VSD | 136(18.8%) | 128(15.3%) | 38(10.6%) |
| ASD | 36(5.0%) | 28(3.4%) | 7(2.0%) |
| AVSD | 38(5.3%) | 41(4.9%) | 18(5.0%) |
| TOF | 67(9.3%) | 56(6.7%) | 28(7.8%) |
| PAVSD(MAPCA) | 57(7.9%) | 54(6.5%) | 18(5.0%) |
| Single Ventricle | 158(21.9%) | 221(26.5%) | 95(26.5%) |
| Others | 201(27.9%) | 248(29.7%) | 111(30.9%) |
| ASD, atrial septal defect; AVSD, atrioventricular septal defect; MAPCA, major aortopulmonary collateral artery; PAVSD, pulmonary atresia with ventricular septal defect; TOF, tetralogy of Fallot; VSD, ventricular septal defect; Significant difference in multiple comparisons (corrected for the holm method): *, period 1 and 2; †, period 1 and 3; ‡, period 2 and 3 |
DAP/BWを中心とした被ばく線量モニタリングの有用性
小児は成人と比較し放射線感受性が高く,余命が長いため,成人に比べて放射線被ばくによる影響が大きく,放射線により誘発されるがんは,年齢依存性とされる5).一方で,診断用放射線などの低線量被ばくと小児がんとの関係性は明らかになっていない6).よって,明確なエビデンスが存在しない以上,小児心臓カテーテルに携わる医療者は,As low as reasonably achievable=ALARAの原則に従って,診断や治療の質を向上しつつ,患者被ばくの低減に努めるべきである1).日本先天性心疾患インターベンション学会レジストリーでは,小児心臓カテーテルインターベンションにおける患者被ばくに関する項目としてAK, DAP, FTが登録されている7).AKはX線を照射された空気が,二次電子の運動エネルギーとして,単位質量あたりどれだけのエネルギーを受け取るかに基づいて定義される線量であり,組織吸収線量の近似値として用いられる.心臓カテーテル検査においては,使用するX線装置における患者の皮膚吸収線量を評価するための測定位置として,患者照射基準点であるアイソセンタからX線管焦点方向に15 cm近づいた基準軸上の点における線量を把握することにより,患者の皮膚入射線量を間接的に把握する指標であり,単位はGyを用いる.皮膚入射線量は主に放射線による皮膚障害への影響を評価するために用いられる線量である.DAPは患者の皮膚面において患者が存在しないであろう場合を仮定した空気カーマの照射野内積分で定義される量であり,単位はGy·cm2で表される8).AK, DAPは同様の手技において体格が大きいほど照射面積も大きくなるため,値が大きくなる.対象とする患者の年齢や体格の違いの影響を受けるため,小児において年代ごとや施設間でAK, DAPを比較する場合,解釈には注意を要する.個人の低線量被ばくによる発がんおよび遺伝的影響のリスクを考慮する上では,EDが重要である3).心臓カテーテルにおけるEDは,PCXMC(STUK社)などのモンテカルロシミュレーションを用いたソフトウェアを使用すれば算出可能であるが,Cアームの位置を変えるごとに変化するX線管焦点−受像間面積距離や,受像面の幅と高さなど複数の項目を入力する必要があり9),日常臨床での使用は現実的でない.正面および側面から照射した場合のDAP値よりEDを推定することができると言われており,Table 1に示した年齢ごとの変換係数にDAPを掛けることで算出される3, 4).正面および側面像のみを使用した場合,心臓カテーテルによるEDはそれぞれ算出したEDを足し合わせることで求められる.今回の検討では,正面および側面像のみ照射を行った症例については月齢に依存せず強い相関関係を認めた.KobayashiらはDAP/BWは年齢の影響を受けないため小児心臓カテーテルにおいて最も信頼できる被ばく線量の指標であり,施設内または施設間での比較が可能であると報告した2).実際に欧米では小児心臓カテーテルにおける被ばくの層別化のための評価ツールとしてDAP/BWが使用されており10),DAP/BWによる被ばく線量のモニタリングは簡便かつ有用であると思われる.
手技ごとの被ばく低減の取り組みとその効果
A群,R群では年代とともに被ばく線量は低減した.当院では,ASD症例において,2017年よりCMRによるenface imagingの撮像を行うことでより適切なサイジングバルーンの推定が術前から可能となり11),バルーンサイジング中のシネ撮像を最小限で行えるようになってきた.また,閉塞栓留置後の造影は施行していないため,手技中の被ばくは透視によるものがほとんどで,低パルス透視の効果が得られやすかったと考えられた.一方で,A群では,FTが年代とともに増加していた.これは,若手医師が増加し研修・教育的操作の時間が増加したことなどが原因と推測される.DAP/BWは減少しており,被ばく線量を低減することができたと言える.
R群における被ばく線量の低減に寄与した最も重要な要因として,2012年より心腔内エコーを用いたジオメトリーの作成を開始し,ジオメトリー作成中の透視がほぼ不要となったことが挙げられる.加えて,2019年にはソフトウェアのバージョンアップによりマッピング作成の精度が向上したことが更なる被ばく低減につながったと考えられた.
C群では年代ごとの被ばく線量は大きく変わらなかった.年代ごとに複数の血管や,複雑な走行をした血管に対し塞栓を行う症例が増加したため,FTが増加傾向だった.一方で,ハイドロゲルコイルなど,コイルの塞栓力の向上により効率の良い塞栓が行えるようになったことや12),低パルス透視の使用により被ばく線量の増加を抑制できたと考えられた.
B群とD群では年代とともに被ばく線量が増加傾向を示した.B群では病変数が最も被ばく線量に影響を与えることが示された.当院では,前述のようにパルス透視,撮影フレームを最低限とするほか,複数回,バルーン拡張を行う際は,透視のみを使用し,シネ撮像の回数を減らすなどの工夫を行ってきたが,年代とともに1セッションで介入する病変数が増加したことや,介入する病変や血管の走行が複雑化したことによりアプローチが困難な症例が増加し,透視時間や造影の回数が増加したことで被ばく線量が増加したと考えられた.3DRAは2DAと比較し広角的,立体的な画像構築により,より客観的な診断,評価に寄与する可能性があり,我々は2013年から3DRAを用いたBAPを開始し2015年にその有用性を報告した13).その後の症例の積み重ねにより,近年では2DAよりも被ばく線量は低下傾向となった.今後,3DRAの活用により更なる被ばく低減効果が期待される.
D群では心臓超音波やCMRの進歩により年代とともにASDやVSDなどの心内構造が単純な疾患における診断カテーテルが減少したため,相対的に被ばく線量が増加したと考えられた.診断カテーテルでは手技時間がインターベンションよりも短く,透視よりも造影時のシネ撮像による被ばくの影響が大きいため,低パルス透視の効果が得られにくかったことも要因の一つと考えられた.
被ばく低減における課題と今後の展望
当院では,1. 患者を適切な位置に配置すること(Flat Panel Detector(FPD)を近づける,X線管から被写体を離すなど),2. 診断や治療に不要な造影を避けること,3. 付加フィルターの使用,4. 照射野を絞ること,5. 低パルス透視(4パルス/秒)を積極的に行うことで小児心臓カテーテルにおける被ばく低減に努めてきた.また,他のモダリティの発展により診断カテーテルの省略や,透視,造影の使用を減少させることができた.一方で複雑な心内構造や血管病変を持つ症例が増加傾向であり,特にB群では被ばく低減の効果を得ることができなかった.Fig. 2に示した通り,期間③において,B群のDAP/BWは他の群より高く,A群の約12倍,C群の約1.6倍,D群の約2.5倍,R群の約5.7倍に上る.加えて,B群においては心臓カテーテル以外にも造影CT,シンチグラフィーなどの被ばくを伴う検査を術前,術後に複数回行う症例もあり,心臓カテーテルにおける被ばく低減の努力はB群を中心に今後も更に必要となる.次世代の撮像装置ではCアームのFPDに新素材のクリスタルシリコンを採用し,X線量に応じたノイズ低減処理が改良されるなど,被ばく低減技術が進歩し14),小児心臓カテーテルにおいても被ばく低減効果が得られている15).また,術前に撮像した他のモダリティの画像をフュージョンできるものも多い.Gorecznyらは経皮的肺動脈弁留置術において,3DRAのフュージョンイメージングにより従来の2DAより被ばくの低減効果を認めたと報告しており16),ソフトウェアや撮像装置の更新は重要である.しかしながら,それらは多額の費用がかかるため,現在使用中の撮像装置で実行可能な,グリッドを使用しないことや17),術者への意識づけ18),被ばく低減のためのプロトコールを作成するなどの努力を行うことは重要であり,実際に被ばく低減の効果が得られることが報告されている19, 20).
研究の限界
本研究では手技を行った術者の違いは考慮に入れていない.当院では,全ての年代で基本的に専攻医(または後期研修医)と指導医がペアとなり,専攻医が熟練度に合わせて指導医の指導のもと,カテーテル操作を行ってきた.
コイル塞栓においてはコイルの種類や数などについては検討していない.