川崎病冠動脈病変後遺症の遠隔期において血管内膜病変が存在し,その評価にblack blood(BB)法を用いたmagnetic resonance(MR)coronary vessel wall imagingが有用であると言われている1–3).しかし,BB法で血管壁肥厚を指摘された病変に対し,光干渉断層法(optical coherence tomography: OCT)で内膜病変の詳細な評価を行った報告はない.我々は川崎病冠動脈瘤合併症例4例の冠動脈の血管壁をBB法とOCTで評価し,比較検討を行った.
画像検査の撮像方法
Magnetic resonance imaging(MRI)装置はPhillips社製Intera 1.5T Achievaを使用し,MR coronary angiography(MRCA)とBB法を用いたMR coronary vessel wall imagingを撮像した.BB法の撮像方法はT1 BB Turbo field echo(TFE)に脂肪抑制(spectral presaturation with inversion recovery: SPIR法)を併用し,収集法はspiral sequenceを使用できないため,low high法を使用した.OCTはST. JUDE MEDICAL社製ILUMIEN OCT Imaging Systemを使用し,6Frシースを挿入し,ガイディングカテーテルは同社製Dragonfly JP Imaging Catheterを使用した.
症例1
症例
11歳男性
現病歴
6歳時に川崎病を発症し初回治療のガンマグロブリン大量療法(IVIg)2 g/kgに反応なく,IVIg 1 g/kgの追加投与を行った.発症1か月後に施行したMRCAで右冠動脈segment 2に最大径4.5 mmの冠動脈瘤を認めた.7歳時,9歳時に施行したMRCAでは冠動脈瘤は不変だった.
画像検査所見
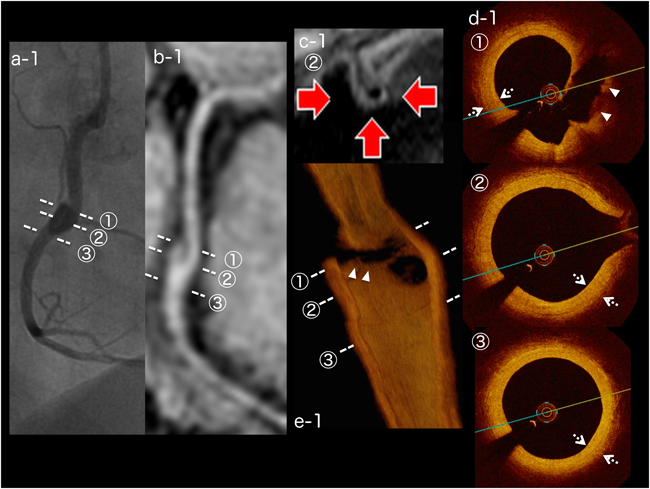
11歳時に施行したMRCAでsegment 2の瘤内に隔壁様の構造物を認め,BB法では瘤部に全周性の血管壁肥厚を認めた.OCTでは全周性に内膜の線維性肥厚を認めた.石灰化や血栓は認めなかった.MRCAで認めた隔壁様構造物の部分には内膜の剥離を認めた(Fig. 1).
症例2
症例
8歳男性
現病歴
生後3か月時に川崎病を発症し,初回治療のIVIg 2 g/kgに反応なく,追加治療でIVIg 2 g/kg×2回,methylprednisolone pulse療法,ulinastatin投与を行った.右冠動脈segment 2に最大径5.6 mm,左冠動脈前下行枝segment 6に最大径5.6 mmの冠動脈瘤が残存した.その後segment 6の瘤は退縮した.3歳時に施行した冠動脈造影(coronary angiography: CAG)でsegment 2の瘤入口部に28%狭窄を認めた.8歳時に労作時胸痛を認め,運動負荷心電図で一過性にII,III,aVfのST低下を認めた.
画像検査所見
8歳時に施行したMRCAでsegment 2に最大径5.1 mmの冠動脈瘤を認め,入口部は2.2 mmと狭小化していた.BB法ではsegment 2の近位部から遠位部にかけて全周性に血管壁の肥厚を認めた.CAGでsegment 2の瘤入口部に40%狭窄を認め,OCTでは瘤全体に内膜の線維性肥厚を認めた.瘤の中央には一部,脂質に富んだ内膜が存在し,遠位部には半周性に内膜の石灰化を認めた.冠血流予備量比(fractional flow reserve: FFR)は0.84であり,インターベンションは行わなかった(Fig. 2).
症例3
症例
17歳女性
現病歴
5歳時に川崎病を発症し初回治療でIVIg 2 g/kgの投与を行った.発症2か月後に施行したCAGで左前下行枝segment 6に最大径5.3 mm,segment 7に最大径3.0 mmの冠動脈瘤を認めた.9歳時に施行したCAGでsegment 6に最大径6.2 mmの冠動脈瘤と瘤入口部に25%狭窄を認め,segment 7の瘤は退縮していた.その後MRCAで経過観察し,病変の変化はなかった.
画像検査所見
17歳時に施行したMRCAでsegment 6の瘤だった部分が狭窄し内腔不整となっており,BB法では全周性に血管壁の肥厚を認めた.CAGではsegment 6に50%狭窄を認め,OCTではsegment 6の狭窄部に内膜の線維性肥厚を認め,石灰化や中膜の剥離を伴っていた.狭窄部より近位側にも内膜の線維性肥厚と新生血管を認めた.FFRは0.85~0.94であり,インターベンションは施行しなかった.
症例4
症例
21歳女性
現病歴
1歳時に川崎病を発症し初回治療のIVIg 200 mg/kg×5日の投与に反応なく,追加治療でIVIg 500 mg/kg×3日の投与を行った.右冠動脈segment 1,左冠動脈主幹部segment 5,前下行枝segment 6に冠動脈瘤を形成した.発症3か月後に施行したCAGでsegment 5に冠動脈瘤を認め,segment 1,6の瘤退縮を認めた.15歳時に施行したMRCAでsegment 5に最大径4 mmの拡張を認め,BB法で血管壁の肥厚を認めた.
画像検査所見
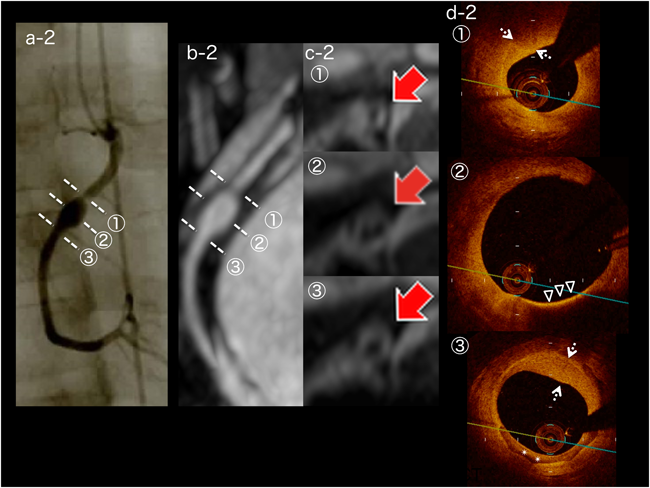
21歳時に施行したCAGで右冠動脈,左冠動脈ともに瘤や狭窄はなかった.OCTではsegment 1,segment 5,segment 6に内膜の線維性肥厚を認め,segment 6に内膜の血管新生を豊富に認めた(Fig. 3).CAG上退縮した瘤やその周囲ではOCTで内膜肥厚を認めたが,急性期に正常だった冠動脈にはOCTを施行した範囲で,内膜肥厚は認めなかった.一方,BB法では解像度が低いため血管壁は均一に描出され,性状の評価はできなかった.
川崎病に対する急性期治療の進歩により,冠動脈後遺症の発生頻度は2.6%と減少傾向であるが,新規患者数は増加傾向で冠動脈後遺症のある患者数は2013年~2014年の2年間で887人と2007年から横ばいである4).Tsudaらは発症100日以内の初回CAGで冠動脈瘤の径が4 mm以上だと,血管内超音波(intravascular ultrasound: IVUS)で内膜肥厚が認められたと報告している5).また,6 mm以上だとリモデリングが強くなり,遠隔期に狭窄病変や石灰化を起こすとも報告している6).冠動脈後遺症の経過観察において,血管内膜の評価は重要である.近年,dual source computed tomography(DSCT)やBB法を用いた内膜評価の報告が散見される1–3, 7).
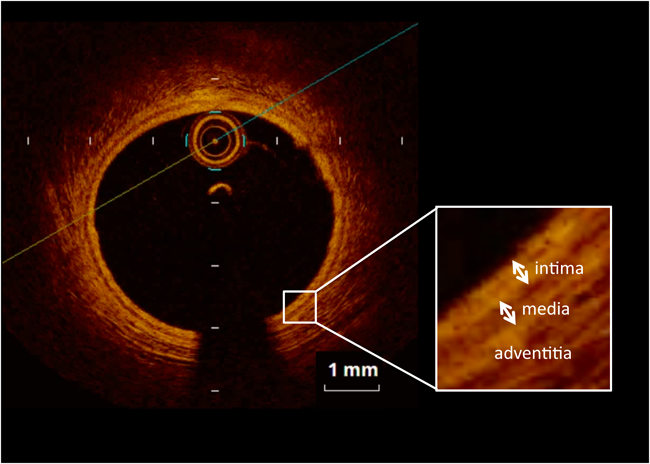
BB法は血流を無信号にし,プラークや内膜を描出する撮像法で,脂肪抑制を併用することで内膜肥厚の検討が可能と言われている2).OCTはカテーテルベースの冠動脈内画像診断法で近赤外線光の干渉により組織を画像化するため,軸解像度が約15 nmと極めて高く,正常な冠動脈は三層構造として描出され,プラークや血栓の性状評価,組織診断に有用である8)(Fig. 4).当院では2009年からMRCAとBB法を用いたMR vessel wall imagingを併用し,冠動脈後遺症における血管壁肥厚の観察を行っている.今回,BB法で壁肥厚を指摘された部位の内膜病変評価のためにOCTを行った.
患者のまとめをTable 1に示した.4症例,4か所の病変でBB法を撮像し,すべての病変に血管壁肥厚を認め,OCTでも内膜肥厚を認めた.内膜の多くは石灰化や,線維性肥厚などの川崎病遠隔期に認められる病変9)だったが,症例2では瘤の内膜に脂質に富んだ病変を認めた.成人冠動脈の粥状硬化病変はマクロファージの集簇により同様の画像を示す8).Dionneらは川崎病冠動脈瘤を有する小児18例に対し,川崎病罹患後平均9年後にOCTを施行し,8例に内膜へマクロファージの浸潤を認めたと報告した10).Suzukiらは小児死亡例の病理所見で,川崎病冠動脈病変にマクロファージの浸潤はなかったと報告しており11),長期経過の冠動脈病変における病態解明が期待される.
Table 1 Summary of four cases| Case | Sex | Age (years) | Age at KD diagnosis years) | Initial therapy | Additional therapy | CAG | MRI (BB) | OCT |
|---|
| Lesions | Wall thickness (mm) | Intima thickness (mm) | Findings |
|---|
| 1 | M | 11 | 6 | IVIg | IVIg | RCA | #1 | N | N/A | 0.14–0.26 | N |
| 2 g/kg | 1 g/kg | | #2 | AN | 2.20–2.79 | 0.24–0.67 | IH, Fib, SI |
| | LCA | | N | N/A | N/A | N/A |
| 2 | M | 8 | 0 | IVIg | IVIg | RCA | #1 | N | N/A | 0.41–0.52 | IH, Fib, NV |
| 2 g/kg | 2 g/kg*2, mPSL | | #2 | AN, LS | 2.74–6.47 | 0.18–0.75 | IH, Fib, Cal, LI, NV |
| pulse, UTI | LCA | #6 | RA | N/A | N/A | N/A |
| 3 | F | 17 | 5 | IVIg | none | RCA | | N | N/A | N/A | N/A |
| 2 g/kg | | LCA | #5 | N | N/A | 0.23–0.38 | IH, Fib |
| | | #6 | LS | 2.72–6.74 | 0.52–1.71 | IH, Fib, SM, Cal, NV |
| | | #7 | RA | N/A | 0.19–1.05 | IH, Fib, Cal |
| | | #11 | N | N/A | 0.16–0.23 | N |
| 4 | F | 21 | 1 | IVIg | IVIg | RCA | #1 | RA | N/A | 0.47–0.55 | IH, Fib |
| 200 mg/kg | 500 mg/kg | | #2 | N | N/A | 0.07–0.10 | N |
| *5 day | *3 day | LCA | #5 | AN | 2.44 | 0.57–0.66 | IH, Fib |
| | | #6 | RA | N/A | 0.46–0.58 | IH, Fib, NV |
| | | #9 | N | N/A | 0.11–0.19 | N |
| Vessel wall thickness of coronary artery lesions on black-blood magnetic resonance imaging was measured using the half-width of the signal level. M; male, F; female, KD; Kawasaki disease, IVIg; intravenous immunoglobulin, mPSL; methylpredonisolone, UTI; ulinastatin, RCA; right coronary artery, LCA; left coronary artery, CAG; coronary angiography, MRI; magnetic resonance imaging, BB; black blood method, OCT; optical coherence tomography, AN; aneurysm, N; normal coronary artery, LS; localized stenosis, RA; regressed aneurysm, N/A; not available, IH; intimal hyperplasia, Fib; fibrosis, SI; separation of the intima, Cal; calcification, LI; lipidOladen intima, NV; neovascularization, SM; separation of the media. |
BB法の最大信号の半分の範囲(半値幅)で測定した血管壁肥厚とOCTでの内膜肥厚を比較したところ,BB法の血管壁肥厚は2.20~6.74 mm,OCTの内膜肥厚は0.18~1.71 mmとかなりの差があった.GreilらはBB法を用いて川崎病冠動脈瘤の血管壁肥厚を測定し,平均2.5±0.5 mmであったと報告しており12),当院の検討とほぼ同等であった.一方,DionneらはOCTにおける冠動脈瘤の内膜肥厚は右冠動脈で平均347.1±173.4 µm,左前下行枝で435.0±158.1 µm,左回旋枝で360.0±165.5 µmであったと報告している10).このように,過去の報告の比較でもBB法での血管壁肥厚とOCTでの内膜肥厚に差があった.BB法で血管壁が厚く見える原因は体動,心拍の影響やスライス厚が5 mmと厚いことが原因と言われている2).さらに,BB法で評価した血管壁肥厚は内膜だけでなく,内膜を含めた血管壁全体,または血管壁と血管周囲組織の変化を合わせて評価している可能性があり,今後の検討が必要である.
BB法の問題点の一つ目は前述のごとく,解像度が低い点である.二つ目は,当院で用いたBB法では血管の全長を描出できず,撮像部位以外の内膜肥厚の存在が否定できないことである.鈴木らは1回の撮像で冠動脈全長の3D画像を作成可能なvolume isotropic turbo-spin-echo acquisition(VISTA)-BB法の有用性を報告している3).一方,OCTにおける問題点の一つ目は患者への侵襲が大きいことである.デバイスを使用するのに最低でも6Frのシースが必要で,体格の小さい小児には出血や動脈閉塞のリスクが高くなる.また画像を得るには,病変に直接デバイスを挿入し,赤血球を排除するために,血管内を透明な液体で置換する必要がある.二つ目は光の浸達度が1~2 mmと浅く8),大きな冠動脈瘤では血管壁の全周を評価できないことである.
本検討によりBB法で血管壁肥厚が存在する部位にはOCTで内膜肥厚が存在することが示された.近年,経過観察目的のCAGは侵襲が大きいため減少傾向にあり13),OCTも侵襲が大きいため施行頻度は少ない.本検討では正常冠動脈壁でBB法とOCTの比較を行えなかったが,北爪らは14歳未満の冠動脈において,BB法で瘤の退縮部位は47.4%で血管壁が描出され,正常冠動脈壁は1か所も描出されなかったと報告している14).BB法を併用したMRCAは,非侵襲的に血管内腔と血管壁を評価できるため内膜肥厚のスクリーニングに有用であると思われる.しかし現状では,BB法の解像度が低いため,内膜肥厚の定量やプラーク性状の評価は困難である.そのためインターベンションの適応が考慮される場合はIVUS,OCTによる内膜病変の詳細な観察が必要となる13).今後,MR装置の高速化,3T装置による高解像度化,3D収集による冠動脈全長の評価など,MRCAの更なる進歩で,川崎病冠動脈後遺症の経過観察における患者の負担軽減が期待される.
引用文献References
1) Suzuki A, Takemura A, Inaba R, et al: Magnetic resonance coronary angiography to evaluate coronary arterial lesions in patient with Kawasaki disease. Cardiol Young 2006; 16: 563–571
2) 武村 濃,鈴木淳子,稲葉利佳子,ほか:川崎病冠動脈障害に対するMR coronary vessel wall imagingの検討.Prog Med 2005; 25: 1833–1836
3) 鈴木淳子,林 慈明,飯山利健,ほか:MRIによる川崎病冠動脈障害の経過観察—特に瘤内血栓の経過—.Prog Med 2014; 34: 1250–1256
4) 第23回川崎病全国調査成績,2015年9月,http://www.jichi.ac.jp/dph/kawasakibyou/20150924/mcls23report1013.pdf
5) Tsuda E, Kamiya T, Kimura K, et al: Coronary artery dilatation exceeding 4.0 mm during acute Kawasaki disease predicts a high probability of subsequent late intima-medial thickening. Pediatr Cardiol 2002; 23: 9–14
6) Tsuda E, Kamiya T, Ono Y, et al: Incidence of stenotic lesions predicted by acute phase changes in coronary arterial diameter during Kawasaki disease. Pediatr Cardiol 2005; 26: 73–79
7) 辻井信之,津田悦子,神崎 歩,ほか:川崎病冠動脈障害におけるDual-Source Computed Tomography(DSCT)の有用性.Prog Med 2015; 35: 1187–1192
8) 高野雅充:OCTによってなにがみえるか.Heart View 2011; 15: 635–643
9) 横内 幸,大原関利章,勝碕譲児,ほか:川崎病冠動脈病変の病理.日本臨床2014; 72: 1518–1521
10) Dionne A, Ibrahim R, Gebhard C, et al: Coronary wall structural change in patients with Kawasaki disease: New insight from optical coherence tomography (OCT). J Am Heart Assoc 2015; 4: e001939
11) Suzuki A, Miyagawa-Tomita S, Komatsu K, et al: Active remodeling of the coronary arterial lesions in late phase of Kawasaki disease immunohistochemical study. Circulation 2000; 101: 2935–2941
12) Greil GF, Seeger A, Miller S, et al: Coronary magnetic resonance angiography and vessel wall imaging in children with Kawasaki disease. Pediatr Radiol 2007; 37: 666–673
13) 日本循環器学会学術委員会合同研究班:川崎病心臓血管後遺症の診断と治療に関するガイドライン(2013年改訂版),http://www.j-circ.or.jp/guideline/pdf/JCS2013_ogawas_h.pdf
14) 北爪 勉,鈴木淳子,武村 濃,ほか:MRIによる川崎病の冠動脈壁肥厚の検討.日小児循環器会誌2011; 27: 35–42