A群β溶血性連鎖球菌(Group A Streptococcus, GAS)の早期診断と抗菌薬の普及によって,本邦において小児科医が急性リウマチ熱(Acute Rheumatic Fever, ARF)の診療に関わることはまれとなった.日本小児循環器学会の希少疾患調査における2005年から2016年の集計では,年間登録数は5~10例に留まっている1).世界的にみても,ARFによる死亡は1995年から2015年にかけて半減した2).死亡率の改善は抗生剤内服による再発予防と,弁膜症に対する心不全治療や弁置換術の進歩によるところが大きく,従来からリウマチ熱の心炎に対して施行されているアスピリン(ASA)や副腎皮質ステロイドによる抗炎症療法は,前方視的検討において有効なエビデンスを確認されていない3, 4).重度の弁逆流に至った例では弁置換が必要となるため,早期診断による再発,重症化予防が患者の予後改善のために重要である.
2015年に改訂Jones Criteria 2015が全米心臓病協会(AHA)から呈示された(Table 1).同診断基準では,地域ごとの罹患率によって診断基準が調整された他,CRP・赤血球沈降速度(ESR)の基準値の明確化,心エコーを用いた心臓弁膜症診断が盛り込まれた(Table 2).また,疑診断時に抗菌薬の予防内服を導入すること,繰り返し心エコー検査を実施することの重要性も明記された5).
Table 1 Revised Jones Criteria 2015 AHA Scientific Statement5)| For all patient populations with evidence of preceding GAS infection | |
| Diagnosis: initial ARF | 2 major manifestations or 1 major plus 2 minor |
| Diagnosis: recurrent ARF | 2 major or 1 major and 2 minor or 3 minor |
| 〈Major criteria〉 | |
| Low-risk populations | Moderate-and high-risk populations |
| Carditis (clinical and/or subclinical) | Carditis (Clinical and/or subclinical) |
| Arthritis (polyarthritis only) | Arthritis (mono- or polyarthritis include polyarthralgia) |
| Chorea | Chorea |
| Erythema marginatum | Erythema marginatum |
| Subcutaneous nodules | Subcutaneous nodules |
| 〈Minor Criteria〉 | |
| Low-risk populations | Moderate-and high-risk populations |
| Polyarthralgia | Monoarthralgia |
| Fever (≧38.5°C) | Fever (≧38.0°C) |
| ESR≧60 mm/1h and/or CRP≧3.0 mg/dL | ESR≧30 mm/1h and/or CRP≧3.0 mg/dL |
| Prolonged PR interval (unless carditis is a major criterion) | Prolonged PR interval (unless carditis is a major criterion) |
| Low-risk populations : ARF incidence ≤2 per 100 000 school-aged children or all-age rheumatic heart disease prevalence of ≤1 per 1000 population per year. |
Table 2 Doppler and morphological findings on echocardiogram in rheumatic heart disease (RHD)| Doppler Findings (regurgitation, all 4 met) | Morphological Findings |
|---|
| Mitral | Mitral (acute) | Mitral (chronic) |
| Seen in at least 2 views | Annular dilation | Leaflet thickning |
| Jet length≧2 cm in at least 1 view | Chordal elongation | Choral thickening and fusion |
| Peak velocity>3 m/s | Chordal rapture resulting in flail leaflet with severe mitral regurgitation | Restricted leaflet motion |
| Pansystolic jet in at least 1 envelope | Anterior (or less commonly posterior) leaflet tip prolapse | Calcification |
| Beading/nodularity of leaflet tips | |
| Aortic | Aortic (either acute or chronic) | |
| Seen in at least 2 views | Irregular or focal leaflet thickening | |
| Jet length≧1 cm in at least 1 view | Coaptation defect | |
| Peek velocity>3 m/s | Restricted leaflet motion | |
| Pan diastolic jet in at least 1 envelope | Leaflet prolapse | |
| On occasion, particularly early in the course of acute rheumatic fever, mitral or aortic valve morphology may be normal on echocardiogram while doppler shows regurgitation. |
本稿では著者らが経験したARF 6例の臨床経過と予後について診断契機,症状,治療内容,経過と予後をまとめ,特に弁膜炎の臨床経過,管理と予後について後方視的に検討した.
Table 3 Characteristics, course, prognosis of patients| Case | Age | Sex | Symptoms at onset | Department of first visit | Duration from onset to RF diagnosis | Clues to diagnosis | Jones Diagnostic Criteria | Valve disease | ECG | Treatment | Follow-up period | Prognosis |
|---|
| Major Criteria | Minor Criteria | Antibiotics | Anti-inflammation | Anti-heart failure |
|---|
| 1 | 3 | f | short breath fatigability | Pediatrics | 3d | heart murmur | carditis | fever ESR, CRP | AR moderate MR severe | LVH SVPC | CTX→AMPC | PSL ASA | Diuretics PDE3-I ACEI | 8y | alive AR mild MR trivial |
| 2 | 5 | f | fever arthralgia joint swelling | Orthopedics | 13d | heart murmur | carditis poly-arthritis | fever poly-arthralgia ESR, CRP | AR moderate | LVH | PCG | PSL | ACEI | 15y | alive AR moderate AVR 13y after onset |
| 3 | 8 | m | fever arthralgia joint swelling | Pediatrics | 35d | migratory arthritis heart murmur | carditis poly-arthritis | fever poly-arthralgia ESR, CRP | MR moderate | w.n.l | AMPC | PSL | ACEI | 1y | alive MR trivial |
| 4 | 9 | f | fever arthralgia joint swelling | Orthopedics | 4y10m | migratory arthritis heart murmur | carditis poly-arthritis | fever poly-arthralgia ESR, CRP | AR severe | LVH | ABPC | PSL | Diuretics ACEI | 14y | alive AR severe AVR 2y after onset |
| 5 | 9 | m | fever arthralgia joint swelling | Pediatrics | 3d | migratory arthritis ECG changes | carditis poly-arthritis | fever poly-arthralgia ESR, CRP PQ prolongation | AR trivial | advanced AVB | ABPC | PSL ASA | — | 10y | alive free from treatment |
| 6 | 13 | m | arthralgia joint swelling | Osteopathic clinic | 10d | fever migratory arthritis heart murmur | carditis poly-arthritis | fever poly-arthralgia ESR, CRP | AR trivial MR moderate | LVH | ABPC/SBT→PCG | ASA | ACEI | 8y | alive AR mild MR trivial |
| ABPC, ampicillin; ABPC/SBT, ampicillin/sulbactam; ACEI, angiotensin-converting-enzyme inhibitor; AMPC, amoxicillin; AR, aortic regurgitation; ASA, acetylsalicylic acid; AVB, atrioventricular block; AVR, aortic valve replacement; CTX, cefotaxime; ESR, CRP, erythrocyte sedimentation rate ≧60 mm/1h and/or and/or C-reactive protein level ≧3.0 mg/dL; LVH, left ventricular hypertrophy; MR, mitral regurgitation; PCG, benzylpenicillin; PDE3-I, phosphodiesterase 3 inhibitor; PSL, prednisolone; SVPC, supraventricular premature contraction |
診断時年齢は3~13歳(中央値8.5歳)で男女ともに3例であった.追跡期間は1~15年(中央値9年)であった.
初診時の主訴,診断の契機
初診時の主訴は4例で発熱および関節炎,1例が関節炎のみ,他の1例(症例5)では関節症状がなく,歩行時のふらつき,易疲労性,息切れで,心不全の関与が疑われた.歩行時のふらつきは舞踏病ではなく心不全による歩行困難であった.整形外科等,小児科以外を初診した症例が含まれ,初診からARFの診断に至るまでの期間は3日~4年10か月(中央値11.5日)であった.5例ではARFを疑われるきっかけが心雑音,弁膜症であった.他の1例は心電図異常であった.初診医療機関が小児科以外であった症例で,診断が遅くなる傾向が認められた.
〈溶連菌感染〉
溶連菌の感染が証明できたのは6例中5例であった.迅速抗原検査で診断されたものが2例(症例3, 4),血清学的検査でASO/ASKの上昇を指摘されたものが2例(症例5, 6)あり,残りの1例(症例1)は迅速抗原検査,ASO, ASK,咽頭培養検査すべてで陽性所見が認められた.症例2は溶連菌感染が証明できなかったが,心炎と移動性多関節炎の既往があり,Jones診断基準の大項目2つと小項目2つ,さらに感染性心内膜炎の否定をもって臨床的にARFと診断した.
〈大項目〉
①心炎
6例中5例でRFと診断されたときすでに弁膜炎が進行していた.大動脈弁閉鎖不全(aortic regurgitation, AR)が5例,そのうち2例は僧帽弁閉鎖不全(mitral regurgitation, MR)を合併し,MR単独が1例であった.心電図異常は2例に認められ,高度房室ブロック,上室期外収縮が各1例であった.
②関節炎
経過中に6例中5例で関節炎が出現した.鎮痛薬投与に反応し,1週間程度で関節痛と腫脹は消退するが,他の部位に新たに出現するという移動性関節炎であった.ARFの治療開始後1か月以上関節所見が持続した症例はなかった.
③皮膚症状
輪状紅斑,皮下結節いずれも認められなかった.症例2で単純性紅斑が認められた.
④精神症状・舞踏病
いずれも認められなかった.
〈小項目〉
①発熱
全例で経過中に改訂Jones Criteria 2015の基準を満たす38.5度以上の発熱が認められた.
②多発関節痛
症例1以外全例で関節痛が認められた.表には記載があるが,いずれも移動性多発関節炎を大症状としてとっているため,多発関節痛は診断基準としてカウントしていない.
③ESR,CRP
全例診断基準を満たす炎症マーカーの上昇が認められた.
④心電図異常(PQの延長)
症例5はPQ延長から高度房室ブロックに至ったが,治療後速やかに改善した.
治療
ステロイド:6例中5例でプレドニゾロン(PSL)が投与された.診断時心不全症状が明らかであった3例(症例1, 2, 4)と最近の症例3では最大量(2 mg/kg/day,最大60 mg/day)を投与された.
アスピリン(ASA):治療開始時に関節症状が認められた2例と,心不全症状が強かった症例1の計3例でASAが投与された.症例3は先行のPSL投与で関節症状が消失したためASAは投与されなかった.
経過と予後
全例抗菌薬の予防内服を導入した.抗炎症療法漸減中の症状の再燃も,経過観察期間中のリウマチ熱の再発もなかった.死亡例もなかった.
〈関節症状〉
抗炎症療法開始時に関節炎が存在した症例は,全例で治療後速やかに軽快し,治療開始後72時間以上経過しても関節症状が残存した症例はなかった.MRI所見やMMP-3値から関節破壊が示唆された例もなかった.
〈弁膜炎〉
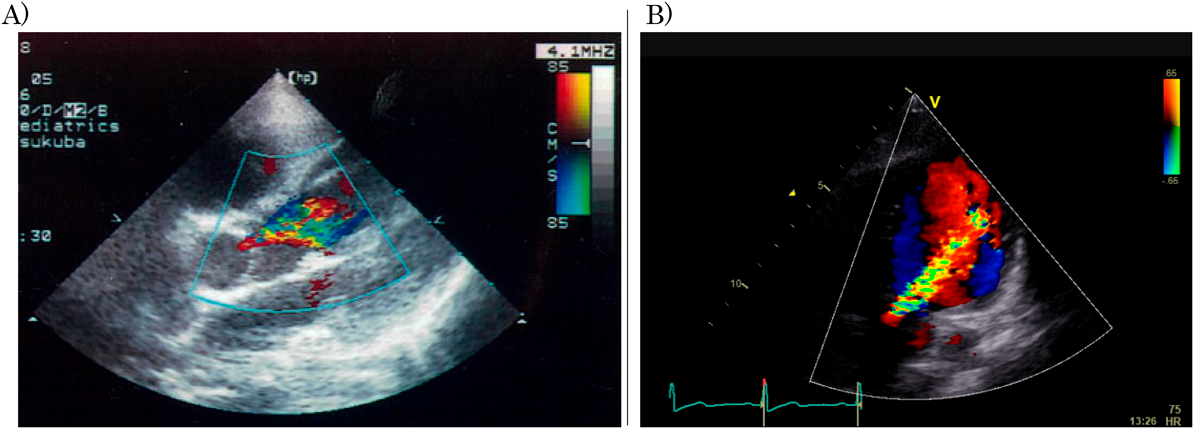
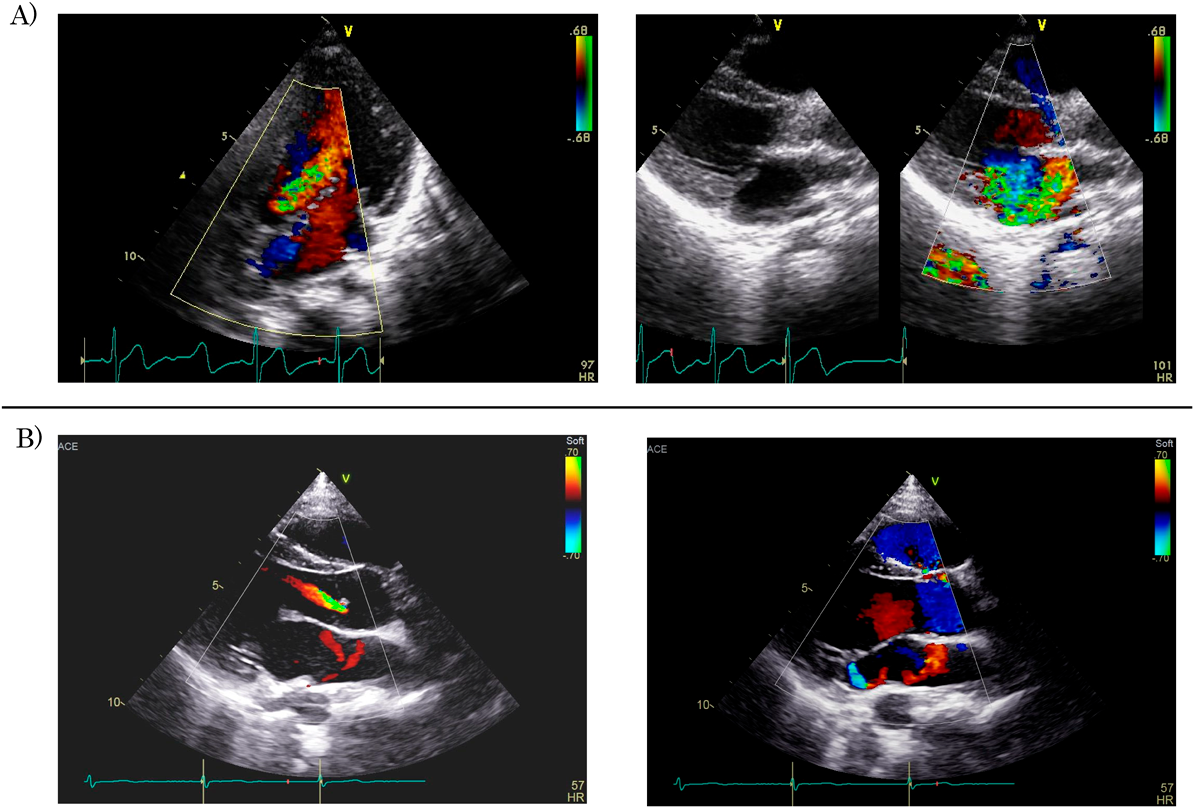
診断時すでに弁膜症を呈していた5例では長期的に弁所見が残存した.ARは長期に残存することが多く,予後に影響した.MRは初期には重度でも長期には全例治療不要な状態にまで改善した.高度房室ブロックを伴い,ステロイドによる治療が先行して実施されていた症例5においては,経過中に軽度のARが出現したが完全に消失し,弁の形態異常も指摘されなかった.残る4例はすべて何らかの弁所見が残存した.心不全が認められた3例中2例(症例2, 4)は大動脈弁置換が必要となった(Fig. 1).残る1例(症例1)も急性期治療終了時には中等度以上のMR, ARが残存していたが,長期的に弁所見が改善し(Fig. 2),抗心不全薬からの離脱可能な状態まで改善した.症例6は治療開始時心不全兆候が認められず,PSLの投与を行わなかったが,長期的にARは軽度増悪傾向を示した.
ARFの診断
今回の6例においては,major criteriaとしては,心炎と多関節炎以外は認められなかった.特に初期症状はほとんどが関節炎であり,ARFの診断にいたった理由は全例が心炎の合併であった.初診時に小児科以外を受診した症例は十分な聴診が行われないことがあり,弁膜炎のスクリーニングもされないため,このことがARFの診断の遅れに関係していたと推察される.ARFの診断が遅れた症例は,初期には溶連菌感染後反応性関節炎(post-streptococcal reactive arthritis, PSRA)や若年性特発性多関節炎(juvenile idiopathic arthritis, JIA)の診断で治療を受けており,心雑音の出現で初めてARFを疑われた.多関節炎におけるARFの鑑別の必要性が改めて示唆された.
本報告例にみられた関節炎・関節痛はいずれもNSAIDs,アスピリンに反応して改善した.NSAIDsによく反応し,1週間程度で移動して関節破壊を呈さない『移動性』多発関節炎は本疾患に特徴的と言える所見で,ARFの早期診断の糸口となり,PSRAやJIAとの鑑別にも有用と報告されている6).近年,PRSAとARFの鑑別について,関節炎部位,血清学的なCRPやESRの上昇の程度,NSAIDsへの反応と関節痛罹患期間,罹患関節の移動などである程度可能と報告されている6, 7).PSRAでは通常二次的な心炎は合併しないが,ARFの除外診断が不十分であると心炎の診断が遅れることが懸念されている8).PSRAの診断はARFの除外によってなされるべきであり,ARF診断不確実例でも疑われた場合は1年以上の抗菌薬予防内服,心エコーの反復検査が推奨されている5).本報告において弁置換を必要とした症例2,4は,いずれも聴診がなされないまま関節炎として治療されていたため診断までに日数を要し,弁逆流が進行した状態で診断された.RHDは感染したGASのM蛋白と心筋,弁膜内皮細胞との分子相同性を契機にした,抗連鎖球菌/心筋モノクローナル抗体の産生や交差反応性T細胞の浸潤で始まり,経時的に弁の病理学的変化が進行する9).ARF患者はその後の溶連菌感染でも容易に弁の所見が進行することが知られており4, 5),診断が遅れると,弁の機能異常は進行する.そのため,早期診断,完全除菌,再感染予防が必要である.特に症例4は他院で関節炎とGASを同定されたもののPSRAと診断され,退院後経過観察を受けていなかった.4年10か月後に心不全を呈して当院で精査を受けた際に,既往の関節炎が移動性関節炎であったこと,心雑音があったことからARFと診断された.経過中に再感染や心炎増悪を繰り返していた可能性が考えられた症例であった.逆に,発症後3日で診断された症例1は診断時にはAR, MRともに重度であったが,長期予後は良好であった.
今回,診断基準に合致する心電図異常は症例5のみで認められた.弁膜炎の所見とPR延長に明らかな関連は見いだされなかった.近年,ARFの経過中にはPR延長だけでなく,期外収縮や脚ブロックなども認められるとする報告が増加している10, 11).今回の経験でも,重度のAR, MRを認めた症例1では急性期に上室期外収縮が認められ,治療とともに消失した.心炎の症状としての期外収縮が示唆された経過であった.症例5はPQ延長から進行して,高度房室ブロックに至り,治療開始後速やかに洞調律に復調している.高度房室や完全房室ブロックを呈する症例はまれで,いずれもARFの改善とともに正常洞調律に復調し,PR間隔も正常に戻ると報告されており,合致する経過であった10–13).一方でAdams-Stokes発作を起こし,ペースメーカーの埋め込みが必要となった症例の報告もあり,注意が必要である13).刺激伝導系の障害が心炎とどのように結びつくのか病理学的にはこれまで十分に検討されていなかったが,2016年に池田らが心臓突然死を起こした12歳男児において病理組織学的に房室結節にARFに特徴的なAschoff小体の集簇があったことを報告し,房室ブロックが心炎と関連していることを証明した14).
弁膜炎の治療
現在RHDの治療は,GASの再発予防と抗心不全療法,進行した弁膜症への手術療法が中心となっており,近年の研究においても弁膜炎の進行の抑制に関する抗炎症療法の有効性は報告されていない3, 4, 15).しかしながら,病態生理学的にはRHDの進行にTNF-αなどの炎症性サイトカインの上昇が関連し,弁膜炎の重症度と相関することが指摘されている16).このことは発症早期の弁膜炎に対しては抗炎症療法が奏功する可能性を示唆していると考えられており,本報告でも,治療開始が早かった症例1は初期には弁所見が高度であったが長期的には予後良好であったのに対し,心不全兆候がなくPSLの投与を行わなかった症例6のARは長期的には悪化傾向を示したことは,早期の抗炎症療法が弁膜症の予後にかかわりうることを示していると考えられた.
現在まで,抗炎症療法がRHDに対して有効であるというエビデンスが得られない理由として,心雑音を呈さない潜在性心炎は2015年の改定まで心炎として認められていなかったこと,先進国においてはARF自体がまれとなり,十分な解析が困難であることが考えられる.2015年の改定により,心エコーがリウマチ熱の心炎の基準として明確に取り入れられたことで,RHDの早期診断の機会が増え,今後抗炎症療法の有効性が示される可能性がある.