近年のリアルタイム3D心エコー法は,マトリックスアレイトランスデューサーの開発と発展,超音波装置に内蔵されるハードの演算能力の向上,加えて3D解析ソフトウエアーの進歩により,3D探触子でvolume dataを短時間に収集,再構築することができるようになった.心拍の速い小児で壁となっていた3D画像の時間分解能や距離分解能の低さは,飛躍的に改善されつつある1).
先天性心疾患の外科修復におけるプランニングやガイド対する3D心エコーの実臨床応用としては,心房中隔欠損や心室中隔欠損の形態評価により,両大血管右室起始症における心室中隔欠損を用いた心内ルート作成に,先天性心疾患の房室弁評価により,複雑な弁形成に,心内の複雑な構造や狭窄病変に対する形態評価により,術後心内狭窄病変の解除,総肺静脈還流異常症の心内ルート作成に用いるのが特によいと考えられる.複雑な心内構造を外科医からの視点(Surgeon’s view)で観察し,解剖学的と手術法について,外科医と循環器医でより深いdiscussionを行うことができる2, 3).
1. 画像の収集について
よいクオリティの3D画像を得るためには,volume dataの収集がもっとも重要なkeyとなる.小児とくに10 kg以下の症例ではできるかぎり高周波の3Dプローベを用いる(7 MHz以上).Volume rate(Frame rate)は心拍100 bpm以上の小児では少なくとも40 Hz前後は必要であろう.
収集に用いる基本断面(中心断面)は,典型的な四腔断面,長軸断面,短軸断面などではない.例えば,乳幼児の心室中隔欠損では肋骨下からの断面が最も適しており,一方で房室弁では傍胸骨でやや心尖部よりからの短軸断面がよいことが多い.
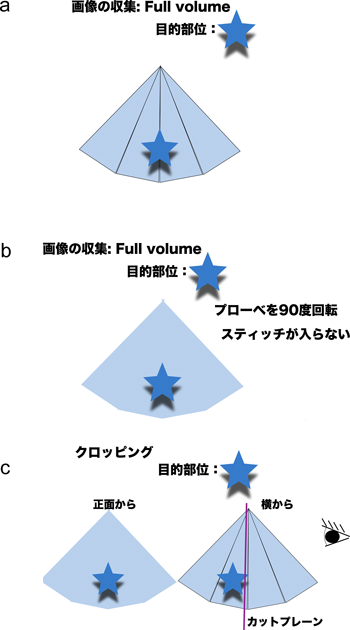
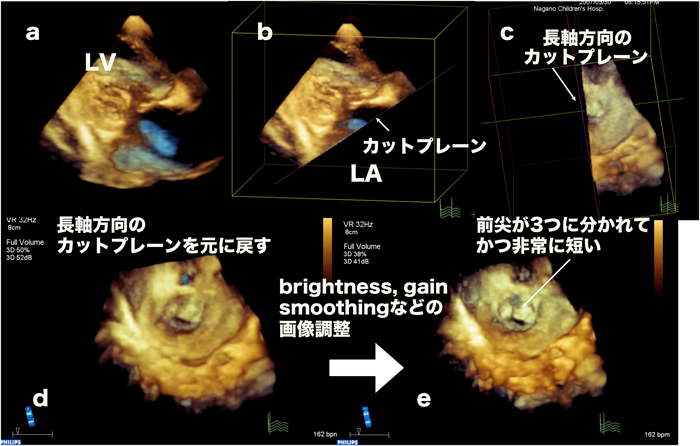
まず,目標部位が中心となって,周囲構造が最もよく描出されている断面であることを2D画像で確認する.3DのX-planeなど複数断面が同時に観察されるモードを使用して,目標物がすべてvolume dataに入っていること,VSDなどでは周辺の構造物がvolume dataの中に入っているかを確認して広角に取り込む方がよい.このときvolume rateが30 Hz前後と低いシングルビートでの収集より,心電図を同期させた4~6スライス(心拍)を統合したフルボリュームモードでなるべく高い40~50 Hz以上の設定で取り込む方がきれいな3D画像を収集することが可能である.しかし,マルチスライスだとモーションスティッチがどうしてもが入ってしまうので,2D画像で3D画像の中心をどこに置くかを見定めたのち,最終的にクロッピングする断面がプローベの断面と平行になるように,目標部位を短軸のフルボリュームで収集する.すると目的とする構造物の中心が1つのスライスの中に入りやすくなる(図1a~c).
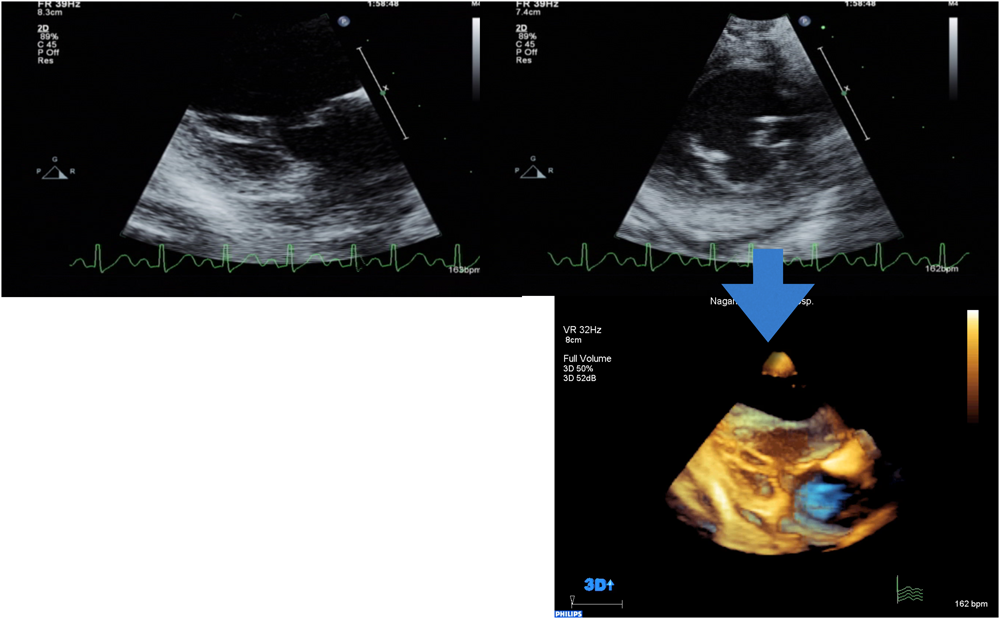
例えば図2では,肋骨下のwindowから心室中隔欠損を描出した両大血管右室起始症の画像である.バイプレーンモードや実際に探触子をその場所で傾けて目標部位:心室中隔欠損と周囲構造物:三尖弁,肺動脈弁,大動脈弁のすべてがよく描出できているのを確認する.さらに2D画像上でfocus,gain,dynamic rangeなどの調整を行う.このとき心室中隔欠損を正面からみた2D画像(en face view)を基本に3D画像をフルボリュームモードで取り込む.このように収集前に2D画像でよく確認することが非常に大切である.
房室弁ではさらに画像収集方法に工夫が必要である.図3は,乳児の先天性僧帽弁閉鎖不全の症例である.やや心尖部からとった傍胸骨長軸断面の2D画像でよく僧帽弁が描出されているwindowを確認する.小児の房室弁は弁葉が薄いため,クロッピングの際にgainを下げてノイズリダクションすると3D画像ではさらに弁葉の輝度が低下して弁葉の画像がとんでしまいまるで孔があいているように見えてしまう.したがって弁葉の輝度が最もはっきり見えるwindowを見つけることが必要である.また,心尖四腔断面像を基に3Dを収集すると房室弁からプローベが目標物から遠くなるので,避けた方がよい.経胸壁ではこのやや心尖よりからのwindowでの収集を奨める.このwindowのままプローベを90度回転し,再度X-planeやbiplane modeで表示される長軸断面で弁葉の輝度を確認して短軸像を基に3D volume dataを収集する.するとクロッピングしたときにマルチスライスによるスティッチが入らない.
2. クロッピングをする前の準備
やみくもにvolume dataのクロッピングを行ってもよい3D画像はできない.外科的修復術のガイドとして先天性心疾患の3D次元表示をする場合,もっとも重要なのは,どのように外科医に見せるかを考えることにある.前もってその疾患の一般的な解剖学的特徴と術式を知っておき,具体的にどのようにクロッピングすべきかを予想をすることで微妙なクロッピング面の角度の調整が可能となる.
3. クロッピング
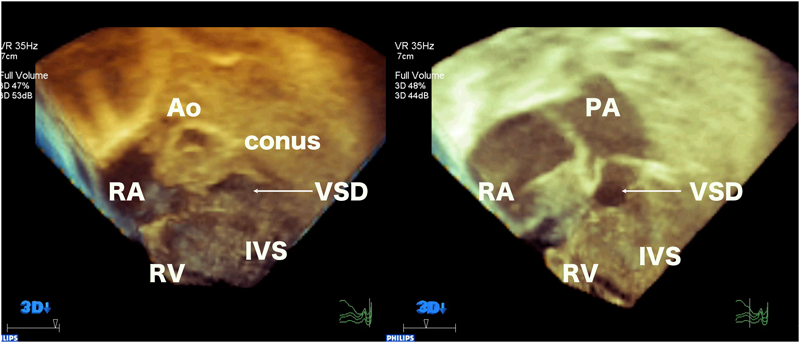
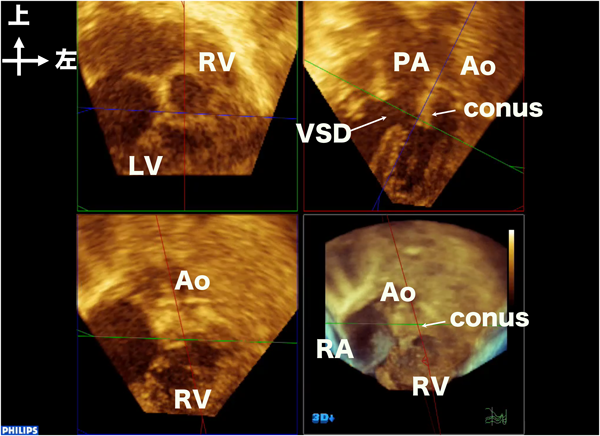
両大血管右室起始症例で実際のクロッピングをしてみる.図4左はvolume dataの右室前面をカット:クロッピングした3D画像である.大動脈弁の下の広い範囲でconus:漏斗部中隔が見える.その向こうに心室中隔欠損が確認できる.図4右は断面をさらに奥に進めると肺動脈弁とその下の大きな心室中隔欠損が確認できた.図5右上のように,心室中隔欠損を中心に矢状断面でもカットすることで前から大動脈,肺動脈,心室中隔欠損の順に並び,この画像からJatene手術をすれば左室から大動脈に狭窄なくルートがとれることがわかる.
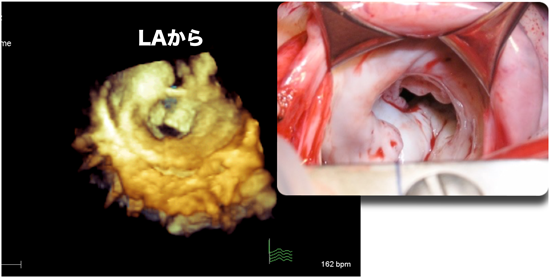
次に前述の僧帽弁閉鎖不全の症例をクロッピングしてみる.まず,左室長軸断面となるような平面でボリュームデータをカットする(図6a).次にもう1面の任意のカットプレーンで左房をカットしていくが,このとき平面ができるかぎり弁輪と平行になるように調整して弁輪に近づけ,ノイズリダクションを行う(図6b).長軸方向にカットした平面をもとに戻して,左房側からみるとSurgen’s viewの僧帽弁画像が得られる(図6c, d).この症例は,前尖が短く三つに分かれ,後尖との間に大きな間隙ができている.この間隙から閉鎖不全が生じていた.この前尖には全く腱策が付着しておらず,低形成な前尖であることがわかる.さらに後尖はtetheringして持ち上がっていない(図6e).弁輪縫縮を加えても弁形成が不可能と判断し,かつ術中所見も一致したため(図7),人工弁置換術を施行した.
我々は先天性心疾患の術中に経心膜3Dエコーを行い,経胸壁心エコーより詳細な心内構造の所見を得ている.手術を受ける小児例の多くは15 kg以下で,経食道3D心エコーのプローベを挿入,使用することはできない.経心膜3D心エコーは直接心臓にあてるために画像は非常によいのはもちろんである.したがって画像収集をうまく行えば精度の高い3D心エコー法が可能となる.全身麻酔下で開胸後に,心膜もしくは心臓の上から高周波3D用プローベをあてて,必要なら一時的に人工呼吸を停止させ,フルボリュームモードを撮像する.解像度,S/N比とも良好で鮮明な画像が得られる.
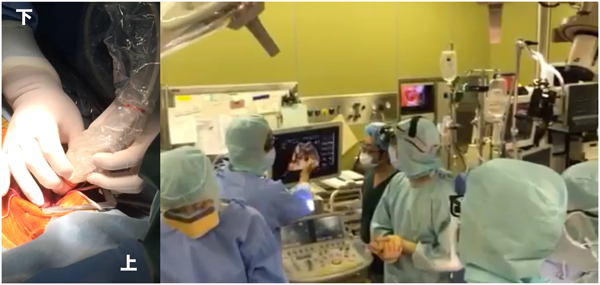
画像収集方法は,前述の経胸壁アプローチと変わりないが画角が十分に取れないため,目的の構造物が画角の中に入っているかどうかに十分に注意を払う必要がある.画像収集時のこつは,心臓を無理に押さえつけないように,血圧に注意しながらプローべを心拍に同期させるようにソフトに密着させることである.両手を使い,片方の手で心臓にあて,もう片方の手でプローベをコントロールするとよい(図8右).
1. 症例1
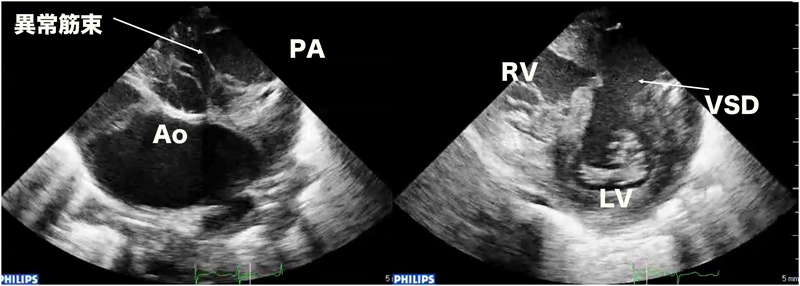
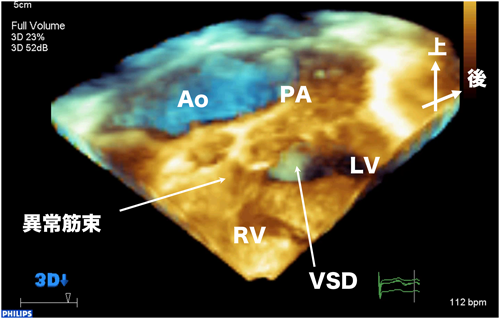
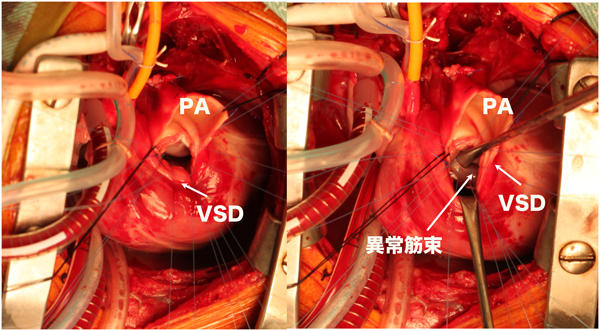
図9に両大血管右室起始症の症例を示す.経心膜2Dエコーでこの心室中隔欠損は大きく肺動脈弁下にあいている.しかし,心室中隔欠損の右縁あたりから異常な筋束が右室自由壁にわたっているのが見える.この筋束と心室中隔欠損の関係について,右室自由壁側をクロッピングして3次元的に描出したのが,図10である.大きな心室中隔欠損を左右に分けるかのように太い異常な筋束が心室中隔欠損の間から右室自由壁までわたっている.つまり,診断は肺動脈弁下型および大動脈弁下型の多孔性の心室中隔欠損となる.図11は肺動脈側から心室中隔欠損を見た画像であるが,肺動脈側から向こう側の大動脈弁下の心室中隔欠損は異常筋束によって確認できない.実際の術中所見でも肺動脈からは弁下のVSDしか見えなかった(図12).よって,大動脈弁下の心室中隔欠損は三尖弁側から,肺動脈弁下の心室中隔欠損は肺動脈弁側から別々にパッチ閉鎖する必要があった.
2. 症例2
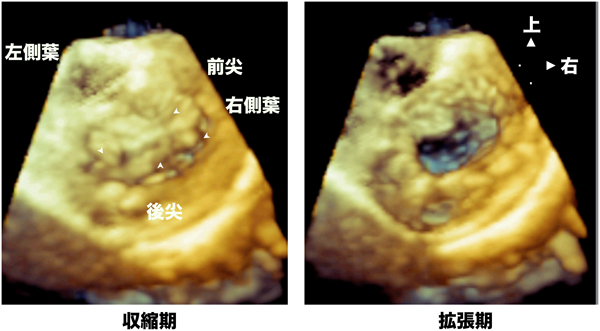
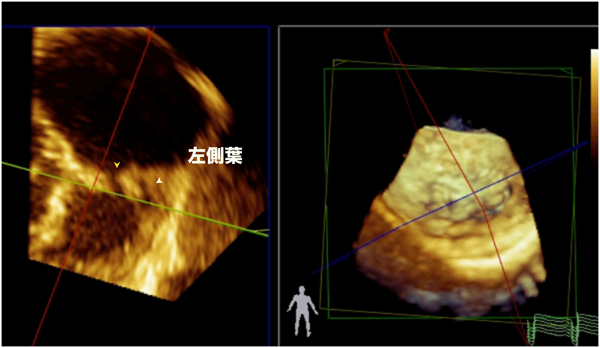
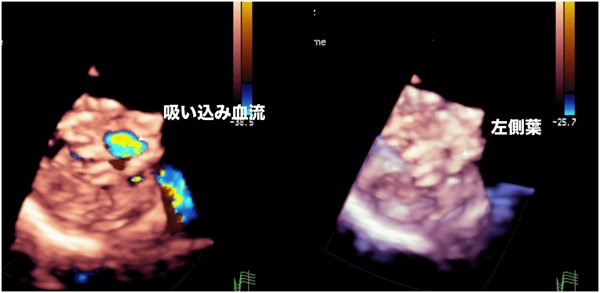
図13の経心膜3D心エコーは,無脾症候群,右室性単心室,重症共通房室弁閉鎖不全の症例である.心房側から見ると,共通房室弁は4葉あり,収縮期と拡張期で見ると左側葉が小さく可動が非常に悪いのがわかる.図14左は左側葉にあわせてvolumeデータを水平面でカットしたものだが,収縮期にcoaptationしていないのがわかる.図15は共通房室弁を心室側から見たカラー3D表示で心室側からの吸い込み血流によるaliasingが生じている.閉鎖不全は同部位で生じていることを確認できた.この症例は2歳,10 kgの症例で,リングによる弁輪縫縮ができないため,この左側葉をKai–Lead法という方法でつぶして弁形成を行った.
このように,共通房室弁や三尖弁は3~5葉の弁であり,閉鎖不全のメカニズムの正確な詳細診断は2Dではまず困難と考えてよい.3D心エコーとくに経心膜で,弁葉の逸脱,テザリング,異常構造の範囲,人工腱策の必要性を見て弁形成や人工弁置換の適応などを判断する.
3. 症例3
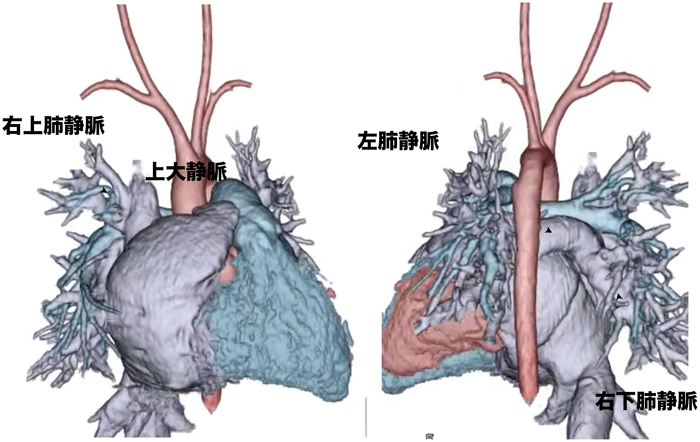
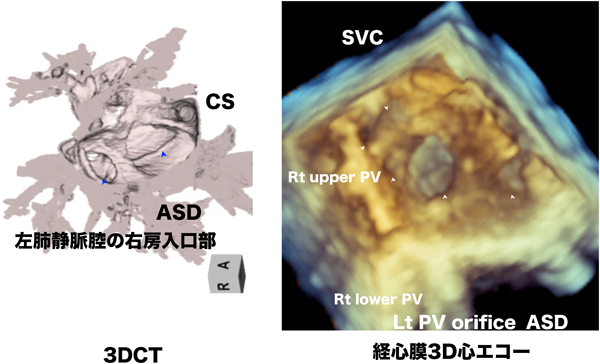
図16は総肺静脈還流異常症のIBとIIBの新生児症例の3DCT画像である.右上の肺静脈は上大静脈に還流,その他の肺静脈は右房に還流していた.3DCTを右房から見てみると左肺静脈の開口のとなりに大きな心房中隔欠損が見える(図17左).しかし,経心膜3D心エコーでは,右房を開けたSurgeon’s viewで見てみると,右上下の肺静脈の還流と左肺静脈の還流部位がよく見え,さらにCTと異なって小さな心房中隔欠損が確認できる(図17).新生児症例で心内のCT画像構築が難しくても3D心エコーでは鮮明に観察することが可能であった.この症例では,肺静脈から左房への心内のルート作成のガイドに非常に有用であった.