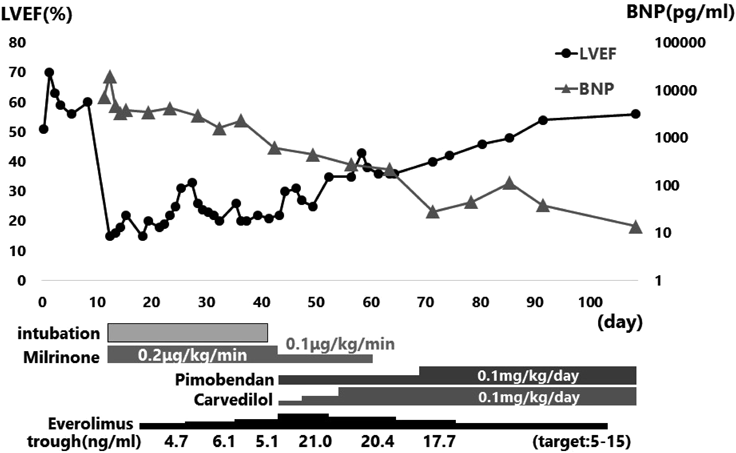
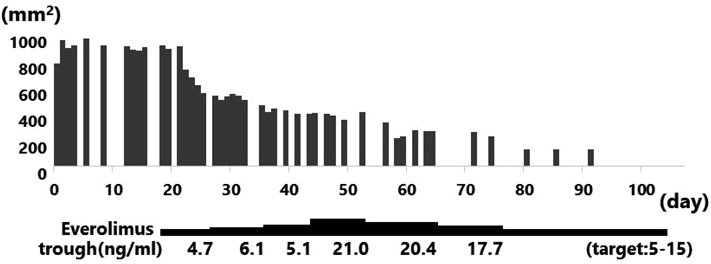
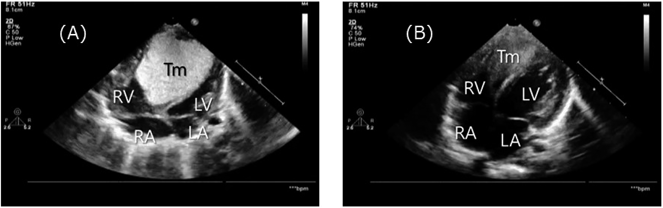
循環破綻を来すほど巨大な心臓横紋筋腫に対し,救命のためeverolimusを使用した1例Regression of Massive Cardiac Rhabdomyoma Causing Circulatory Collapse with Everolimus Therapy
重光 祐輔1,馬場 健児1,近藤 麻衣子1,栗田 佳彦1,栄徳 隆裕1,福嶋 遥佑1,平井 健太1,吉本 順子2,鷲尾 洋介2,大月 審一1Yusuke Shigemitsu1, Kenji Baba1, Maiko Kondo1, Yoshihiko Kurita1, Takahiro Eitoku1, Yosuke Fukushima1, Kenta Hirai1, Junko Yoshimoto2, Yosuke Washio2, Shinichi Otsuki1
1 岡山大学病院小児循環器科Okayama University Hospital, Pediatric Cardiology ◇ Okayama, Japan
2 岡山大学病院小児科Okayama University Hospital, Pediatrics ◇ Okayama, Japan
受付日:2016年5月14日Received: May 14, 2016
受理日:2016年8月27日Accepted: August 27, 2016
発行日:2016年9月1日Published: September 1, 2016