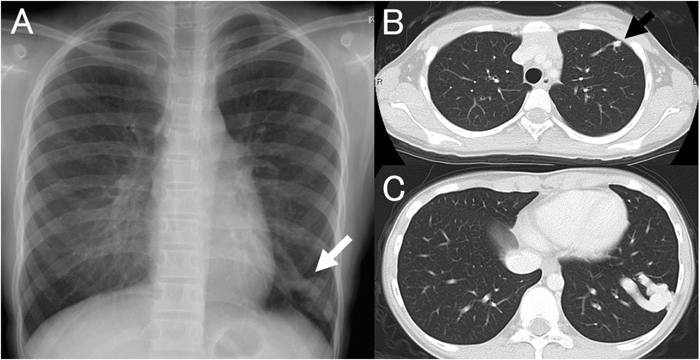
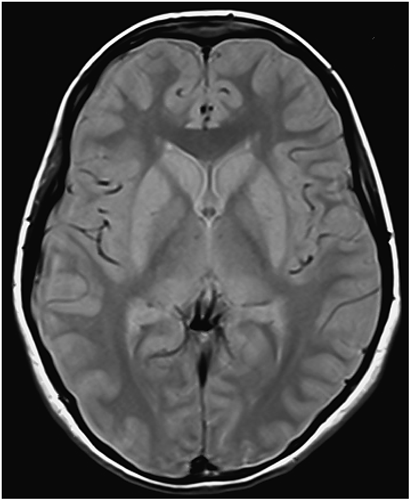
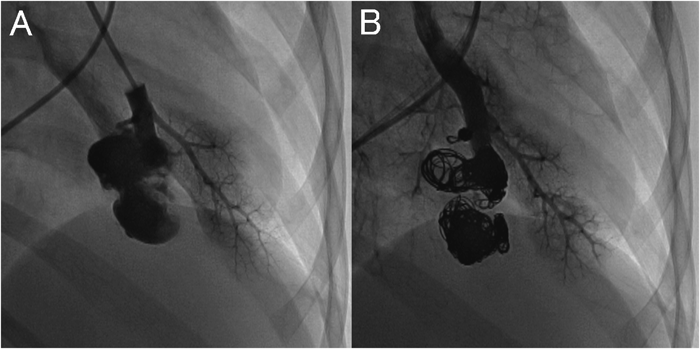
肺動静脈瘻を伴う遺伝性毛細血管拡張症の新規遺伝子変異1女児例A Case of Hereditary Hemorrhagic Telangiectasia with a De Novo Mutation in Endoglin
1 横浜市立大学附属病院小児循環器科Department of Pediatric Cardiology, Yokohama City University Hospital ◇ Kanagawa, Japan
2 国立循環器病研究センター研究所分子生物学部Department of Bioscience and Genetics, National Cerebral and Cardiovascular Center Research Institute ◇ Osaka, Japan
3 国立循環器病研究センター小児循環器科Department of Pediatric Cardiology, National Cardiovascular Center ◇ Osaka, Japan
4 神奈川県立こども医療センター循環器内科Department of Cardiology, Kanagawa Children’s Medical Center ◇ Kanagawa, Japan