新生児期集中管理:重症疾患の手術までNeonatal Intensive Care for Critical Cardiac Disease
長野県立こども病院小児集中治療科Department of Pediatric Intensive Care, Nagano Children’s Hospital ◇ 〒399-8288 長野県安曇野市豊科31003100 Toyoshina, Azumino-shi, Nagano 399-8288, Japan
新生児期の重症先天性心疾患を適切に管理することは,小児医療向上の重要な課題の一つである.循環管理には心収縮力・前負荷・後負荷・心拍数に規定される心拍出量と,流出路大血管形態・血管抵抗に規定される肺体血流バランス,合わせて6要素を評価しながら行う必要がある.新生児期の循環管理では,肺血流増加によるショックを事前に予防し,安定した循環動態で手術につなげることが主たる目的であり,血行動態変化を事前に予測して管理し,循環管理には速やかな集中治療を導入することが必要とされる.周産期の重症先天性疾患は,疾病による循環異常だけでなく,周産期特有の全身生理の理解と外科的治療選択の判断が必要となり,総合的に全身管理を施行することが重要である.新生児期の重症先天性心疾患の術前管理にゴールデンマニュアルはない.正確な血行動態の評価のもと適切に管理を行い,安定した血行動態で外科的治療にのぞむことが重要である.
Adequate circulatory management in critical congenital heart diseases is vital in pediatrics because of poor prognosis. Understanding and managing factors such as contractility, load, cardiac morphology, and vascular resistance are vital in controlling cardiac output and maintaining balance between the systemic and pulmonary circulations. Particularly, in neonates, securing systemic blood flow through the regulation of pulmonary blood flow is an important issue, because there is a high risk of cardiogenic shock with increased pulmonary blood flow, resulting in general deterioration or death. Furthermore, not only cardiac care but also general care is needed to prevent several complications including non-cardiac complications. Detailed diagnosis, accurate understanding of the pathophysiology, and prediction of hemodynamics will lead to improved care of neonates with critical congenital heart disease.
Key words: neonate; congenital heart disease; intensive care; cardiac output; morphology
© 2015 特定非営利活動法人日本小児循環器学会© 2015 Japanese Society of Pediatric Cardiology and Cardiac Surgery
重症先天性心疾患は乳児死亡原因の第一位を占め,新生児期の重症先天性心疾患を適切に管理することは,小児医療向上の重要な課題の一つである.新生児期の重症症例の多くは,外科的もしくはカテーテルによる治療を必要とすることから,出生後から治療介入までの管理を可能な限り良好に保つことが予後改善に重要と考えられる.さらに周産期の重症先天性疾患は,疾病による循環異常だけでなく,周産期特有の全身生理の理解と外科的治療選択の判断が必要となり,総合的に全身管理を施行することが重要である.
先天性心疾患の血行動態管理において重要な点は,“心拍出量を規定する要因”と“心血管の形態・血管抵抗による肺体血流バランス”を常に念頭に置く必要がある.
心臓は血液を全身に送るポンプである.一般の機械ポンプに比較して動物の心臓に特徴的なことは,Frank-Starlingの心臓法則にあるように,負荷により拍出量が変化することである.すなわち心ポンプ機能の評価に負荷という概念を組込む必要があり,心拍出量の規定には前負荷・後負荷・心収縮能・心拍数といった規定因子がある.先天性心疾患の管理においてもこの基本的法則はあてはまり,血行動態管理においては常にこの四要素を念頭に入れることが重要である.
前負荷は容量負荷とも言われ,“心室に流入してくる血液量”すなわち,半月弁逆流がなければ房室弁を通過する血流量と考えてよい.房室弁通過血流が増加すると,Frank-Starlingの上行脚の範囲内であり,かつ心収縮力と後負荷が一定であれば,心拍出量と血圧は上昇する.この時,内因性エネルギー(Elastic Potential Energy)は若干増加し,外的エネルギー(External Work)は拍出量に比例して増加,すなわち心筋酸素消費量が増加する.このことから一般の臨床においてVolume負荷を行った際には,心室のエネルギー消費を増大させることで血圧と心拍出量を増加させていることが解る(Fig. 1A, B).
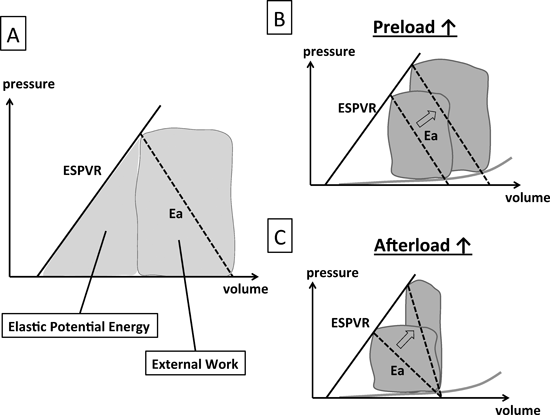
A: End-systolic pressure volume relationship (ESPVR) is a parameter of cardiac contractility. Arterial elastance (Ea) is a parameter of afterload. The triangle area surrounded by ESPVR and the pressure volume loop demonstrates elastic potential energy in a single beat. The square area surrounded by the pressure volume loop shows external work in a single beat. B: In cases of increased preload, cardiac output, blood pressure, and cardiac oxygen demand are increased by elevation of elastic potential energy and external work. C: In cases of increased afterload, cardiac output is decreased, whereas cardiac energy consumption (elastic potential energy and external work) is increased, resulting in deterioration in the efficiency of pump function.
後負荷は圧負荷とも言われ,“心室の出口である大血管の弾性率”で表され,心室拡張末期容積が一定であれば心室収縮末期圧に規定される.血管収縮効果により後負荷を増加すると,心収縮力と前負荷が一定であれば,心拍出量は低下し血圧は増加する.この時,内因性エネルギー(Elastic Potential Energy)は増加し,拍出量が低下しても外的エネルギー(External Work)は大きく変化しない.このことから一般の臨床において血管収縮作用による昇圧効果は,心室のエネルギー消費を増大させるが心拍出量を低下させるので,非効率な血行動態に変化すると考えられる(Fig. 1B, C).
心収縮能は心室形態が左心室か? 右心室か? 心筋性状・心筋繊維走行・心室内伝導・心形態・ホルモン・薬物等により規定される,ある時点での心室固有の能力と考えられる.様々な負荷の変化に生理的範囲内で順応することで,様々な状況変化に対応している.心収縮能低下を改善するには,心筋細胞内のカルシウムハンドリングを改善する薬剤を選択する場合が多い(カテコラミンβ受容体刺激薬・PDE3阻害薬等).
一般的には,心拍数が増加しても前負荷の減少がなければ一回拍出量は保たれることから心拍出量は増加する.徐脈は心室拡張期を延ばし前負荷増加による一回拍出量増加の可能性はあるが,心拍数減少による心拍出量低下の影響が強い.また頻脈は心室拡張期を短縮し前負荷減少を生じる可能性がある.
心臓から駆出された血液により生命を維持するため,許容範囲の体循環と肺循環を維持する必要があり,血行動態の管理上最も重要な事項は体循環血流量の保持である.一方,肺血流は血液酸素化に大きく寄与するが,特に新生児期の先天性心疾患においては,体循環血液量が保たれていれば各臓器への酸素供給量は保たれることから,必ずしも肺血流が多く必要とはならない.心拍出量が十分にある場合には,肺血流量が多くても体血流量が保たれていれば循環動態は保たれるが,心拍出量が乏しい場合には肺血流量が少ない状態(すなわち低酸素血症)でも体血流量保持を優先しなければならない.すなわち,体血流量を確保することが最も重要であり,心拍出量をふまえた上で体血流と肺血流のバランス管理をする必要がある.
体肺血流バランスを考える際に重要なことは,“流出路から大血管までの形態”と“体血管と肺血管の血管抵抗”を評価する必要がある.駆出された血液の流れは,心室–大血管関係・流出路形態・半月弁形態・大血管径等といった心血管形態により大きく左右され,それ故に心エコー検査による形態診断は血行動態を把握するために極めて重要であることは言うまでもない.正確な形態診断が先天性心疾患の血行動態管理上極めて重要であるということであり,循環管理を行う医師は常にその評価ができる体制を構築しておかなければならない.
体血管抵抗が肺血管抵抗に比して高いことは広く知られている事実である.胎児期の肺血管抵抗は肺胞が虚脱していることから体血管抵抗に比して極めて高いが,出生の第一呼吸により劇的な変化を示す.出生直後の肺血管抵抗は体血管抵抗とほぼ同等まで低下し,その後,日を追うごとに肺血管抵抗は低下していく.肺血管抵抗の低下の程度は個人差が大きく,数日で十分に低下する場合もあれば,21トリソミーといった全身疾患の合併や全身状態が不良であることで肺高血圧が遷延化する例も稀ではない.
以上のように心拍出量によって規定された循環血液は,心大血管形態と血管抵抗によって体肺血流量が決定する.新生児期は肺血管抵抗の変動が大きいことから,肺血流量が増加し体血流量が減少する場合が比較的多い.以上のことを念頭に置きながら,心収縮力・前負荷・後負荷・心拍数の4つの要素に規定される心拍出量と,流出路大血管形態・血管抵抗の2要素に規定される肺体血流バランス,合わせて6つの要素を評価しながら循環管理を行う必要がある.
新生児期の循環管理を行う最大の目的は体循環血液量を確保することであり,その評価は極めて重要である.顔色・末梢の暖かさ・脈拍触知やCapillary Refill Timeといった臨床所見は極めて重要であり,様々な検査に先立って評価が必要な項目である.その臨床所見にモニターのパラメータや検査所見が合致するかどうかにより体循環量の確保の程度を定性的に評価できる.尿量は古典的な体循環の指標であり日常臨床で使用されているが,利尿剤使用時には体循環血流量を過大評価する可能性があり,逆に腎不全時には体循環血流量を過小評価する可能性がある.血圧は心拍出量と後負荷の結果として得られる数字であり,心拍出量の減少時にも後負荷が高い場合には低血圧を示さないことから,体循環量を過大評価する可能性がある.この場合には血管内血液量の減少により動脈血圧ラインの波形のDicrotic Notchが消失したり基線の呼吸性変動が見られる場合がある.体血流量が減少すると静脈酸素飽和度(SvO2)は低下することから,体循環の評価の指標になる.体血流減少時には循環時間が長くなることから,静脈血液ガス所見でpH低下・Base Excessの低下・CO2の貯留・Lactateの上昇する場合があり体循環の指標になるが,この場合でも動脈血液ガス所見では保たれていることが多い.また体循環減少時には近赤外線光を用いた脳内酸素飽和度測定も低値を示すことが多く,体循環減少の指標となる.
心拍出量は心収縮能・前負荷・後負荷・心拍数を評価し,必要と思われる心拍出量を管理することが必要となる.収縮末期圧容積関係(ESPVR)は収縮能の指標であるがベッドサイドでの測定は困難であり,心収縮能は心エコーにて実際の心筋の動きを定性的または半定量的に評価するのが一般的である.前負荷はCVP測定やIVC径の観察により推定する.後負荷は平均血圧・四肢の末梢所見等で定性的に推定する.これらの3因子で一回拍出量が決定され,心拍数により心拍出量が規定される.CVPやIVC径は前負荷と常に相関するわけではなく,後負荷も実測値としての算出は困難であり,ベッドサイドでの心室負荷は総合的に判断するしかない.
実際の臨床では,低いCVP・良好な末梢循環・尿量と血圧の維持・血行動態に矛盾する低酸素血症がなければ良好な心機能であることが推察できる.例えば循環血液量減少が示唆される場合は,前負荷・心収縮能・心拍数を評価し,心拍出量増加を試みる.この際には血管収縮作用の強い薬剤は心筋酸素消費量の増加と心拍出量の低下をきたす可能性がある.管理中,高血圧が認められ,前負荷過剰と示唆された場合には利尿剤等による前負荷軽減を,後負荷過剰と示唆された場合には血管拡張薬等による後負荷軽減を,強心剤使用による心過収縮が示唆される場合には強心剤減量を考慮し,心拍出量の調整を行う.心収縮・心負荷に矛盾しない臨床症状・モニター値・検査値であれば一般的には安定した血行動態と考えられ,逆に矛盾点が存在する場合にはたとえモニター値が正常範囲内だったとしても,血行動態評価を再確認するのが望ましい.
体肺血流バランスは主に心血管形態と体肺血管抵抗により規定される.主に,血流バランスが体血流優位(Low Pulmonary Blood Flow)もしくは肺血流優位(High Pulmonary Blood Flow)となるかは形態診断により決定される.多くの新生児期の重症先天性心疾患は形態上,肺血流優位・体血流減少となる場合が多く,生後数日で体血流不全すなわちショックとなる場合も少なくない.
肺体血流比はFick法に基づく計算で概算され,肺静脈の酸素飽和度を100%と仮定した場合,動脈酸素飽和度と混合静脈血酸素飽和度で計算できる.体肺血流比1 : 1を目指して循環管理を行うのが一般的であり,管理上の注意点は,経皮的酸素飽和度モニター(SpO2)は必ずしも動脈血酸素飽和度(SaO2)と一致しないこと,体循環量によって静脈酸素飽和度(SvO2)は大きく変動することを念頭に置き,必要に応じてSpO2,SaO2,SvO2を比較することが重要である.
前述のように新生児期の循環管理において問題となるのは肺血流増加による体血流減少であることが多く,これに対して肺血流減少または体血流増加を目的とした血管作動療法が選択される.肺血管収縮は低酸素性肺動脈攣縮現象を利用した肺血管収縮により,肺血管抵抗を上げることで肺血流量を低下させる治療が一般的である.これは空気に窒素を付加し低濃度酸素で換気することで肺血管収縮を惹起し(Fig. 2),肺血管のみを選択的に収縮することができる治療で,肺体血液バランスの管理に極めて有用である.肺血管抵抗増加目的に血管収縮剤を使用することは,体血管抵抗も増加させ心臓負荷・心筋酸素消費を増大させるために使用を避けることが望ましい.
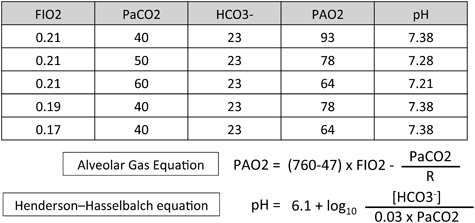
Alveolar oxygen pressure and arterial blood gas can be calculated using the alveolar gas equation and Henderson–Hasselbalch equation. Alveolar oxygen pressure decreases upon inhalation of air that is low in oxygen. Although hypoventilation causes low alveolar oxygen pressures, pH is decreased by hypercapnia, resulting in metabolic acidosis.
一方,体血管抵抗を下げて体循環血液量を増加させる治療は,調整が難しい.血管拡張剤による血管拡張作用を補う体血流量の増加が得られない場合には血圧低下を呈する可能性がある.また血管選択性により肺血管抵抗も下げることで,肺血流増加を助長する可能性もあり,循環動態を悪化させる危険性もある.したがって肺血流増加時に血管拡張剤を使用する際には,窒素による低濃度酸素を使用した肺血管を選択的に収縮させる治療を併用できる準備をしておくのが肝要である.また,四肢末梢の保温等の体循環改善は,古典的な治療ではあるが有用と考えられる.
生後,日を追うごとに肺血管抵抗が低下することで体循環不全が生じた状態(いわゆるHigh Pulmonary Flow Shock)は,新生児期重症先天性心疾患の予後を不良にする因子である.体血流減少が示唆された際には,酸素消費量の低下・心拍出量増加そして肺体血流バランスの調整を試みる必要がある.酸素消費量の低下は鎮静・鎮痛・人工呼吸管理を必要に応じて選択することで調整する.ショック時には体血管抵抗は代償性に上昇しており,肺血流増加を助長している場合が多く,鎮静は極めて重要である.心拍出量増加は,輸液による前負荷増加・Inotropic Agentによる心収縮増加・心拍数増加を可能な範囲で調整することで心臓全体の拍出量増加を試みる.Inotropic Agentで強い末梢血管収縮作用を有する薬剤は避けることが望ましい.血流バランスは低濃度酸素吸入療法・末梢血管拡張療法を行い,体血流増加を試みる.
新生児期の循環管理では,肺血流増加によるショックを事前に予防し,安定した循環動態で手術につなげることが極めて重要である.すなわち,ショックを生じてからの対応では時すでに遅いことを自覚しておくことが重要である.例えば血液ガス所見悪化,血圧低下や徐脈が生じた時点では,病態の悪化はすでに進んでいることを示しており,血行動態変化を事前に予測して管理する必要がある.これらの管理を行うためには,人工呼吸管理・動脈ライン・中心静脈ライン(もしくはそれにかわるライン)等の速やかな集中治療を導入することが重要と考えられる.
新生児期の重症先天性心疾患においても,必要な集中治療管理を施行するために手技の習得は重要である.集中治療のために気管内挿管・人工呼吸管理・動脈ライン確保・CVライン確保・PIライン確保・尿カテーテル挿入といった基本的手技の他に,エコー・ドレナージ・非侵襲的陽圧換気(NIPPV)・一時的ペーシング等の習熟は日常的に必要となる.特に形態診断・循環管理の心エコー,頭蓋内評価のための頭部エコー,腹部臓器評価のための腹部エコーは新生児全身管理には必須と考えられる.
新生児期の循環動態が不安定である際は,多臓器へ悪影響を及ぼす可能性が高く,特に重症先天性心疾患の管理においては,循環動態だけでなく,呼吸状態・神経学的評価・栄養管理・感染防御等の全身的な病態を常に把握し,必要に応じて適切に対応しなければならない.また様々な先天奇形症候群の合併がある場合も多く,疾患に応じ遺伝相談を含めた対応が重要である.さらに新生児期は易感染・神経学的未熟性・高ビリルビン血症・他の先天奇形症候群の検索・周産期母子環境等の,様々な新生児期特有の生理的及び社会的課題に対応する必要がある.
新生児期の重症先天性心疾患の病態生理は固有の病態であることが多く,ゴールデンマニュアルはない.患者それぞれの病態生理を正確に評価し,血行動態変化を予測して適切に管理することで,安定した病態で外科的治療に向かうことができる.
This page was created on 2015-03-09T14:55:08.828+09:00
This page was last modified on 2015-03-23T21:17:18.295+09:00
このサイトは(株)国際文献社によって運用されています。