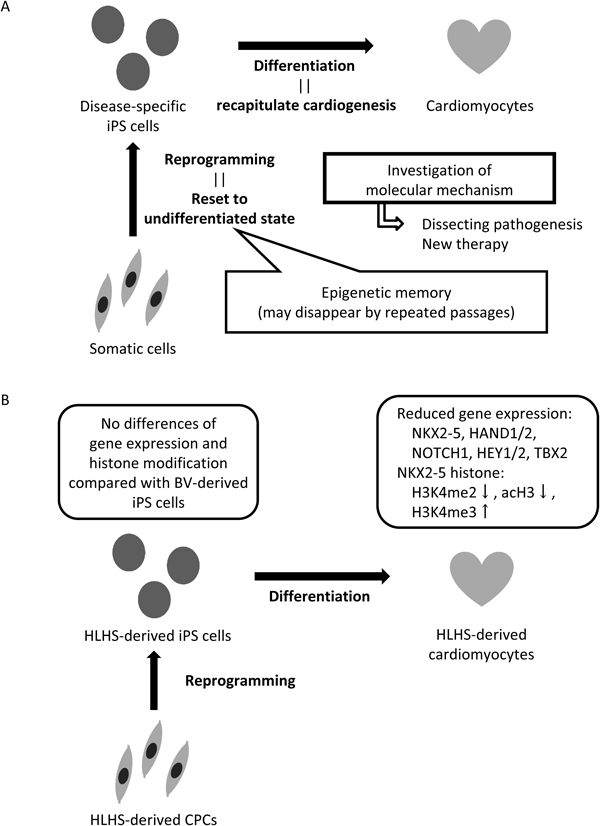
疾患特異的iPS細胞を用いた先天性心疾患の病態解明Congenital Heart Diseases and Disease-specific iPS Cells
1 岡山大学大学院医歯薬学総合研究科心臓血管外科学教室Department of Cardiovascular Surgery, Graduate School of Medicine, Dentistry and Pharmaceutical Sciences, Okayama University ◇ 〒700-8558 岡山県岡山市北区鹿田町二丁目5番1号2-5-1 Shikata-cho, Kita-ku, Okayama-shi, Okayama 700-8558, Japan
2 岡山大学病院新医療研究開発センター再生医療部Department of Regenerative Medicine, Center for Innovative Clinical Medicine, Okayama University Hospital ◇ 〒700-8558 岡山県岡山市北区鹿田町二丁目5番1号2-5-1 Shikata-cho, Kita-ku, Okayama-shi, Okayama 700-8558, Japan