心疾患の主診断(Fig. 1)
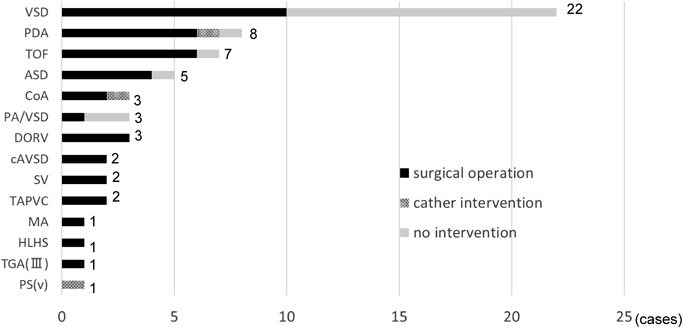
心疾患の主診断は心室中隔欠損22例,動脈管開存8例,Fallot四徴7例,心房中隔欠損5例,大動脈縮窄,肺動脈閉鎖兼心室中隔欠損,両大血管右室起始が各3例,完全型房室中隔欠損,単心室,総肺静脈還流異常が各2例,僧帽弁閉鎖,左心低形成症候群,完全大血管転位,肺動脈狭窄が各1例であった.61例中43例(70%)が心疾患に対する治療介入を必要としその内訳は,外科手術40例,カテーテル治療3例であった.カテーテル治療の内訳は肺動脈狭窄に対するバルーン拡大,大動脈縮窄に対するバルーン拡大,動脈管に対するコイル塞栓術が各1例であった.
合併消化管疾患
合併消化管疾患は鎖肛31例(51%),食道閉鎖17例(28%),十二指腸閉鎖・狭窄10例(16%),Hirschsprung病10例(16%)であった(重複あり).本院への紹介前に前医で消化管疾患の手術を受けていた例が9例あった.
消化管疾患の胎児診断(Fig. 2)
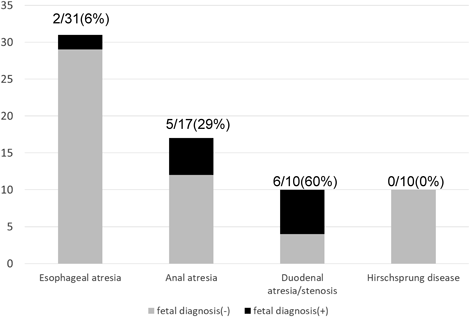
消化管疾患の胎児診断は,食道閉鎖5/17例(29%),鎖肛2/31例(6%),十二指腸閉鎖・狭窄6/10例(60%),Hirschsprung病0/10例(0%)でされていた(61例68疾患).院内出生が10/61例(16%)であった背景もあるが,十二指腸閉鎖・狭窄を除いて胎児診断例は少なく,診断率は全体で13/61例(21%)であった.しかし,院内出生に限ると8/10例(80%)であった.また心疾患の胎児診断率は,5/61例(8%)であった.院内出生に限っても3/10例(30%)と診断率は高くなかった.
染色体異常・奇形症候群
染色体異常等の全身性合併症を伴うものが31/61例(51%)あった.その内訳はDown症候群15例,VATER連合5例,CHARGE症候群3例で,22 trisomy 2例,その他46XYdel(11)(q23.3),47XY+mar, 9p−, Kabuki症候群,Treacher–Collins症候群,Coffin Siris症候群が各1例であった.
手術と治療経過
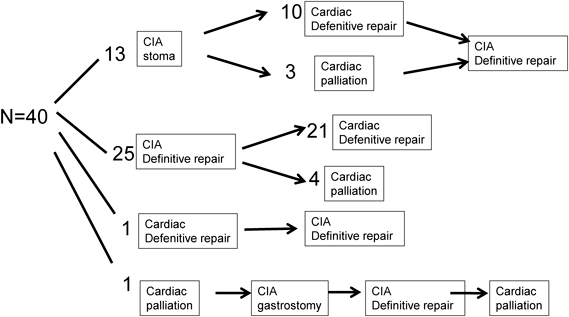
心疾患の初回手術時期は,日齢1~5歳(中央値3か月)で新生児期は18例であった.消化管疾患の初回手術時期は日齢0~2歳(中央値2日)であった.心疾患,消化管疾患ともに手術したものが40例(66%)でその治療経過をFig. 3に示す.内訳は1)消化管姑息手術→心臓手術→消化管根治術の順であったものが13例,2)消化管根治術→心臓手術が25例,3)心臓手術→消化管根治術が2例であった.38例は消化管疾患の手術を先行し,その後心臓手術を行っていた.
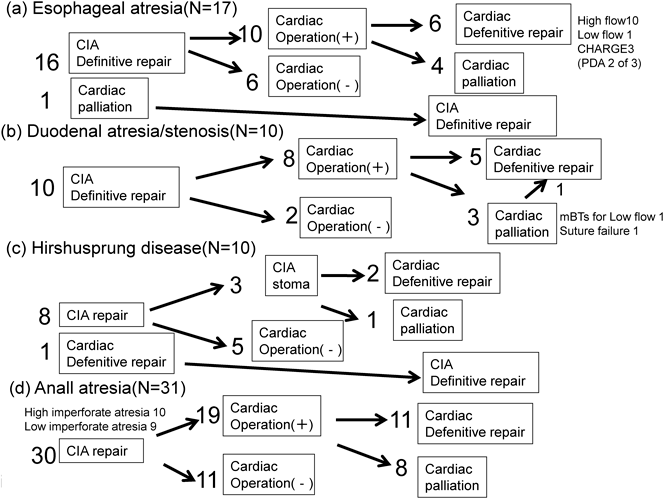
ここから,消化管閉塞症と先天性心疾患ともに手術を行なった40症例に関して消化管閉鎖症の疾患別にサブグループ(食道閉鎖,十二指腸閉鎖・狭窄,Hirschsprung病,鎖肛)に分けて検討する(Fig. 4).
食道閉鎖は17例中11例で,消化管と先天性心疾患ともに手術を行っていた.全例C型(下側の食道が気道につながっている)でありLong-gap症例はなかった.肺血流減少の心疾患は1例あり,Fallot四徴のために生後1か月時に修正Blalock–Taussig短絡術(BTシャント術)が必要であったが,消化管の創傷治癒に影響なく,感染性心内膜炎を呈することもなかった.肺血流増加の疾患が10例あったが,消化管手術後の経過は良好で経腸栄養が確立し,心臓手術を施行できた.CHARGE症候群が3例あり,うち2例の心疾患は動脈管開存症でともに新生児期に結紮術を施行した.胎児診断の1例で,当初の治療予定を関係診療科で見直す対応が必要となった.心疾患は大動脈縮窄,両大血管右室起始,左室低形成で,院内出生で消化管疾患,心疾患ともに胎児診断されていた.食道閉鎖と大動脈縮窄の同時手術はリスクが高いため,当初は食道閉鎖の手術後,状態が安定したところで大動脈縮窄の修復術を計画していた.しかし,出生後2時間で呼吸不全のため人工呼吸管理を要するとともに気管食道瘻のため腹部膨満が増強した.さらには,プロスタグランジンE1製剤の持続静注により,高肺血流による心不全が増悪,窒素ガス吸入による低酸素換気療法が必要となった.そのため,小児循環器,小児心臓外科,小児外科と協議のうえ日齢1に緊急避難的に両側肺動脈絞扼術と胃瘻増設を施行した.状態の安定を待って日齢3に食道閉鎖根治術を行い,日齢22にバルーン心房中隔裂開術,経腸栄養が確立した日齢26に大動脈縮窄修復術を施行した.しかしその後心臓カテーテル検査後の原因不明の低血糖のため重度の脳障害となりフォンタン手術まで到達できていない.肺血流増加型の心疾患10例のうち,CHARGE症候群の3例以外の7例は食道閉鎖の術後経過は良好で問題なく心疾患の管理ができた.その7例のなかで1例はDown症候群を合併した単心室の症例で,日齢1に食道閉鎖根治術を施行し術後経過は良好で2歳でFontan手術に到達した.
十二指腸閉鎖・狭窄は10例中8例で,消化管と先天性心疾患ともに手術を行っていた.全例で日齢10日以内に消化管手術を施行して概ね安定した状態で心疾患の手術を施行できた.完全大血管転位III型の1例でBTシャント術を施行したが,BTシャント術は消化管手術後の経過が落ち着き栄養の確立した生後4か月であった.そのため,BTシャント術の肺血流増加による消化管の術後への影響はなかった.一方心室中隔欠損症,大動脈縮窄症,Down症候群の1例で,日齢2に消化管手術を施行したが,日齢7に高肺血流のため腸管の縫合不全を合併し,状態が安定せず2,100 gと低出生体重児であり,日齢9に両側肺動脈絞扼術を施行した.その後,循環動態が安定し栄養を確立することができた.生後1か月で大動脈縮窄修復術と心内修復術を実施した.
Hirschsprung病は10例中4例で,消化管と先天性心疾患ともに手術を行っていた.3例が人工肛門を造設後,心臓手術を施行していた.1例は人工肛門を必要せず,消化管の状態が安定しており心室中隔欠損症と右室二腔症の心内修復術後に,消化管の根治術を施行していた.なお,2例が人工肛門を造設したDown症候群で,劇症型腸炎による急激な脱水を契機とした末梢循環不全のため急変,死亡した.
鎖肛(31例中19例)に関しては,概ね消化管手術後の経過は良好で経腸栄養が確立し,心臓手術を施行できた.高位鎖肛(10例)は,人工肛門を日齢1~6(中央値1)に造設し,8か月~2歳8か月(中央値1歳5か月)で消化管根治術を施行していた.また心疾患に対しては3例に姑息術を日齢3~8か月,7例に心内修復術を日齢48~2歳8か月(中央値1歳4か月)に施行していた.低位鎖肛(9例)では,日齢0~1(中央値1)に初回手術で消化管根治手術を施行し,心疾患の姑息術を5例で日齢1~10か月(中央値2か月)に,4例で心内修復術を2か月~1歳7か月(中央値5か月)に施行していた.BTシャント術を施行したFallot四徴症の症例が3例あったが,消化管術後の創傷治癒に影響することはなかった.ただ1例で人工肛門の位置が心臓手術に影響し,当初の治療予定を多科で見直す対応が必要であった.在胎36週6日,出生体重2,805 gで出生した.診断は両大血管右室起始,肺動脈弁狭窄,中位鎖肛,Kabuki症候群であった.日齢1に会陰式肛門形成術を施行したが,術後イレウスのため横行結腸人工肛門造設術を施行した.さらに術後腹腔内腸管穿孔のため,人工肛門はやむをえず胸部近くの上腹部に造設した.その後,肺血流増多による心不全症状が出現しその時点では,正中切開を要する心内修復は感染のリスクが高いと判断し,生後2か月でいったん左開胸で肺動脈絞扼術を施行し,体重増加を待って1歳3か月時に心内修復術を施行した.
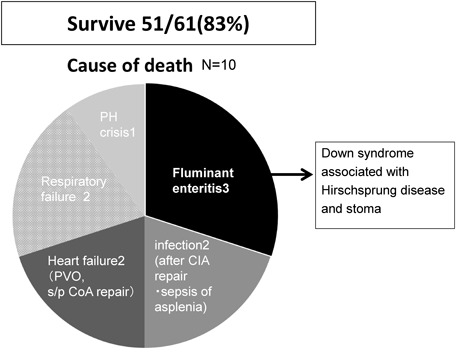
予後(Fig. 5)
全体の生存率は51/61例(83%)であった.死亡10例の死因は劇症型腸炎による脱水3例,感染2例,心不全2例,呼吸不全2例,肺高血圧クリーゼ1例であった.染色体異常は61例中31例(51%)であったが,死亡例10例の中では7例(70%)であった.消化管疾患が死因となったのは4例で,うち3例はHirschsprung病で人工肛門を造設したDown症候群で,死因は劇症型腸炎による急激な脱水を契機とした末梢循環不全であった(Table 1).3例とも胃腸炎発症から10~20時間以内に死亡するという非常に急激な経過を辿っていた.消化管疾患が死因となった4例の残り1例は食道閉鎖術後の敗血症であった.
Table 1 Three patients of fulminant enteritis with Hirschsprung disease and Down syndrome | Age | Heart disease | QpQs | Time from the onset of colitis to death | WBC (/µL) | CRP (mg/dL) |
|---|
| 1 | 11 m | VSD | 3.07 | 20 hr | 26,500 | 0.0 |
| 2 | 1y1m | s/p VSD closure | 1.05 | 12 hr | 16,900 | 1.56 |
| 3 | 1y11m | cAVSD, hypoplastic RV, s/pPAB | 1.21 | 10 hr | 5,000 | 11.15 |
| cAVSD, complete atrioventricular septal defect; PAB, pulmonary artery banding; VSD, ventricular septal defect. |
今回我々は,当施設での先天性消化管閉塞症を合併した心疾患の治療経過,予後を検討したが,関係診療科の連携のもと個々の症例に応じた治療計画を立てることで生存率83%であった.基本は消化管の手術を先行して,心疾患の手術を施行することで,従来の報告と同様の良好な結果が得られた.また,染色体異常・奇形症候群が半数あり死亡例の70%を占めていた.川田らは,食道閉鎖,鎖肛などの消化管病変を合併した心疾患75例のうち死亡例は10例と報告している1).また,遠隔予後を規定するのは,多くの場合心疾患そのものの重症度と考察している.Walkerらは,新生児の消化管手術を施行した18例の心疾患を対象とした検討を行い,死亡例は2例と報告している(左心低形成症候群と総動脈幹症,ともに死因は心不全)2).また,新生児死亡の原因に占める心疾患の割合は鎖肛では72.7%,食道閉鎖では10%を占めるという報告がある3).今回の我々の検討では,予後に関しては従来の報告とほぼ同様の成績であり,消化管疾患が死因となったのは4例のみであった.一方,今回の検討で死亡例10例のうち7例(70%)が染色体異常・奇形症候群を合併例であった.予後については,心疾患そのものよりも染色体異常・奇形症候群の存在の関与が大きいと推察された.
食道閉鎖は,VATER症候群として多発奇形を合併することが多い.Spitzらは重症心奇形の合併のみが食道閉鎖の独立した予後不良因子になるとして新しいリスク分類を提唱している4).食道閉鎖の問題点として陽圧換気による腹部膨満と消化液の逆流による誤嚥がある.胃食道逆流や気管食道瘻に起因する反復性誤嚥により生じる低酸素性肺血管攣縮は単独で高度の肺高血圧を生じ得ると村上らは述べている5).特に,Fontan手術を目指す心疾患で食道閉鎖を合併する症例では,早期に食道閉鎖の手術を施行し,慢性肺障害を防ぐ必要があるとしている.また,Long-gapで一期的に食道を吻合できない症例や染色体異常・奇形症候群など,嚥下障害を伴う症例でも誤嚥に起因する肺障害のため右心バイパス術を困難にする要因となる.さらに,食道閉鎖は開胸での消化管手術で不潔操作となるので,人工血管を用いる心臓手術を回避したいが,必要な時は,感染性心内膜炎への注意を払うべきである.
今回消化管疾患・心疾患とも緊急性を要した症例が1例あった.C型食道閉鎖,大動脈縮窄,両大血管右室起始,左室低形成,CHARGE症候群の例で,出生後,肺血流増多のために日齢1に緊急的に両側肺動脈絞扼術を施行し,循環動態を安定させたうえで日齢3に食道閉鎖根治術を行った.その後,日齢26に大動脈縮窄修復術を施行した.この症例は,食道閉鎖根治術前に肺血流量適正化のための心臓手術が必要であった.麻生らは,胎児診断された症例で24時間以内の超緊急手術例が多く施行できるようになっており,出生前より消化管疾患・心疾患に対して個々の症例に応じた介入を計画し,準備できるので,出生前診断は有用であると報告している6).しかし今回の検討では,消化管疾患の胎児診断例が13/61例(21%)と未だに少なく,改善が必要である.
十二指腸閉鎖・狭窄疾患に関して,1例で新生児期に心室中隔欠損症・大動脈縮窄症の高肺血流による縫合不全があり両側肺動脈絞扼術を施行した症例があった.なお,BTシャント術後に十二指腸手術後の創傷治癒に影響した症例はなかった.肺血流を動脈管に依存する例やBTシャント術後例で,特に高肺血流に傾く症例では拡張期血圧が低下し腸管血流が低下する.そのような病態では,消化管手術後の創傷治癒に影響し壊死性腸炎やイレウス,縫合不全などの合併症への注意が必要である.
村上らは,上腹部の人工肛門の存在は胸骨正中切開後の縦隔洞炎のリスクを高めると述べている5).今回,我々が経験した人工肛門の位置が心臓手術に影響した両大血管右室起始・肺動脈弁狭窄・中位鎖肛の症例は,消化管疾患の緊急性のため,人工肛門を正中近くに造設せざるをえなかった.正中切開を要する心内修復では感染のリスクが高く,いったん左開胸で肺動脈絞扼術を施行し,体重増加を待ち鎖肛根治術,人工肛門閉鎖後に心内修復術を行った.高位鎖肛で人工肛門を造設後に開心術を行う場合には人工肛門造設の位置を通常より下方もしくは正中より遠ざける工夫が必要と考えられた.
消化管疾患が死因となった症例は4例あった.特筆すべき点は,うち3例は急性胃腸炎で,全例Hirschsprung病で人工肛門を造設したDown症候群であったことである.いずれも胃腸炎発症から10~20時間以内に死亡するという劇症型の経過を辿っていた.死因は劇症型腸炎による急激な脱水を契機とした末梢循環不全であった.池田らは,Hirschsprung病にDown症候群と心奇形を同時に合併すると死亡率が38.1%と高率になると報告している7).Teitelbaumらは,80人のHirschsprung病の患児を対象とし,腸炎の合併率についてDown症候群13例と非Down症候群67例とで比較し,Down症候群は46%,非Down症候群は19%と有意差を認めると報告している8).Hirschsprung病の術前腸炎は,Hirschsprung病の早期診断および早期手術により,その頻度および死亡例は経年的に著明に減少している9).しかし,Hirschsprung病で人工肛門を造設したDown症候群が腸炎を発症した時は,急激な脱水を契機とした末梢循環不全の発症を念頭において診療にあたることが重要である.特に,肺血流増加型の心疾患のように体血管血流量が不十分な病態では腸管循環が悪化し腸管蠕動が低下することで,劇症型腸炎の悪化が急速である可能性が高いので十分に注意することが重要である10).