妊娠経過
在胎18週0日,一絨毛二羊膜双胎,切迫流産のため他院より当院へ紹介された.在胎18週6日,TTTS,切迫流産,子宮頚管無力症のため入院管理とした.在胎19週1日,頸管長の短縮を認めマクドナルド手術を施行した.在胎19週4日,受血児に心拡大,腹水,皮下水腫が出現した.TTTS, Quintero StageIVと診断し胎児治療のため転院した.転院後,受血児に重度のMR,重度の三尖弁閉鎖不全(tricuspid regurgitation; TR)を指摘された.心胸郭断面積比(cardiothoracic area ratio; CTAR)61%で最大羊水深度は受血児12.5 cm,供血児0.8 cmであった.在胎19週5日,9本の吻合血管に対してFLPを施行した.在胎22週3日,最大羊水深度は受血児8.7 cm,供血児4.6 cm,重度のMR, TRは持続した.在胎23週3日,受血児の心嚢水,腹水は軽減した.在胎25週3日,最大羊水深度は受血児4.0 cm,供血児4.0 cmと羊水量の差はなくなったが,CTAR50%で重度のMR, TRは持続した.在胎27週0日,周産期管理のため当院へ母体搬送された.
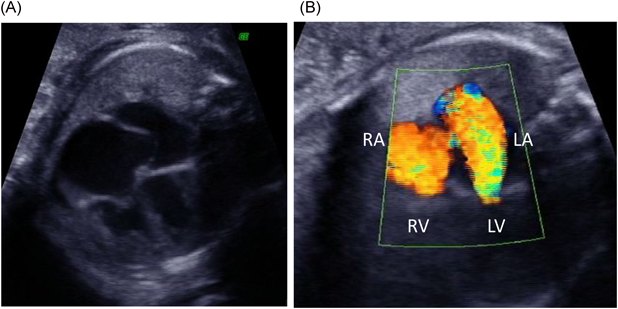
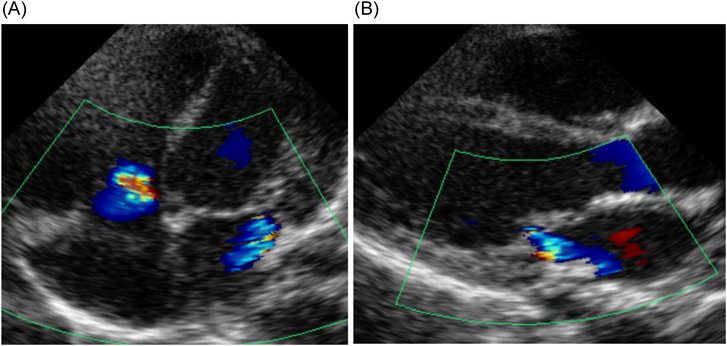
胎児心臓超音波検査ではCTAR47%,心横径ϕ35.6 mm,心拍数148 bpm,四腔は著明に拡大,右室壁の肥大を認め,僧帽弁輪径11.2 mm, MR重度,三尖弁輪径10.4 mm, TR重度,左室駆出率(Left ventricular ejection fraction; LVEF)50%であった(Fig. 1).肺動脈弁の狭窄はなく,動脈管,卵円孔の閉鎖は認めなかった.また,供血児はCTAR29%,心横径28.0 mmと週数相当であり房室弁逆流を認めなかった.在胎週数が早く,FLP後のため房室弁逆流が改善する可能性に期待し経過観察とした.分娩時期に関しては,供血児に異常がないため供血児を優先して判断する方針とした.経過中,胎児のnon-stress test(NST)では両児ともにreassuring patternで,臍帯血流の途絶が見られず観察を続けることができた.出生前の弁輪径とCTARの推移は在胎28週1日,僧帽弁輪径12.4 mm,三尖弁輪径14.1 mm.在胎29週5日,僧帽弁輪径12.9 mm,三尖弁輪径13.3 mmで在胎32週1日,僧帽弁輪径12.3 mm,三尖弁輪径13.6 mm, CTAR47%であり,重度のMR, TRは持続した.在胎32週4日,前期破水のため帝王切開とした.
出生後経過
患児はMask & bagによる酸素投与後も心拍数60 bpmの徐脈が遷延したため気管挿管し,回復した.Apgar scoreは1分3点,5分3点でNICUに入院した.
入院時所見
身長43.5 cm,体重1,742 g,血圧42/26 mmHg,心拍数150 bpm,呼吸数50回/分,経皮的酸素飽和度96%(吸入酸素濃度100%下),浮腫は軽度で正常新生児相当,肝臓を3横指触知した.胸部聴診所見では心尖部にLevine2/6度の収縮期雑音に加え拡張期ランブルを聴取した.
入院時検査所見
血液生化学検査:脳性ナトリウム利尿ペプチド(brain natriuretic peptide; BNP)1155.5 pg/mL, Hb 15.0 g/dL, Ht 47.5%(双胎供血児はHb 15.9 g/dL, Ht 49.8%で2児間に差を認めなかった.)
酸素100%投与下での静脈血液ガス:pH 7.256 pCO2 44.6 mmHg pO2 79.1 mmHg sO296.7% HCO3 −19.2 mmol/L ABE −7.5 mmol/L Lac 40.0 mg/dL
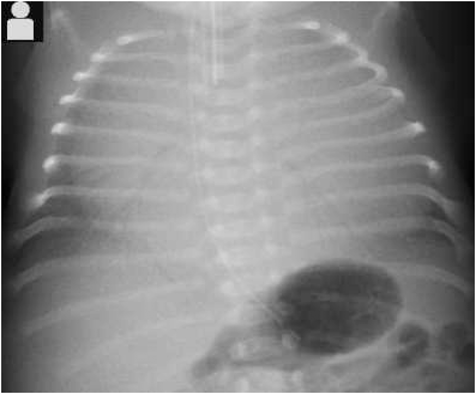
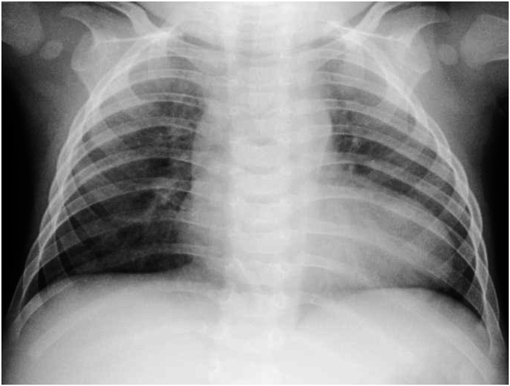
胸部X線:心胸郭比80.3%,Bomsel分類IV度(Fig. 2)
心電図:心拍数152/分,軸35度,両心房負荷,両心室肥大(Fig. 3)
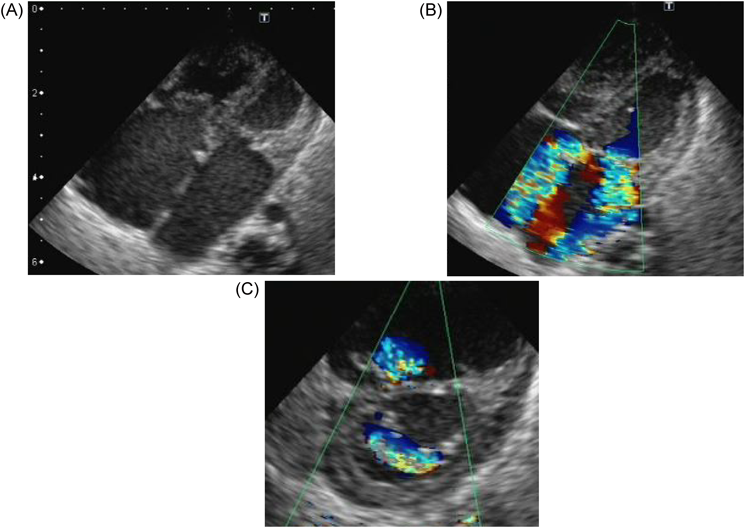
心臓超音波検査:僧帽弁輪径10.8 mm,僧帽弁に肥厚(A1–A3, P2)と前尖(A2)に軽度の逸脱あり,MR重度でA1からA3まで幅広く認め左心房後壁へ向かう,乳頭筋は2つ認め腱索に断裂なし,左室流入血流E/A=0.86/1.0 m/s,三尖弁輪径12.7 mm, TR重度で接合不全を認め中央部から後方かつ中隔側へ向かう(Fig. 4),推定右室圧66.0 mmHg, LVEF 57.8%,左室拡張末期径(left ventricular end-diastolic dimension; LVDd)16.5 mm,左室壁厚2.9 mm,動脈管径1.5 mmで左右短絡,冠動脈起始異常なし.
入院後経過
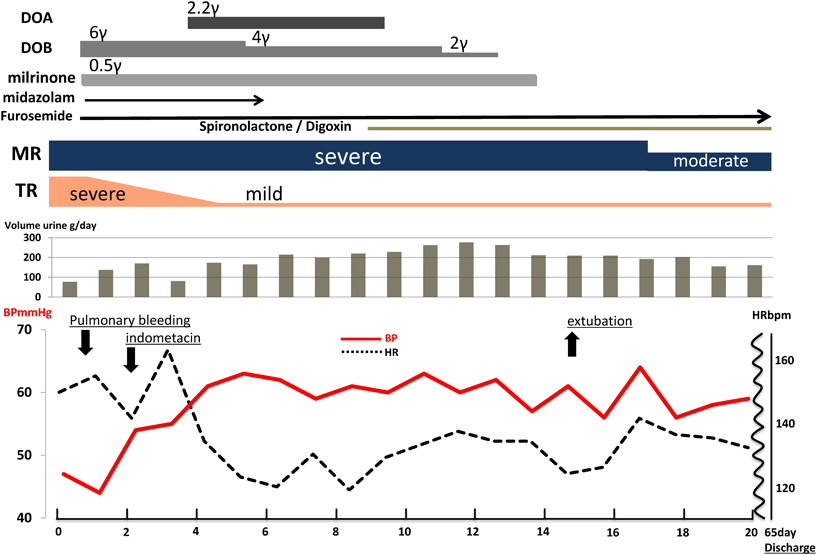
マイクロバブルテストはweakで,新生児呼吸窮迫症候群(respiratory distress syndrome; RDS)と診断しサーファクタントを2バイアル気管内投与した.水分制限,人工換気,酸素吸入,ドブタミン,ミルリノンで治療を開始した(Fig. 5).
日齢1:啼泣後に大量の肺出血を生じ,酸素飽和度が90%に低下した.ミダゾラムの持続点滴で鎮静を行い呼吸状態は安定した.その後肺出血は見られず酸素を減量した.
日齢2:重度のMR, TRは持続しLVDd 22.4 mm,僧帽弁輪径10.2 mm,三尖弁輪径13.4 mm,推定右室圧52.9 mmHg(体血圧50 mmHg前後)であった.動脈管径が1.8 mmと拡大し,左右短絡量増加,左房径は29.4×28.3 mmに拡大した.そのため動脈管の閉鎖による左室容量負荷軽減を目的に,インドメタシン0.2 mg/kgを投与した.
日齢3:動脈管の閉鎖を確認しLVDd 20.7 mm,推定右室圧40 mmHg(体血圧60 mmHg前後)と改善傾向となった.
日齢4:MR重度と不変も左房径15.9×18.8 mmと縮小,僧帽弁輪径10.8 mm,三尖弁輪径12.8 mm, LVDd 20.3 mm,推定右室圧22.8 mmHg,TR軽度と軽快した.フロセミドの静注では尿量が乏しく,腎血流量増加目的でドパミンの点滴を開始し,以後尿量は増加し安定した.
日齢5:経管栄養を開始し,以降は徐々に増量した.
日齢7:水分制限を解除し鎮静を中止した.
日齢8:体重1,402 gで,以後,体重増加傾向となった.
日齢17:僧帽弁輪径10.0 mm, LVDd 18.5 mm, MRは中等度に改善し,左室・左房拡大が軽減した.
日齢24:酸素吸入を中止した.
日齢36:BNP=7.2 pg/mLと正常化した.
日齢43:僧帽弁輪径11.8 mm, LVDd 20.8 mm, MRは軽度に改善.
日齢50:利尿剤を中止した.
日齢65:体重3,448 gで退院した.
生後6ヶ月の胸部X線では心胸郭比63.0%と改善した(Fig. 6).生後9ヶ月時にMRは軽度と悪化なく,心機能良好のため,ジゴキシンの内服を中止した.1歳時の心臓超音波検査では僧帽弁の両尖に肥厚と前尖(A2)に軽度逸脱を認め,MR軽度でA2と前交連より吹く,TR軽度,LVEF 72.2% LVDd 24.6 mm(Fig. 7)と悪化なく,発達も正常で外来経過観察中である.
なお,双胎供血児はMask & bagによる酸素投与で回復した.出生体重1,668 gで,Apgar scoreは1分8点,5分9点であった.胸部X線上Bomsel分類II度のRDSと診断し気管内挿管の上,サーファクタントを2バイアル気管内投与した.日齢1に人工換気から離脱し,日齢34に体重2,452 gで退院した.
本症例は次の2点が興味深い.1点目はFLP後に羊水量の差と胎児水腫は改善したが,胎児期の重度MR, TR,心拡大が残存したこと.2点目は胎児期に改善しなかったMRが出生後の治療で改善したことである.
一般的に受血児に認められる頻度の高い異常は,心室肥大(18~49%),CTARの増大(47%),心室の拡張(17~31%),TR(35~52%),MR(6~15%)で,まれな異常としては肺動脈狭窄や肺動脈閉鎖が報告されている1–4).
TTTS受血児に生じるMRは容量負荷による機能的な逆流と考えられる.しかし,本症例は容量負荷が消失したFLP後もMRは改善しなかった.MRは出生後の評価でA1からA3と幅広く吹き機能的な逆流を示唆されたが,僧帽弁に肥厚(A1–A3, P2)と前尖(A2)に逸脱所見があり,器質的な異常も疑われた.LosadaらはTTTSの経過で受血児に異常僧帽弁弧を生じたと報告した6).この報告ではTTTS11組の剖検例より受血児4例に異常僧帽弁弧を認め,うち3例はTTTS初期の胎児心臓超音波検査で正常な四腔断面像,僧帽弁であったと報告している.経過中に僧帽弁は次第に厚くなり小葉の可動性が低下しMRの進行が確認された.この異常な僧帽弁は発生停止ではなく乱流関連で生じた後天性奇形である可能性を考察している.また,胎児期にMRを生じさせる機序として血管作動性ペプチドが関与している可能性もある.TTTS受血児の心機能不全と血管作動薬のEndothelin-1, BNP値の上昇が相関したとの報告がある7).特にEndothelin-1は,心臓を含むさまざまな器官で線維化を促進することが示されている.これは,血管作動性のペプチドが二次的に弁病変を生じさせる可能性を考察している.
出生時MR, TRは双方重度であったが,LVEFは保たれていた.TRは出生後,胎児循環からの離脱により改善を認めた.MRは,強心剤,血管拡張薬,水分制限の後に動脈管の閉鎖,呼吸状態や肺高血圧の改善を起点に軽快した.本症例を顧みると左室容量負荷の軽減のため,早期の動脈管閉鎖が望ましいと考えた.HerbergらはFLP後に生存したTTTS双胎について後方視的に検討し,重症度の高い受血児においても,MR, TR,収縮能,拡張能が長期にわたり正常化したことを報告した5).
本症例は,啼泣により肺高血圧が増強し肺出血を生じたため,重度のMRがある場合は鎮静剤の使用を含めた注意深い管理が必要である.
娩出時期については議論となったが,初診時,在胎27週と未熟であり,FLP後のため改善の期待があること,供血児に異常所見がないことから早期娩出は躊躇われた.経過中,両児ともにNSTはreassuring patternで,臍帯血流の途絶なく観察を続けることができた.結果的には前期破水のため32週で出生に至ったため,分娩時期の適切な時期を検討することはできなかった.また,受血児に生じた重度のMRがFLP後,満期まで観察することで,改善が見られた可能性についても評価できなかった.胎内でMRが改善せず,胎児の状態が悪くなるようなら,本症例のように生後の治療に期待するのも考慮してもよいかもしれない.