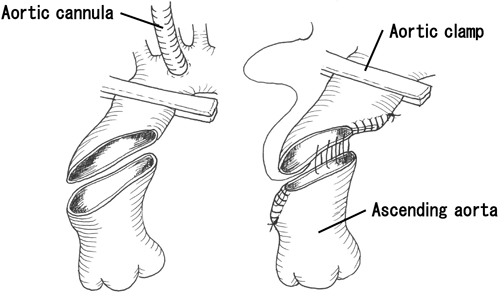
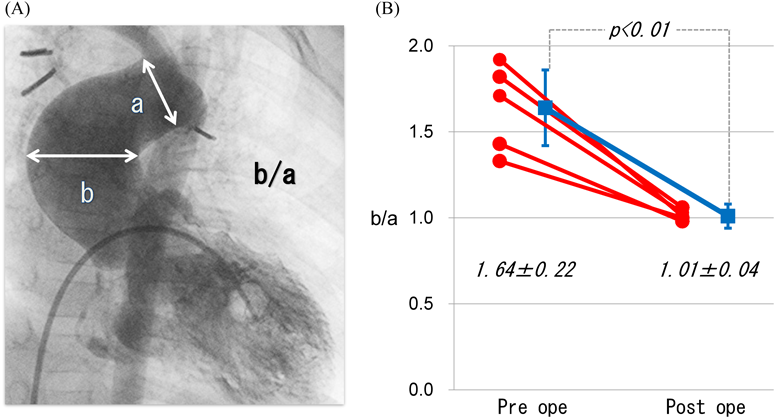
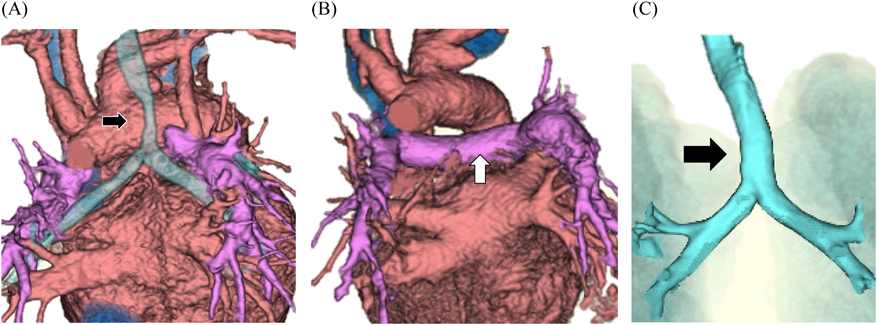
大動脈弓下狭小例に対する自己組織によるascending aortic extension法の中期遠隔成績:5例の経験Mid-term Results of an Ascending Aortic Extension and Plication Technique for Narrowing the Retroaortic Space: Five Cases
1 独立行政法人地域医療機能推進機構 中京病院こどもハートセンター心臓血管外科Department of Cardiovascular Surgery, Chukyo Children Heart Center, Japan Community Healthcare Organization Chukyo Hospital ◇ Aichi, Japan
2 独立行政法人地域医療機能推進機構 中京病院こどもハートセンター小児循環器科Department of Pediatric Cardiology, Chukyo Children Heart Center, Japan Community Healthcare Organization Chukyo Hospital ◇ Aichi, Japan
3 豊橋市民病院心臓外科Department of Cardiac Surgery, Toyohashi Municipal Hospital ◇ Aichi, Japan